Clear Sky Science · es
Diversidad genética de Pseudomonas aeruginosa aislada de muestras clínicas mediante el marcador molecular ISSR en un hospital universitario de atención terciaria
Por qué los gérmenes hospitalarios nos importan a todos
Cualquiera que haya pasado tiempo en un hospital—ya sea como paciente o visitando a un familiar—depende de que los antibióticos funcionen cuando más se necesitan. Pero algunos gérmenes se están volviendo tan resistentes que incluso nuestros fármacos más potentes tienen dificultades para detenerlos. Este artículo explora a uno de esos agentes problemáticos, una bacteria llamada Pseudomonas aeruginosa, y muestra cómo científicos de un hospital indio cartografiaron su variedad genética oculta para entender mejor por qué es tan difícil de controlar.
Un germen persistente en los hospitales modernos
Pseudomonas aeruginosa es un adversario escurridizo. Prospera en ambientes húmedos, desde tubos de ventilación hasta apósitos de heridas, y ataca sobre todo a personas con defensas debilitadas por enfermedad, quemaduras o estancias hospitalarias prolongadas. Puede causar infecciones graves en pulmones, sangre, vías urinarias y heridas. Lo que la hace especialmente peligrosa es su capacidad para resistir múltiples antibióticos a la vez, convirtiendo infecciones rutinarias en crisis potencialmente mortales y aumentando los costos de tratamiento y las estancias hospitalarias en todo el mundo.
Mirar debajo de la superficie de la infección
Para ver cuán diversa es realmente esta bacteria dentro de un mismo hospital, los investigadores recogieron 100 muestras bacterianas de sangre, orina, esputo y hisopos de heridas obtenidos durante la atención rutinaria en un gran hospital universitario del este de la India. Se centraron en 18 cepas resistentes a múltiples fármacos y evaluaron cómo reaccionaba cada una frente a un amplio panel de antibióticos. Preocupantemente, más de cuatro de cada cinco muestras eran resistentes a medicamentos clave como cefoperazona, meropenem e imipenem—fármacos a menudo reservados como última línea cuando otros fallan. Algunos antibióticos, incluidos algunos menos usados, aún funcionaron mejor, lo que sugiere opciones terapéuticas remanentes pero cada vez más limitadas. 
Leer los “códigos de barras” de las bacterias
Contar qué fármacos fallaban fue solo la mitad de la historia. El equipo también quiso saber si estas infecciones provenían de una única “supercepa” exitosa que se propagaba por el hospital, o de muchas linajes no relacionados que llegaban y evolucionaban de forma independiente. Para ello usaron un enfoque de huella genética llamado ISSR, que resalta los fragmentos de código genético situados entre secuencias cortas repetidas. Cuando se amplifican por PCR y se separan en un gel, estos fragmentos forman un patrón de bandas que actúa como un código de barras para cada cepa. Con 17 cebadores informativos, los investigadores generaron 95 bandas de ADN distintas y luego compararon los patrones entre las 18 cepas mediante herramientas informáticas que agrupan huellas similares.
Muchos primos lejanos, no un superbacterio único
Las comparaciones genéticas revelaron que el hospital no estaba lidiando con un clon descontrolado. En cambio, las cepas se agruparon en varios clústeres distintos, con puntuaciones de similitud que iban desde parientes bastante cercanos hasta primos muy distantes. Algunos aislados que se comportaron de forma similar en las pruebas de sensibilidad resultaron genéticamente diferentes, mientras que otros relacionados compartían elementos de resistencia. Los diagramas de componentes principales y los árboles reforzaron el panorama de múltiples linajes coexistiendo en la misma instalación en lugar de una cepa dominante que se expandiera. Esta diversidad probablemente surge a medida que las bacterias intercambian genes, mutan y se adaptan bajo la exposición constante a antibióticos y al sistema inmunitario humano. 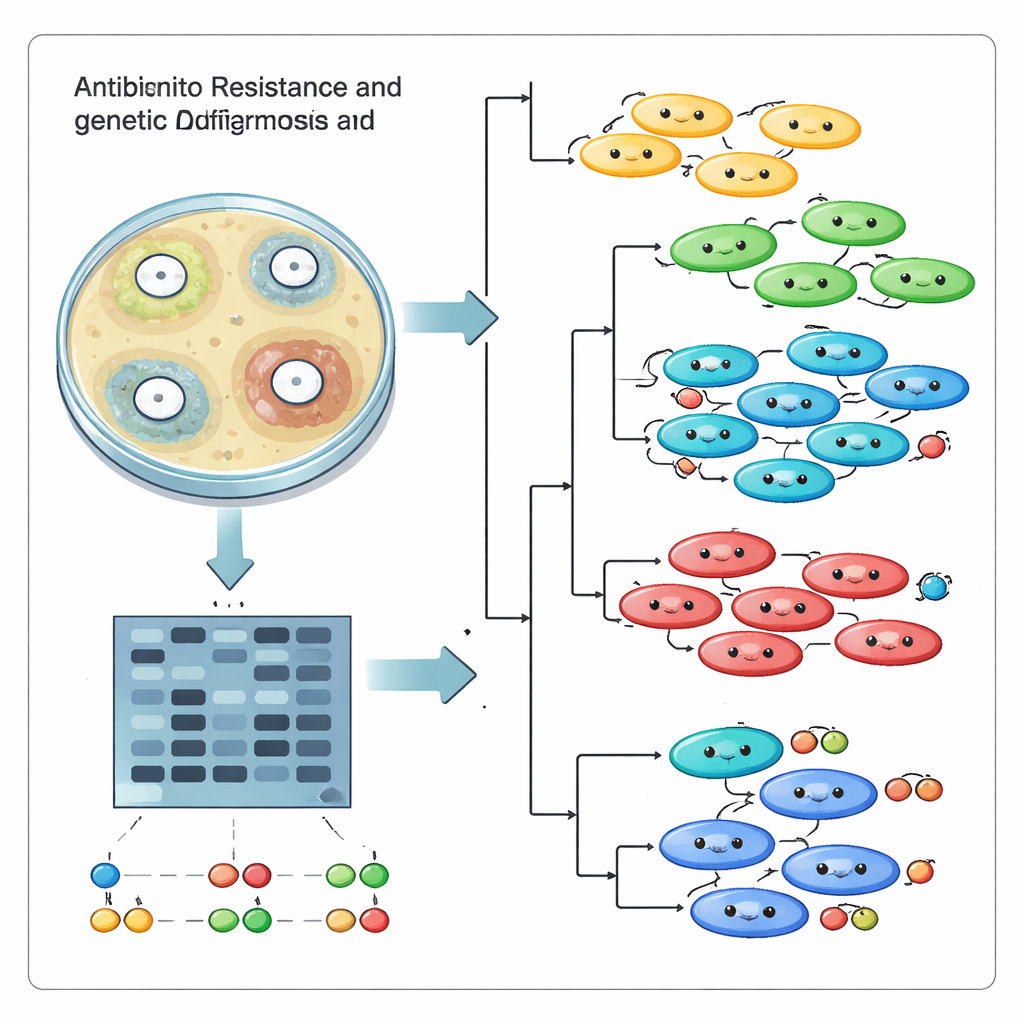
Qué significa esto para pacientes y hospitales
Para los hospitales, estos hallazgos transmiten un mensaje claro: rastrear solo qué antibióticos fallan no es suficiente. Dado que cepas genéticamente distintas pueden compartir patrones de resistencia similares—y las muy relacionadas pueden comportarse de forma diferente—los equipos sanitarios necesitan tanto pruebas rutinarias de sensibilidad a los fármacos como vigilancia genética periódica para ver cómo cambia la población bacteriana con el tiempo. El enfoque ISSR empleado aquí es relativamente simple y de bajo coste, lo que lo hace atractivo en entornos con recursos limitados, aunque los autores subrayan que combinarlo con secuenciación del genoma completo en estudios futuros ofrecería una visión más completa.
Un paisaje oculto que exige vigilancia
En términos sencillos, este estudio muestra que dentro de un único hospital, Pseudomonas aeruginosa no es un único enemigo, sino una multitud de alborotadores relacionados pero distintos, muchos ya armados contra varios antibióticos. Al cartografiar este paisaje oculto de diversidad, los investigadores proporcionan herramientas y conocimientos que pueden ayudar a los médicos a elegir tratamientos más dirigidos y a los equipos de control de infecciones a diseñar estrategias de contención más inteligentes. La vigilancia continua de estos patrones genéticos será esencial para adelantarse a este germen adaptable y mantener la atención hospitalaria segura para los pacientes.
Cita: Mishra, P., Sahoo, D. & Sahu, M.C. Genetic diversity of Pseudomonas aeruginosa isolated from clinical samples with ISSR molecular marker in a tertiary care teaching hospital. Sci Rep 16, 5315 (2026). https://doi.org/10.1038/s41598-026-35090-8
Palabras clave: Pseudomonas aeruginosa, resistencia a los antibióticos, infecciones hospitalarias, diversidad genética, tipificación molecular