Clear Sky Science · es
La fórmula Shen-Shuai-II inhibe la glucólisis aeróbica a través de SIRT1 en un modelo de insuficiencia renal por ablación/infarto 5/6
Por qué importa este estudio renal
La enfermedad renal crónica afecta a millones de personas en todo el mundo y con frecuencia conduce a la cicatrización irreversible del riñón, denominada fibrosis. Los fármacos actuales ralentizan el daño pero rara vez lo detienen. Este estudio explora cómo una fórmula herbal tradicional china, Shen‑Shuai‑II‑Recipe (SSR), podría proteger los riñones al reajustar suavemente la forma en que las células renales usan la energía, ofreciendo pistas para nuevas formas de tratar el daño renal a largo plazo.
Células renales hambrientas de energía bajo estrés
Nuestros riñones están llenos de pequeños túbulos que filtran la sangre y regulan sales y agua de forma continua. Estas células tubulares normalmente queman grasa de manera eficiente para obtener la energía que necesitan. En la enfermedad renal crónica, las lesiones repetidas las empujan a un modo distinto: comienzan a degradar azúcar muy rápidamente, un proceso llamado glucólisis aeróbica. Esta estrategia de emergencia ayuda a la supervivencia a corto plazo pero produce exceso de ácido láctico y está estrechamente relacionada con la formación de cicatrices en el riñón. Los autores señalan que este cambio metabólico aparece en muchas formas de daño renal y hoy se considera un factor clave en la progresión de la fibrosis.
Una fórmula tradicional puesta a prueba
Para investigar cómo actúa SSR, los investigadores usaron un modelo de rata bien establecido de daño renal severo llamado modelo de ablación/infarto 5/6, en el que se elimina o bloquea quirúrgicamente la mayor parte del tejido renal. Tras la lesión, las ratas recibieron SSR, el fármaco para la presión arterial losartán (un tratamiento estándar) o ningún tratamiento activo durante ocho semanas. La función renal se siguió con pruebas sanguíneas y de orina habituales, y el tejido renal se examinó al microscopio y mediante mediciones proteicas. Las ratas que recibieron SSR o losartán mostraron niveles más bajos de productos de desecho en sangre y menos proteína en orina que las ratas no tratadas, lo que indica mejor función renal. Las tinciones del tejido mostraron menos acumulación de colágeno y menos signos de fibrosis en los grupos tratados, con SSR aliviando claramente el daño estructural.
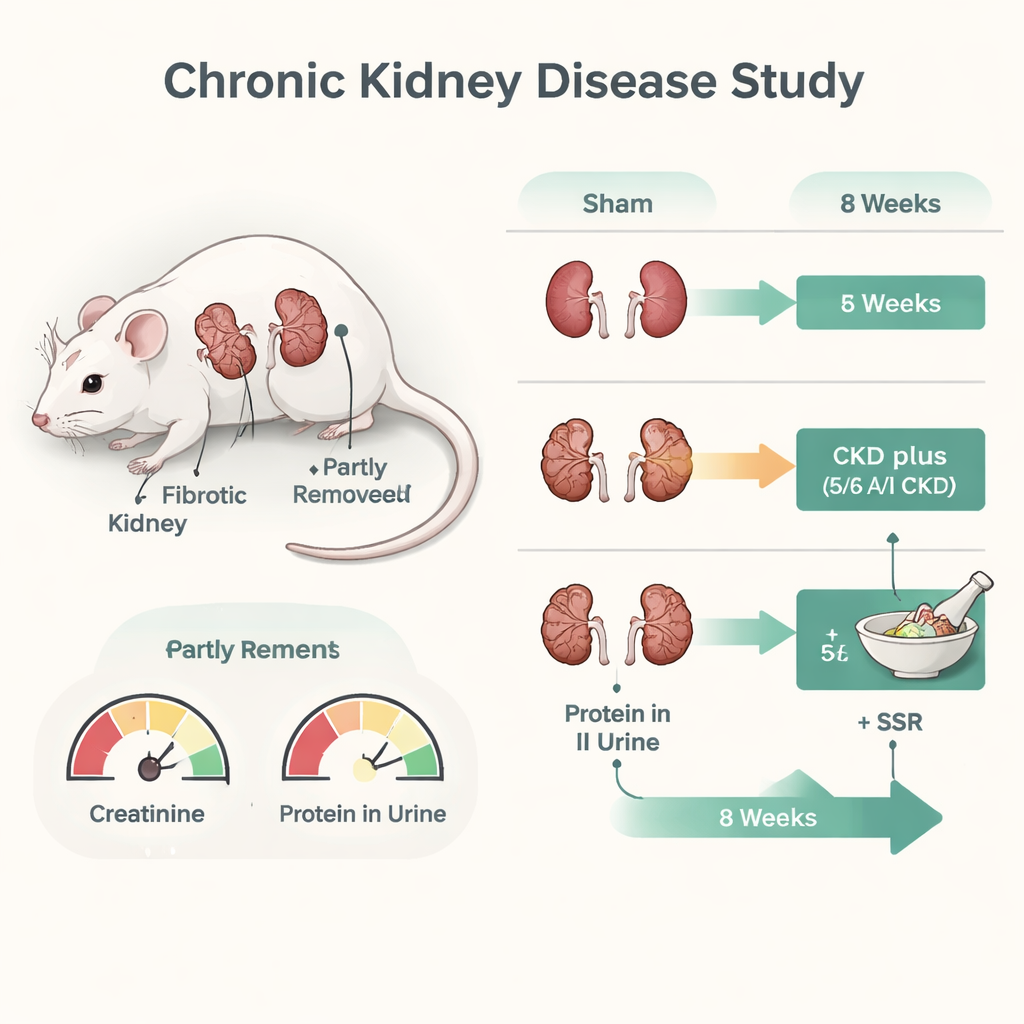
Reduciendo la quema de azúcar en riñones dañados
El equipo se centró entonces en el metabolismo energético dentro de las células renales. En los riñones dañados, los niveles de enzimas clave de la glucólisis, como HK2 y PFKFB3, estaban elevados, y los niveles de ácido láctico eran más altos mientras que el ácido pirúvico era menor —marcadores de una glucólisis sobreactivada. El tratamiento con SSR revirtió estos cambios: las enzimas relacionadas con la glucólisis disminuyeron, los niveles de ácido láctico cayeron y el equilibrio de metabolitos se desplazó hacia un estado más sano. Efectos similares se observaron en células tubulares renales de rata cultivadas expuestas a bajo oxígeno en el laboratorio, lo que imita el entorno crónicamente pobre en oxígeno de los riñones enfermos. Bajo hipoxia, estas células se volvieron más fibróticas y glucolíticas, pero el suero de animales tratados con SSR redujo las proteínas fibróticas, disminuyó la actividad glucolítica y preservó la glucosa en el medio de cultivo.
Un interruptor molecular: SIRT1 y HIF‑1α
Los investigadores se centraron en dos reguladores moleculares que vinculan los niveles de oxígeno con el metabolismo: SIRT1, una enzima que detecta el estado energético de la célula, y HIF‑1α, un factor de transcripción que activa genes de la glucólisis bajo bajo oxígeno. En los riñones de ratas enfermas y en células renales hipóxicas, los niveles de SIRT1 disminuyeron mientras que HIF‑1α aumentó. El tratamiento con SSR elevó SIRT1 y suprimió HIF‑1α, en paralelo con la reducción de la glucólisis y la fibrosis. Para probar si SIRT1 era esencial para los beneficios de SSR, el equipo empleó ARN de interferencia pequeño para reducir SIRT1 en células renales. Cuando SIRT1 fue silenciado, SSR ya no pudo disminuir HIF‑1α, las enzimas de la glucólisis, la acumulación de ácido láctico ni los marcadores fibróticos. Esto indica que SIRT1 es un interruptor central a través del cual SSR ejerce sus efectos protectores.
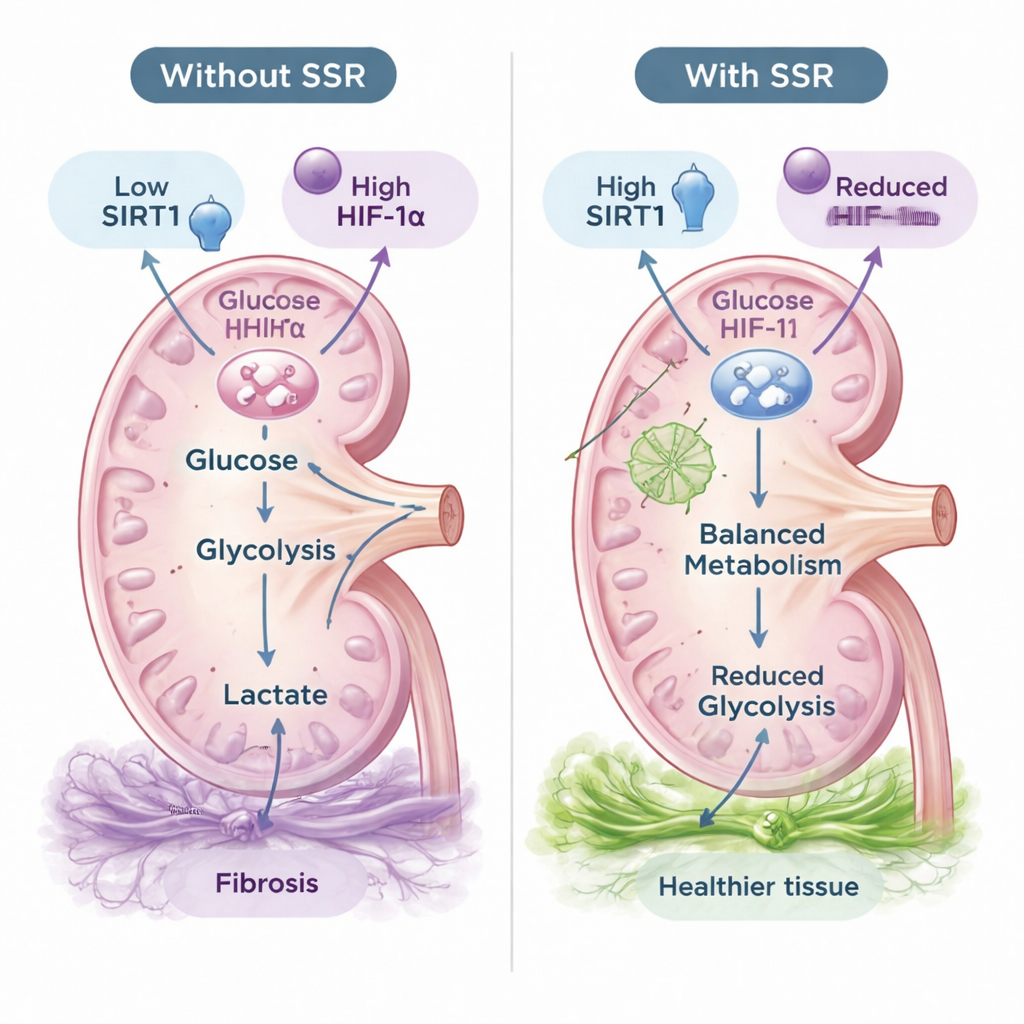
Qué podría significar para futuros tratamientos
Los autores proponen que SSR actúa como un “reprogramador metabólico” multicomponente para el riñón: al potenciar SIRT1 y mantener HIF‑1α bajo control, evita que las células tubulares queden atrapadas en un estado dañino de alta glucólisis y frena la acumulación de tejido cicatricial. Varios ingredientes conocidos de SSR ya se han relacionado individualmente con la activación de SIRT1 y con un mejor control del uso de azúcares en otros órganos. En conjunto, pueden actuar de forma sinérgica en el riñón. Aunque este trabajo se realizó en ratas y cultivos celulares y todavía no demuestra beneficio clínico, pone de relieve el metabolismo energético —y específicamente el eje SIRT1/HIF‑1α— como un objetivo prometedor. En términos sencillos, ayudar a las células renales a usar el combustible de forma más inteligente puede ser una de las claves para ralentizar, o algún día detener, la cicatrización renal crónica.
Cita: Lan, T., Zhang, X., Lyu, X. et al. Shen-Shuai-II-Recipe inhibits aerobic glycolysis through SIRT1 in 5/6 ablation/infarction renal failure model. Sci Rep 16, 5022 (2026). https://doi.org/10.1038/s41598-026-35061-z
Palabras clave: enfermedad renal crónica, fibrosis renal, metabolismo energético, glucólisis aeróbica, medicina tradicional china