Clear Sky Science · es
Estructura cristalina de la cistatina B de Echinococcus multilocularis revela una característica novedosa en las stefinas clásicas
Por qué importa el arma secreta de un parásito hepático
La echinococosis alveolar es un nombre largo para una infección por una pequeña tenia que se comporta de forma muy parecida a un cáncer de crecimiento lento en el hígado. Suele ser mortal, y los fármacos actuales funcionan mal y pueden provocar efectos secundarios graves. Este estudio analiza una molécula concreta producida por el parásito, una proteína llamada EmCystatin-B, para entender cómo podría ayudar al gusano a eludir nuestras defensas y cómo algún día podría convertirse en diana para nuevos tratamientos.
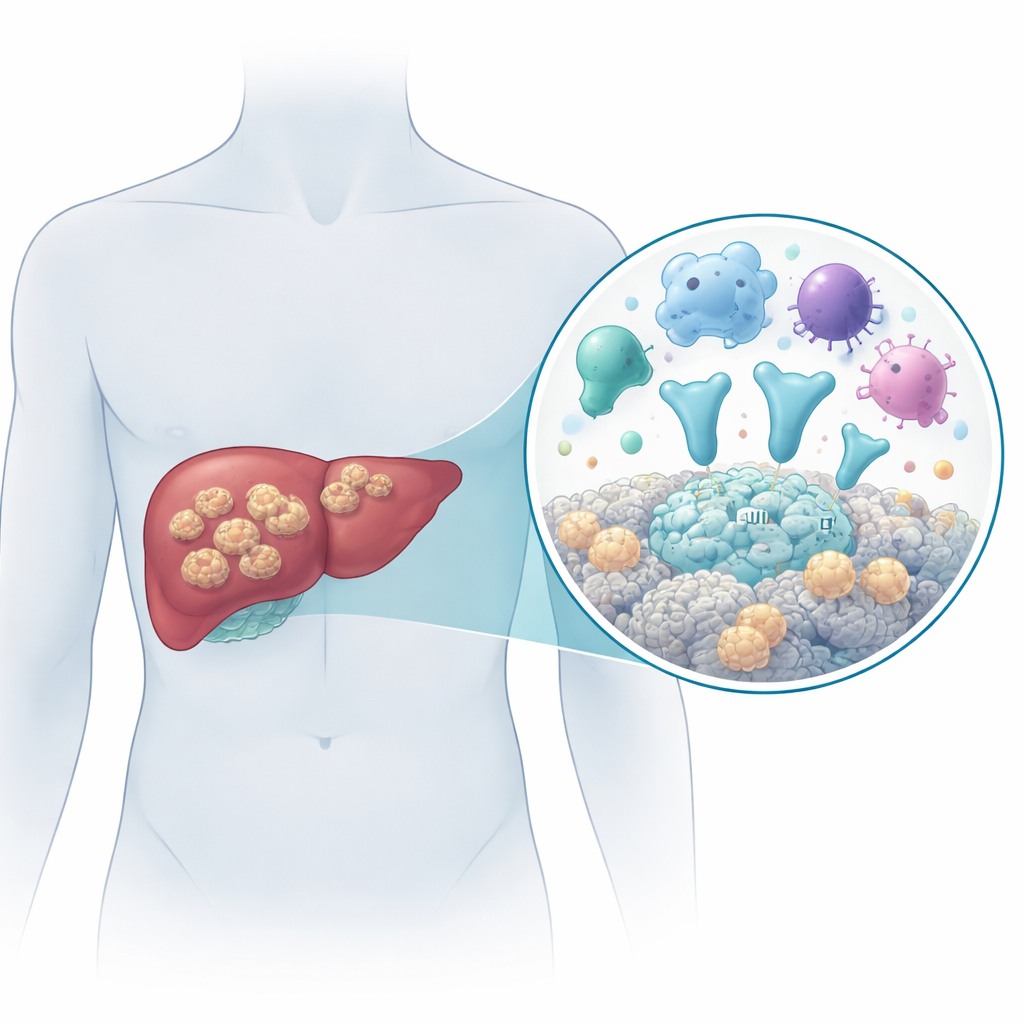
Una tenia peligrosa que crece como un tumor
La enfermedad la causa la fase larvaria de la tenia Echinococcus multilocularis. Las personas se infectan al ingerir accidentalmente huevos del parásito, por ejemplo en alimentos o agua contaminados. Una vez dentro del cuerpo, las larvas se instalan principalmente en el hígado y crecen como numerosos pequeños sacos llenos de líquido que infiltran el tejido circundante, se extienden a órganos cercanos como el bazo y, a veces, alcanzan lugares lejanos como los pulmones o el cerebro. Sin un tratamiento eficaz, más de 9 de cada 10 pacientes mueren en un plazo de 10 a 15 años. La cirugía combinada con fármacos antiparasitarios de larga duración es actualmente la mejor opción, pero el diagnóstico precoz es difícil y los medicamentos no curan la infección de forma fiable. Eso hace crucial comprender cómo interactúa el parásito con el cuerpo humano a nivel molecular.
Una proteína parasitaria que desactiva enzimas cortantes
Muchos animales, incluidos los humanos, producen una familia de proteínas llamadas cistatinas que actúan como seguros frente a poderosas enzimas digestivas conocidas como proteasas de cisteína. Estas enzimas pueden trocear otras proteínas y son importantes en procesos como la degradación de componentes celulares envejecidos y la activación de respuestas inmunitarias. Los parásitos han aprendido a fabricar sus propias proteínas tipo cistatina para interferir con las enzimas y el sistema inmunitario del huésped. En este trabajo, los investigadores identificaron una proteína tipo cistatina de E. multilocularis y la denominaron EmCystatin-B. Encontraron que el gen de EmCystatin-B está mucho más activo en las cabezas larvarias maduras del parásito (protoscolex) que en el tejido quístico circundante, y que la proteína está presente en el citoplasma y el núcleo de las células del parásito, especialmente en células germinativas «tipo stem» en división. Ensayos de laboratorio mostraron que EmCystatin-B puede bloquear con fuerza la actividad de la catepsina B humana, una proteasa de cisteína importante implicada en la inmunidad y la remodelación tisular.
Una forma familiar con un giro inesperado
Para ver exactamente cómo está construida EmCystatin-B, el equipo cristalizó la proteína purificada y utilizó cristalografía de rayos X para resolver su estructura tridimensional a resolución casi atómica. Como otros miembros de la familia de las cistatinas, cada unidad de EmCystatin-B tiene una forma característica: un segmento helicoidal central respaldado por varias hebras planas y en forma de cinta, formando una cuña que normalmente encaja en el sitio activo de una proteasa. Por su secuencia y la ausencia de un péptido señal evidente para la secreción, EmCystatin-B pertenece al subgrupo de las «stefinas», que suelen ser proteínas pequeñas intracelulares que no contienen puentes disulfuro estabilizantes. Sorprendentemente, la estructura reveló que aunque cada unidad de EmCystatin-B presenta el pliegue esperado, la forma en que estas unidades se asocian entre sí es inusual y específica de la especie en comparación con su homóloga humana, la cistatina B.
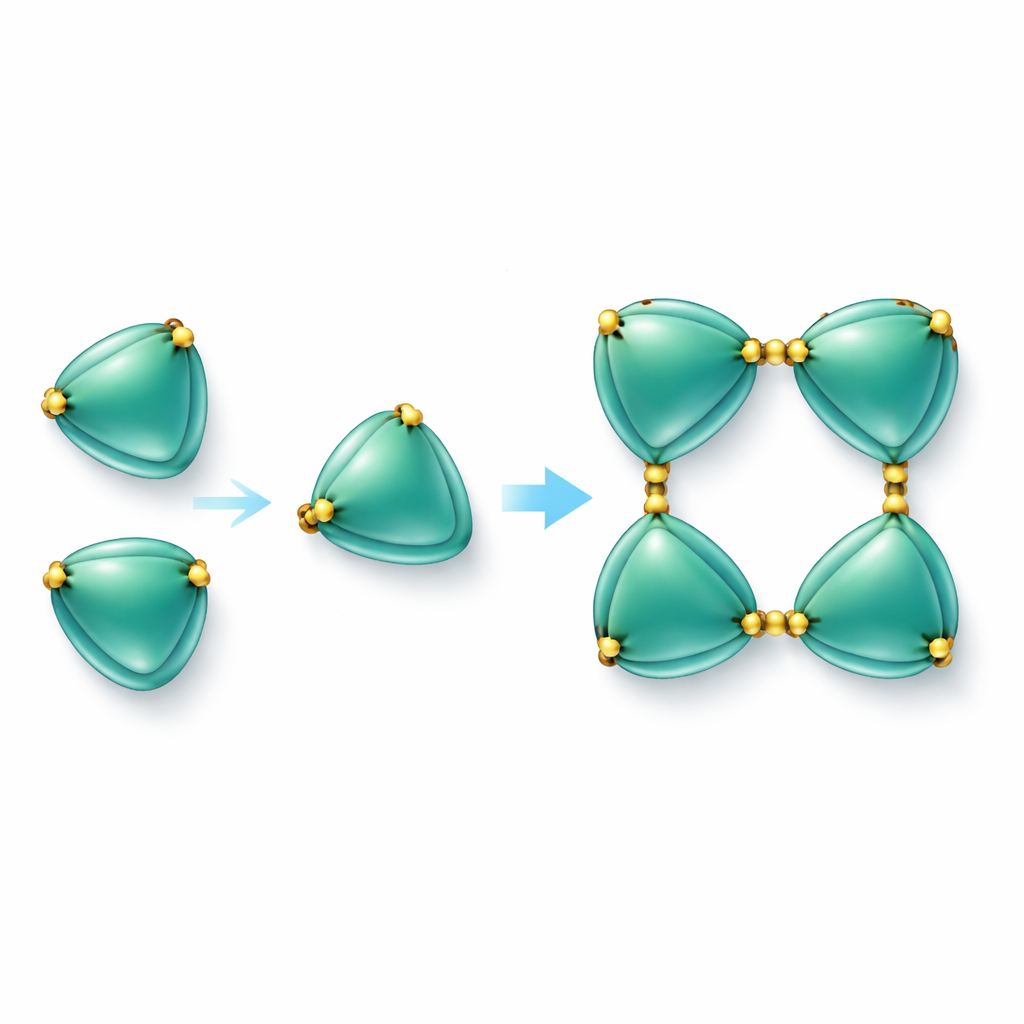
Construir cadenas proteicas con enlaces de azufre
El hallazgo más llamativo fue que las moléculas de EmCystatin-B no flotan simplemente como unidades individuales. En cambio, pueden unirse de forma escalonada para formar dímeros (pares) y luego tetrámeros (grupos de cuatro). Dos mecanismos diferentes ayudan a formar los dímeros iniciales. En uno, una parte de una molécula se desplaza y completa la estructura de su vecina, un fenómeno conocido como intercambio de dominios. En el otro, pares de moléculas se unen mediante puentes disulfuro, enlaces químicos fuertes entre aminoácidos que contienen azufre (cisteínas). En EmCystatin-B, la cisteína en la posición 4 de una molécula se enlaza con la cisteína en la posición 76 de una molécula compañera. Cuatro de estos enlaces cruzados estabilizan el tetrámero. Este uso de múltiples puentes disulfuro intermoleculares es totalmente nuevo para las stefinas clásicas, que típicamente carecen de tales enlaces. Cuando los investigadores cambiaron estas cisteínas clave por otro aminoácido, la proteína ya no pudo ensamblarse de forma eficiente en complejos de orden superior y su capacidad para inhibir la catepsina B cayó drásticamente.
Qué significa esto para combatir la infección
Para un no especialista, el mensaje es que el parásito ha evolucionado una versión especialmente diseñada de una familia proteica común, usando «remaches» químicos adicionales para fijar varias unidades inhibitorias entre sí. Esta forma oligomérica parece importante para desactivar una enzima del huésped que de otro modo ayudaría a controlar la infección. Al desvelar la arquitectura precisa de EmCystatin-B y sus ensamblajes únicos ligados por disulfuro, el estudio amplía nuestra comprensión de cómo las proteínas cistatina pueden ajustarse entre especies. A largo plazo, estos hallazgos podrían guiar el diseño de fármacos que bloqueen el efecto protector de EmCystatin-B sobre el parásito o que imiten sus propiedades calmantes del sistema inmunitario para tratar enfermedades inflamatorias.
Cita: Hong, W., Cheng, Z., Xu, Z. et al. Crystal structure of Echinococcus multilocularis cystatin B reveals a novel feature in classical stefins. Sci Rep 16, 5114 (2026). https://doi.org/10.1038/s41598-026-35060-0
Palabras clave: echinococosis alveolar, Echinococcus multilocularis, cistatina B, estructura proteica, modulación inmunitaria