Clear Sky Science · es
Interrupción del ensamblaje del inflamasoma NLRP3 mediante la remodelación inducida por ligando de las interfaces del dominio pirina
Por qué importa calmar la inflamación descontrolada
Muchas enfermedades crónicas —desde la artritis y la gota hasta las enfermedades cardíacas y la neurodegeneración— se alimentan de un sistema de alarma inmune hiperactivo dentro de nuestras células. Una parte clave de esta alarma, llamada inflamasoma NLRP3, nos ayuda a combatir infecciones pero también puede impulsar una inflamación dañina cuando funciona mal. Este estudio describe una nueva molécula pequeña, denominada E9, que se dirige a un paso temprano en la activación de NLRP3, ofreciendo un enfoque novedoso para diseñar fármacos que reduzcan la inflamación nociva sin apagar por completo el sistema inmune.
Una alarma celular con un lado oscuro
Cuando nuestro organismo detecta peligro, las células inmunitarias ensamblan el inflamasoma NLRP3, un complejo proteico de gran tamaño que actúa como una alarma molecular. Una vez formado, este complejo activa una enzima llamada caspasa-1, que a su vez activa potentes mensajeros inflamatorios, incluidas las citocinas IL-1β e IL-18. Estas señales son vitales para combatir infecciones y eliminar tejido dañado. Pero si el inflamasoma permanece activado demasiado tiempo o se enciende en el momento equivocado, contribuye a enfermedades inflamatorias crónicas que afectan las articulaciones, los vasos sanguíneos, el cerebro y otros órganos. Por ello, investigadores de todo el mundo buscan maneras precisas de controlar NLRP3 sin suprimir la inmunidad de forma generalizada.
Más allá de los objetivos farmacológicos habituales
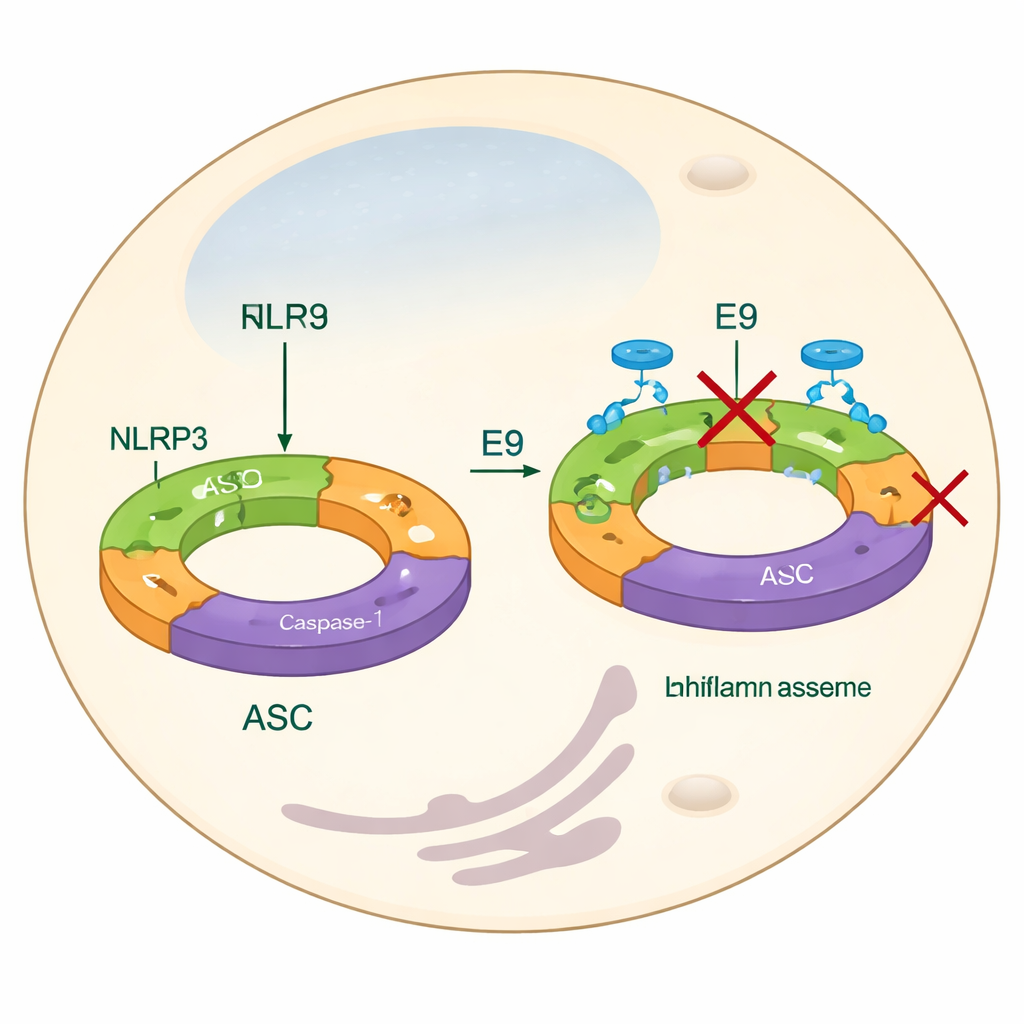
La mayoría de las estrategias actuales para domar a NLRP3 se centran en bloquear sus productos finales —como IL-1β— o en interferir con un dominio central similar a un motor que emplea moléculas energéticas como el ATP. Aunque estos enfoques pueden funcionar, pueden pasar por alto los pasos iniciales del ensamblaje y no abordan por completo cómo las proteínas NLRP3 se unen para formar una máquina funcional. En este trabajo, los autores se fijan en cambio en el dominio pirina, una parte de NLRP3 que ayuda a que las unidades individuales se conecten formando filamentos largos. Estos filamentos reclutan después otra proteína adaptadora, ASC, que se agrupa en brillantes “manchas” dentro de las células —un sello visual de la activación del inflamasoma. Al encontrar compuestos que eviten que los dominios pirina encajen correctamente, el equipo pretende impedir la formación del inflamasoma desde el principio.
Encontrar una molécula que rompa la cadena
Los investigadores cribaron una biblioteca de 1500 moléculas pequeñas recién sintetizadas usando una prueba ingeniosa basada en luz. Fusionaron fragmentos divididos de una luciferasa al dominio pirina de NLRP3; cuando dos dominios pirina se unían, los fragmentos enzimáticos se reensamblaban y producían luz. Los compuestos que bloqueaban el contacto pirina–pirina provocaban una caída de la señal lumínica. De esta criba identificaron cuatro candidatas prometedoras, destacando una —E9— por su fuerte y constante inhibición. Mediciones adicionales mediante una técnica llamada termofóresis a microescala mostraron que E9 se unía de forma firme al dominio pirina a concentraciones muy bajas (submicromolares), confirmando que su efecto no era un azar sino el resultado de una interacción específica.
Ver el efecto dentro de células vivas
Para comprobar si E9 también funcionaba en un sistema vivo, el equipo recurrió a células humanas con características inmunes diseñadas para producir una versión fluorescente de ASC. Cuando estas células se estimulan con componentes bacterianos y un segundo disparador, NLRP3 se activa y las proteínas ASC se agrupan en manchas brillantes que pueden contarse bajo el microscopio. En presencia de E9, el número de estas manchas disminuyó notablemente, de forma comparable o superior a algunos inhibidores conocidos de NLRP3. Esto demostró que interferir en los contactos del dominio pirina es suficiente para reducir el ensamblaje del inflamasoma y los pasos tempranos de la muerte celular inflamatoria, al menos en condiciones de laboratorio.
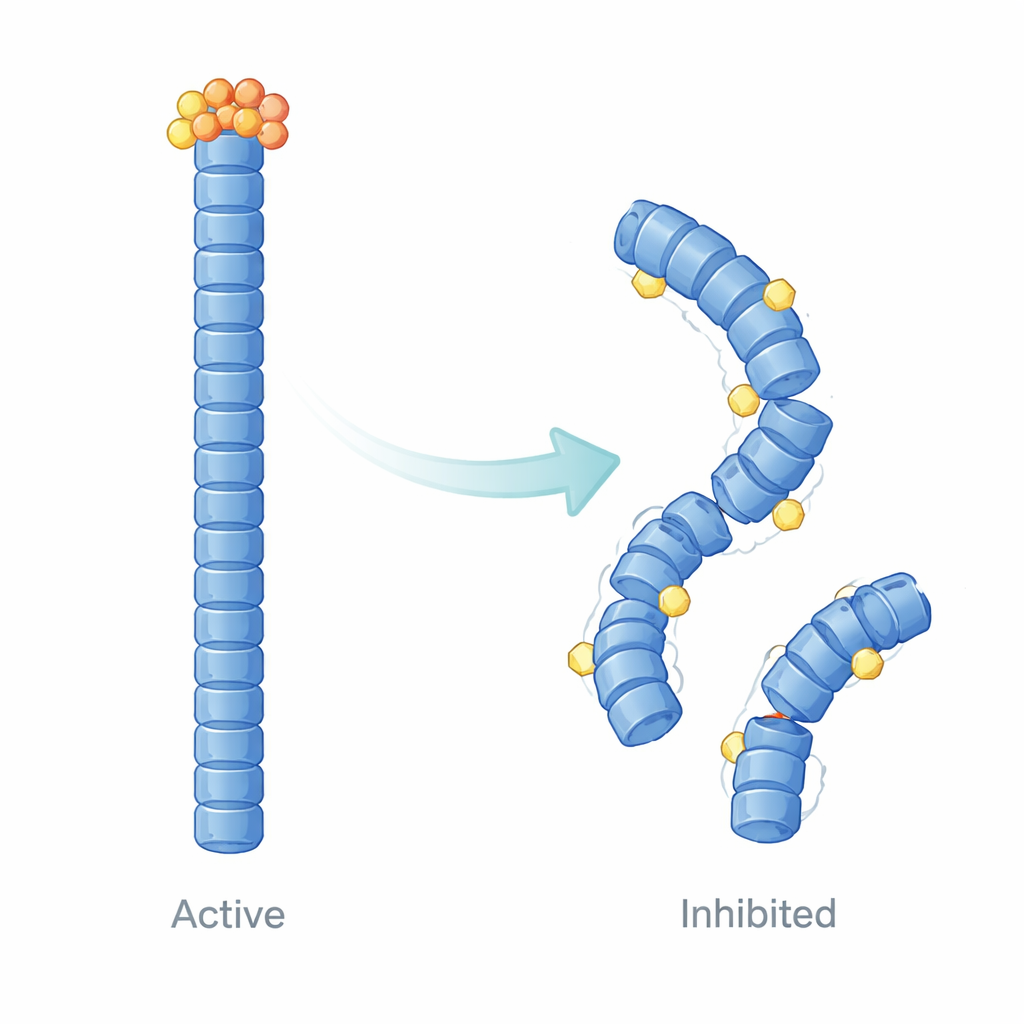
Cómo E9 remodela el andamiaje del inflamasoma
Más allá de medir simplemente la unión, los autores emplearon modelado estructural computacional y simulaciones de dinámica molecular para visualizar cómo E9 cambia el comportamiento de los filamentos de NLRP3 a lo largo del tiempo. Sus cálculos sugieren que E9 se aloja en superficies de contacto específicas donde tocan los dominios pirina, aflojando y remodelando sutilmente el filamento. En lugar de una estructura cooperativa uniforme y estable, el filamento se vuelve desigual: las regiones cercanas a E9 se vuelven más flexibles y pierden su alineación precisa, mientras que otras partes quedan dinámicamente aisladas. Estos cambios amortiguan los movimientos a gran escala y la comunicación estrecha necesarios para el reclutamiento eficiente de ASC, proporcionando una explicación física a la reducción de manchas observada en las células.
Qué podría significar para futuras terapias
En conjunto, los hallazgos sitúan a E9 como un prototipo de una nueva clase de fármacos dirigidos al inflamasoma que actúan interrumpiendo las interfaces entre los elementos constitutivos de NLRP3 en lugar de bloquear su uso de energía o sus productos finales. Aunque el trabajo actual se limita a ensayos in vitro, simulaciones computacionales y cultivos celulares —y se requieren estudios adicionales en animales y humanos— demuestra que moléculas pequeñas diseñadas con cuidado pueden remodelar el propio andamiaje del inflamasoma. Para pacientes con enfermedades impulsadas por una inflamación descontrolada, fármacos enfocados en las interfaces podrían algún día ofrecer un control más preciso, reduciendo la activación inmunitaria nociva mientras mantienen en gran medida las defensas esenciales.
Cita: Khosravifard, S., Hosseinkhani, S., Bakhtiary, N. et al. Disruption of NLRP3 inflammasome assembly via ligand-induced remodeling of pyrin domain interfaces. Sci Rep 16, 4951 (2026). https://doi.org/10.1038/s41598-026-35050-2
Palabras clave: inflamasoma NLRP3, dominio pirina, inhibidor de pequeñas moléculas, inmunidad innata, piropotosis