Clear Sky Science · es
Perfil molecular del carcinoma de células claras de riñón primario frente a metástasis asincrónicas emparejadas revela heterogeneidad en el microambiente inmunitario tumoral
Por qué importa este estudio sobre cáncer de riñón
El cáncer de riñón con frecuencia se disemina a otras partes del cuerpo, y las inmunoterapias modernas no funcionan por igual en todos los pacientes ni en todos los tumores. Este estudio examina en profundidad el carcinoma de células claras renal —el tipo más común de cáncer de riñón— para ver cómo se comporta de forma diferente el sistema inmunitario en el tumor primario del riñón frente a sus metástasis posteriores. Comprender estas diferencias podría ayudar a explicar por qué algunos tumores responden mejor al tratamiento que otros y orientar una atención más precisa y personalizada.
Un vistazo a tumores primarios y metastásicos
Los investigadores se centraron en 19 pacientes a los que se les extirpó el tumor renal (el tumor primario) y que más tarde desarrollaron metástasis en lugares como pulmón, hueso, hígado, glándula suprarrenal, ganglios linfáticos o tejido blando. De estos pacientes recogieron 42 muestras tumorales: 19 primarios y 23 metástasis no tratadas. Extrajeron ARN —una molécula que refleja qué genes están activados— de cortes finos de tejido preservado y utilizaron secuenciación de alto rendimiento para capturar la actividad génica en miles de genes por muestra. 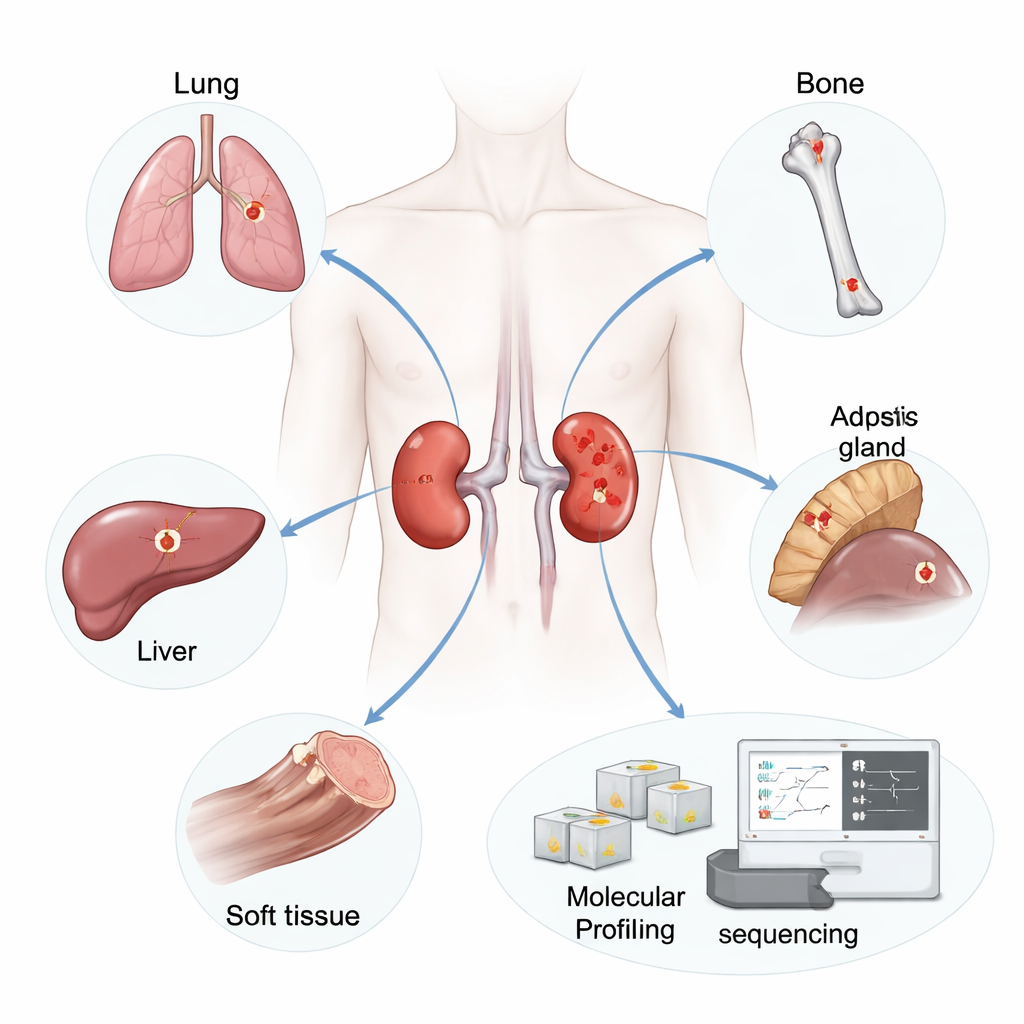
Los tumores primarios y metastásicos son molecularmente distintos
Al analizar los patrones de actividad génica, hallaron que los tumores renales primarios tendían a agruparse entre sí y eran más similares entre sí que a sus propias metástasis. En otras palabras, la metástasis de un paciente podía diferir más de su tumor original que de la metástasis de otra persona. Miles de genes mostraron mayor o menor actividad en metástasis comparadas con los primarios. Los tumores metastásicos presentaron señales más fuertes de programas génicos vinculados a la división celular rápida y al comportamiento agresivo, incluidos caminos implicados en puntos de control del ciclo celular y la producción de proteínas. En contraste, los primarios estaban más enriquecidos en rutas de estrés y señalización, como la hipoxia (bajo oxígeno) y la señalización inflamatoria, lo que sugiere presiones biológicas distintas en el riñón frente a órganos distantes.
El paisaje inmune cambia a medida que el cáncer se disemina
Más allá de la actividad génica bruta, los científicos estimaron qué tipos de células inmunitarias estaban presentes en cada tumor utilizando un método computacional que deconvoluciona datos de ARN en bloque. Descubrieron una diferencia llamativa: los tumores renales primarios contenían una fracción significativamente mayor de células T reguladoras (Tregs), un tipo de célula inmunitaria que atenúa las respuestas inmunitarias y puede proteger a los tumores del ataque. Los primarios también mostraron más células dendríticas en reposo, monocitos, células asesinas naturales y células T CD8+. En contraste, las metástasis eran más ricas en lo que se conoce como macrófagos M2 —células inmunitarias a menudo asociadas con la reparación de heridas y un entorno que apoya al tumor en lugar de matarlo— junto con más células plasmáticas y células dendríticas activadas. 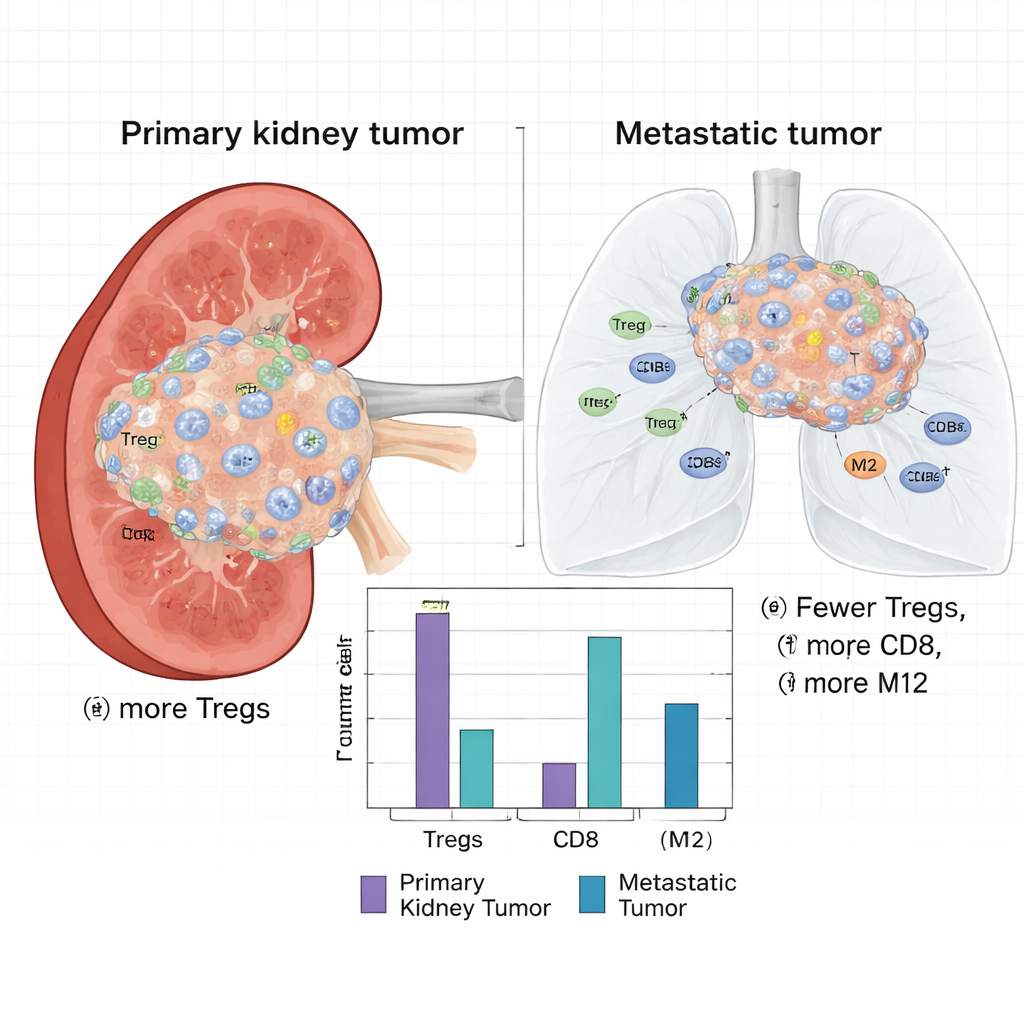
Las metástasis pulmonares y óseas cuentan historias inmunitarias distintas
Al centrar el análisis en sitios metastásicos específicos surgieron matices importantes. Las metástasis pulmonares mostraron mayor actividad de conjuntos génicos ligados al control de la división celular (el punto de control G2M) y factores de transcripción E2F, así como alta expresión de hornerina, una proteína vinculada al crecimiento de vasos sanguíneos en tumores. Sus tumores primarios renales emparejados estaban más enriquecidos en programas génicos relacionados con la hipoxia y, de nuevo, tenían más Tregs. Las metástasis óseas, por el contrario, destacaron por una activación más intensa de la transición epitelio–mesénquima, un proceso que ayuda a las células cancerosas a volverse más móviles e invasivas. Estas lesiones óseas también contenían niveles más altos de macrófagos M2, mientras que los primarios que las generaron mostraron mayor expresión de HHLA2, una molécula de punto de control inmunitario reconocida recientemente. En conjunto, estos hallazgos subrayan que los entornos inmunitarios y moleculares de las metástasis no solo difieren de los de los primarios, sino que además varían entre distintos sitios metastásicos.
Equilibrio de células inmunitarias y resultados en pacientes
Para entender qué significan estos patrones inmunitarios para los pacientes, el equipo recurrió a tres grandes conjuntos de datos públicos de carcinoma renal de células claras. Usaron el mismo enfoque computacional para estimar los niveles de Tregs y de células T CD8+ y luego los asociaron con los resultados de supervivencia. En las distintas cohortes, las personas cuyos tumores presentaban una combinación de bajos niveles de células T CD8+ (las principales T que matan el cáncer) y altos niveles de Tregs tendieron a tener peores resultados en términos de supervivencia libre de progresión o supervivencia específica de la enfermedad, incluso tras ajustar por edad, grado del tumor y estadio. Aunque el estadio general siguió influyendo fuertemente en la supervivencia, el equilibrio entre las Tregs supresoras y las células CD8+ agresoras emergió como un marcador adicional de riesgo.
Lo que esto implica para la futura atención del cáncer de riñón
En términos accesibles, este estudio muestra que el tumor renal original y sus metástasis habitan “vecindarios” inmunitarios diferentes. El tumor primario parece especialmente competente en reclutar células pacificadoras que silencian el sistema inmunitario, lo que podría explicar en parte por qué los tumores renales in situ a menudo responden menos bien a la inmunoterapia que los depósitos metastásicos. Mientras tanto, las metástasis desarrollan sus propios sistemas de apoyo local que varían según el órgano. Estas ideas sugieren que los médicos podrían necesitar, en ocasiones, muestrear tanto el tumor renal como las metástasis para comprender por completo la enfermedad de un paciente, y que tratamientos que combinen inhibidores de puntos de control inmunitario con estrategias dirigidas a las Tregs o a los macrófagos M2 podrían mejorar los resultados en personas con carcinoma renal de células claras metastásico.
Cita: Cotta, B., Nallandhighal, S., Monda, S. et al. Molecular profiling of primary versus paired asynchronous metastatic clear cell renal cell carcinoma reveals heterogeneity in tumor immune microenvironment. Sci Rep 16, 5473 (2026). https://doi.org/10.1038/s41598-026-35021-7
Palabras clave: cáncer de riñón, microambiente tumoral, inmunoterapia, metástasis, células T reguladoras