Clear Sky Science · es
Base estructural de la diosgenina como agonista inverso del receptor huérfano relacionado con el ácido retinoico γ
Por qué importa un compuesto vegetal y un interruptor inmunitario
Muchas condiciones crónicas —desde enfermedades autoinmunes como la esclerosis múltiple y la psoriasis hasta la obesidad y la diabetes tipo 2— están impulsadas por señales inmunitarias sobreactivas y por fallos en las señales metabólicas. Los científicos llevan tiempo buscando fármacos más seguros que puedan ajustar estas señales con precisión. Este estudio explora cómo la diosgenina, una molécula natural presente en ciertas plantas medicinales y en ñames, se une a una proteína reguladora del sistema inmunitario llamada RORγ y la convierte en un estado menos activo. Entender esta interacción a nivel atómico podría abrir la puerta a terapias más suaves y específicas, derivadas de un armazón vegetal ya conocido.
Un mando maestro para la inmunidad y el metabolismo
RORγ forma parte de una gran familia de «receptores nucleares»: proteínas dentro de las células que encienden o apagan genes en respuesta a pequeñas moléculas. Esta proteína en particular es un controlador clave de un grupo de células inmunitarias conocidas como células Th17, que producen la señal inflamatoria IL-17A y se han relacionado con enfermedades autoinmunes como la esclerosis múltiple, la psoriasis, la artritis reumatoide y la enfermedad de Crohn. RORγ también influye en cómo se desarrollan las células adiposas y en la respuesta del organismo a la insulina, lo que lo vincula con la obesidad y la diabetes. Debido a este amplio alcance, RORγ se ha convertido en un objetivo atractivo para fármacos, pero muchas moléculas sintéticas que se unen a él han presentado problemas de seguridad, selectividad o eficacia en humanos.
Un remedio tradicional ofrece un candidato prometedor
La diosgenina es una molécula tipo esteroide extraída de plantas como especies de Dioscorea (ñame silvestre) y varias hierbas medicinales tradicionales. Se ha estudiado por sus posibles beneficios antiinflamatorios, anticancerígenos, antidiabéticos y cardiovasculares en modelos celulares y animales. Trabajos previos sugirieron que la diosgenina podría influir en la vía RORα/γ y suprimir respuestas Th17 dañinas, pero no estaba claro si actuaba directamente sobre RORγ ni cómo modulaba el comportamiento de la proteína. Para responder a esto, los autores cribaron una biblioteca de compuestos naturales con un ensayo sensible de unión y identificaron la diosgenina como un ligando potente de la región de unión al ligando de RORγ.
Cómo la diosgenina empuja a RORγ en sentido inverso
Los investigadores examinaron cómo la diosgenina afecta la capacidad de RORγ para reclutar proteínas auxiliares que o bien aumentan (coactivadores) o bien reprimen (correpresores) la actividad génica. Sorprendentemente, la diosgenina fomentó que RORγ se uniera a ambos tipos de socios, un patrón distinto al de un antagonista natural conocido, el ácido ursólico. En ensayos celulares con reporteros que miden el encendido y apagado génico, la diosgenina redujo de forma constante la actividad dirigida por RORγ de manera dependiente de la dosis, con potencias en el rango submicromolar. Este comportamiento encaja con el perfil de un «agonista inverso»: un compuesto que no solo bloquea la actividad basal, sino que impulsa activamente el receptor hacia un estado apagado, incluso cuando por sí solo estaría activo.
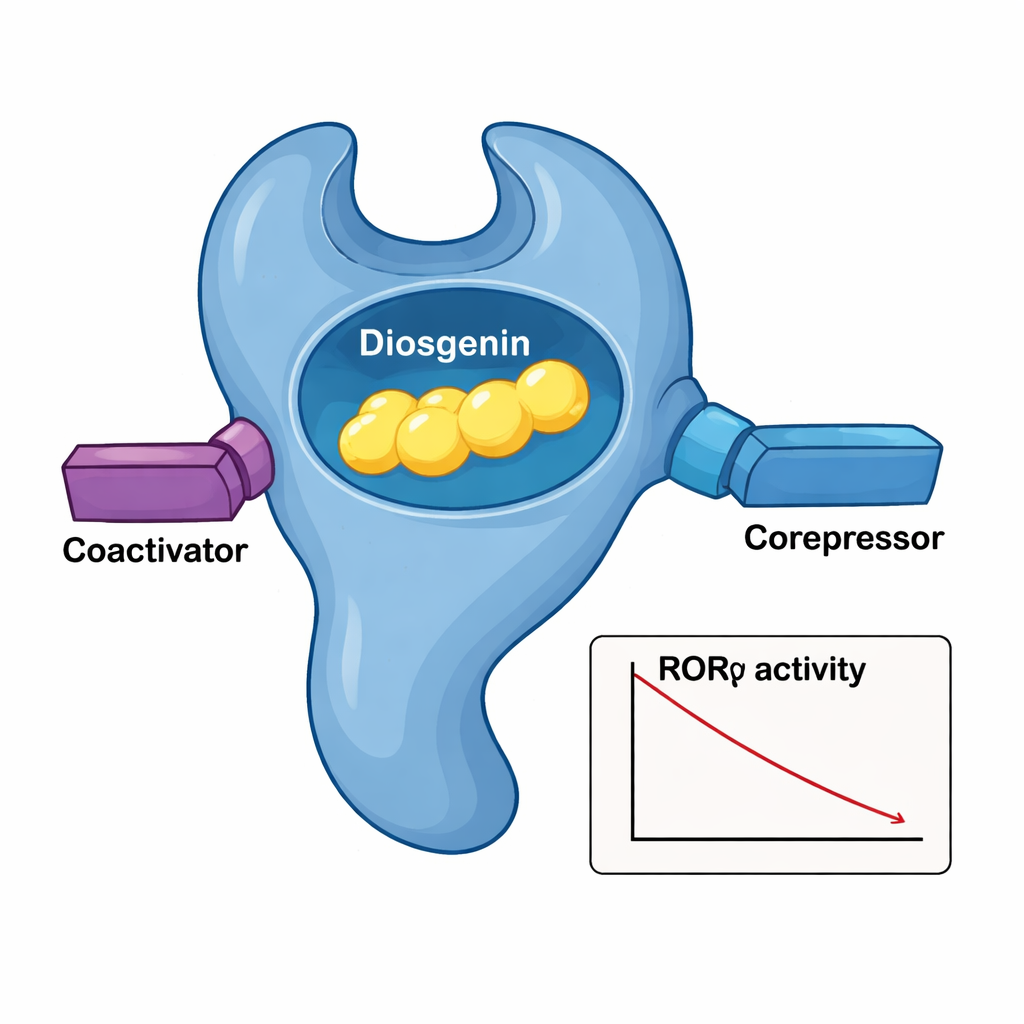
Un primer plano del apretón molecular
Para ver exactamente cómo encaja la diosgenina en RORγ, el equipo resolvió la estructura cristalina tridimensional del dominio de unión al ligando de la proteína con la diosgenina alojada en su interior. El receptor se pliega en un haz de hélices en capas, formando un bolsillo que acuna el cuerpo similar a un esteroide de la diosgenina. Una red de interacciones hidrofóbicas ajustadas de varios aminoácidos actúa como un guante a medida alrededor de la columna vertebral de la molécula, mientras que un grupo hidroxilo crítico en la diosgenina forma enlaces de hidrógeno mediadas por agua con dos residuos de arginina. Cuando se alteraron esos residuos del bolsillo de uno en uno, la capacidad de la diosgenina para silenciar RORγ disminuyó, confirmando su importancia. Comparaciones estructurales con el complejo RORγ–ácido ursólico mostraron que la diosgenina mantiene una hélice terminal clave (AF‑2) en una posición «similar a la activa» aun cuando reduce la transcripción global, lo que explica por qué puede atraer simultáneamente tanto coactivadores como correpresores.
De la estructura cristalina a futuros medicamentos
La imagen detallada de la interacción diosgenina–RORγ pone de manifiesto dos ventajas notables para el diseño de fármacos. Primero, el bolsillo del receptor muestra suficiente flexibilidad para reconocer distintas formas de ligando, lo que permite a los químicos ajustar el armazón de la diosgenina para mejorar la selectividad por RORγ y reducir enlaces no deseados a otros receptores nucleares. Segundo, el origen natural de la diosgenina y su conocida baja toxicidad inherente en modelos preclínicos la convierten en un punto de partida atractivo frente a algunos compuestos totalmente sintéticos que se han estancado en ensayos. En términos sencillos, este trabajo revela cómo una molécula derivada de plantas puede unirse a un interruptor central inmunometabólico y volverlo en sentido inverso, ofreciendo una plantilla estructural para desarrollar tratamientos más seguros y eficaces para enfermedades relacionadas con RORγ.
Cita: Chen, S., Tian, S., Liang, J. et al. Structural basis for diosgenin as an inverse agonist of retinoic acid receptor-related orphan receptor γ. Sci Rep 16, 4765 (2026). https://doi.org/10.1038/s41598-026-35006-6
Palabras clave: ROR gamma, diosgenina, enfermedad autoinmune, receptor nuclear, agonista inverso