Clear Sky Science · es
Caracterización transcriptómica del espliceo alternativo aberrante en los músculos esqueléticos de pacientes con sarcopenia
Por qué los músculos envejecidos pierden fuerza
La sarcopenia—la pérdida gradual de masa y fuerza muscular con la edad—es una de las principales razones por las que las personas mayores tienen dificultades para tareas cotidianas, desde subir escaleras hasta llevar la compra. Este estudio se adentra en el músculo envejecido a nivel del ARN, los mensajes que indican a las células qué proteínas producir. Los autores muestran que en la sarcopenia muchos de estos mensajes de ARN se cortan y cosen de maneras anormales, lo que podría alterar la producción de energía en el músculo y señalar nuevos objetivos para tratamiento.
Pérdida muscular y el sistema de “edición” genética del cuerpo
Nuestros genes están escritos en ADN, pero las células trabajan a partir de copias de ARN de esos genes. Antes de que un mensaje de ARN se use, las células normalmente lo recortan y empalman—como si editaran una película—de modo que un gen puede producir varias versiones de una proteína. Este proceso, llamado splicing alternativo, es especialmente activo en el músculo, que necesita proteínas finamente ajustadas para contraerse, repararse y adaptarse al ejercicio. Cuando el splicing falla, pueden producirse versiones proteicas incorrectas o perderse otras importantes, lo que contribuye a enfermedades como las distrofias musculares y algunos trastornos cerebrales. Los autores sospecharon que una capa oculta similar de mal edición del ARN podría estar impulsando la sarcopenia.
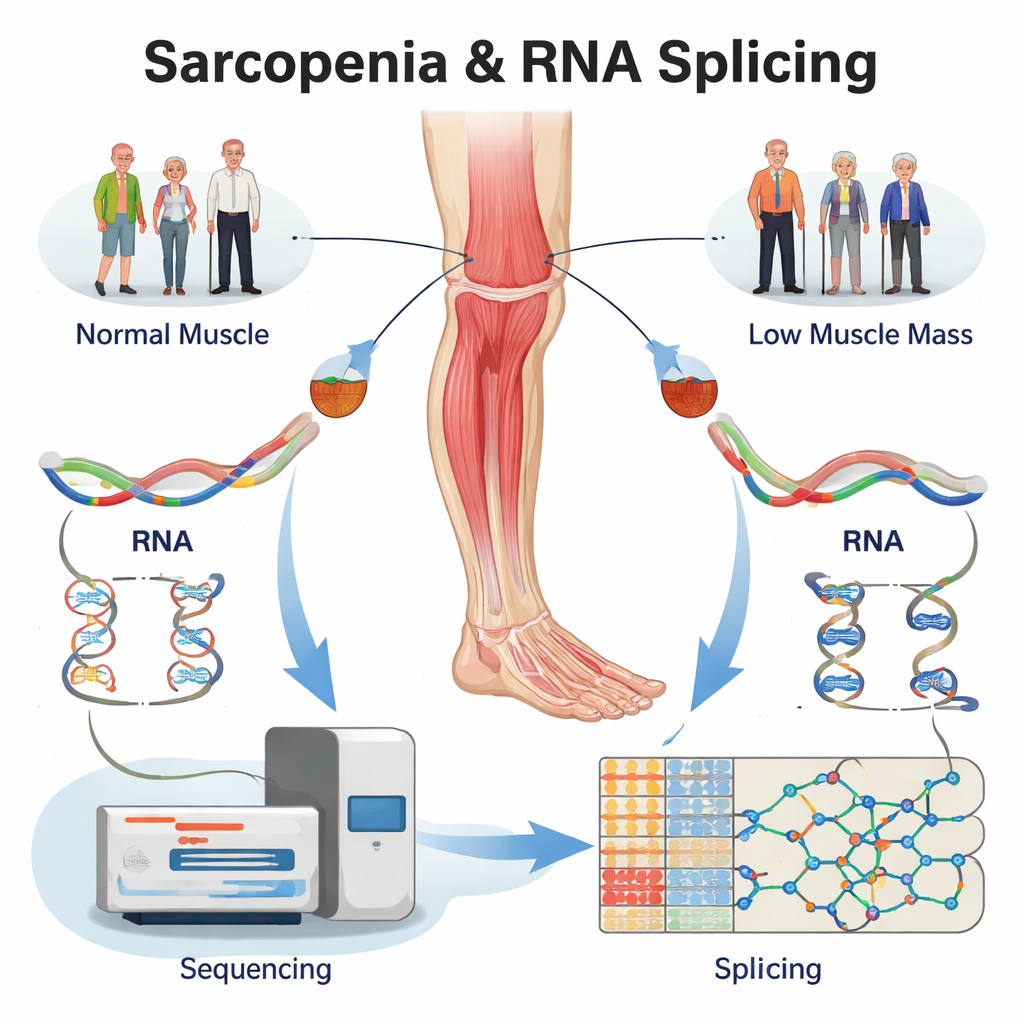
Releer datos existentes para encontrar errores ocultos en el ARN
En lugar de reclutar nuevos voluntarios, el equipo reanalizó un gran conjunto de datos de secuenciación de ARN ya existente a partir de biopsias del muslo humano. Las muestras procedían de cuatro grupos: adultos mayores con sarcopenia manifiesta, personas con solo baja masa muscular, personas con solo baja fuerza muscular y controles sanos emparejados por edad. Usando software especializado, primero confirmaron que cientos de genes estaban regulados al alza o a la baja en los músculos enfermos. Más importante aún, luego analizaron cómo se empalmaba el ARN de cada gen, catalogando más de 5.000 cambios de splicing en los tres grupos problemáticos en comparación con el músculo sano. Estos cambios se concentraron en unos pocos tipos básicos—como el salto de un exón o la elección de un sitio de corte alternativo—patrones que se sabe que alteran fuertemente la estructura de las proteínas.
Fábricas de energía y vías sensores de combustible celular alteradas
Los cambios de splicing aparecieron en genes que están en el corazón de la biología muscular. Muchos genes afectados codifican partes de las mitocondrias, las pequeñas fábricas de energía que impulsan la contracción muscular. En el músculo sarcopénico, 16 genes implicados en la fosforilación oxidativa—el proceso que convierte los nutrientes en energía utilizable—presentaron splicing alterado, especialmente componentes de los complejos mitocondriales que manejan el transporte de electrones y el bombeo de protones. Otros cambios aparecieron en genes que fabrican o usan NAD⁺, una molécula clave para la energía y la reparación celular. En lugar de mostrarse simplemente más o menos abundantes, enzimas importantes como CD38, PARP2 y varias sirtuinas produjeron variantes de ARN diferentes, lo que sugiere que el equilibrio entre la producción y el consumo de NAD⁺ está distorsionado a nivel del splicing. Los genes afectados también se agruparon en vías de señalización muscular bien conocidas, incluidas las rutas AMPK y FoxO, que actúan como medidores de combustible y respondedores al estrés celular.
Patrones compartidos en distintas etapas—y entre especies
De manera notable, muchos de los mismos genes mostraron cambios de splicing no solo en personas con sarcopenia completa, sino también en aquellas que solo tenían baja masa muscular o solo baja fuerza. Esto sugiere que el splicing anómalo comienza temprano y atraviesa las diferentes manifestaciones clínicas de la enfermedad. Para probar si estos cambios podían reproducirse en un modelo animal, los investigadores indujeron atrofia muscular en ratones con dexametasona, un esteroide usado habitualmente para imitar algunas características de la sarcopenia. Los ratones desarrollaron una fuerza de agarre más débil y peor rendimiento en pruebas de carrera y equilibrio. Cuando el equipo secuenció el ARN muscular de los ratones, nuevamente encontraron cientos de genes con splicing alterado. Alrededor de una quinta parte de estos coincidieron con los genes humanos asociados a la sarcopenia, y muchos estaban implicados en el control de la transcripción, la estructura de la cromatina y el propio splicing—interruptores de mayor nivel que pueden remodelar la producción proteica global de una célula.
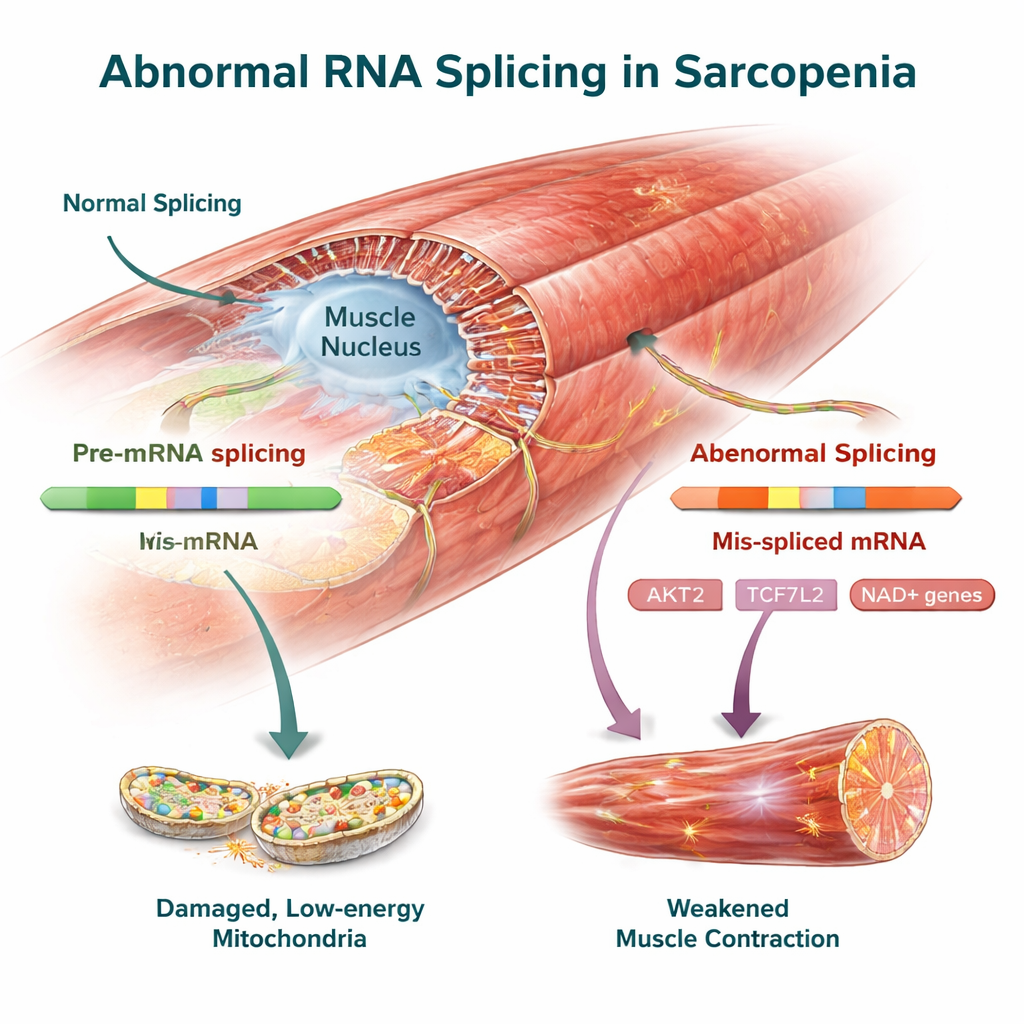
Genes clave del control muscular como posibles dianas terapéuticas
Entre los cambios conservados entre especies hubo varios genes ya vinculados con la salud muscular. AKT2, un regulador central del crecimiento y la síntesis proteica en el músculo, mostró desplazamientos de splicing distintivos tanto en humanos como en ratones que podrían reducir su capacidad para mantener la masa muscular. TCF7L2, parte de la vía de señalización Wnt, junto con FMNL2 y USP40, que ayudan a organizar el andamiaje interno del músculo y el control de calidad proteica, también presentaron variantes de ARN alteradas. El equipo confirmó experimentalmente estos cambios de splicing en músculo de ratón, reforzando la idea de que son características reales de la enfermedad y no artefactos del análisis de datos.
Qué significa esto para prevenir la fragilidad
Para el público general, la conclusión es que la sarcopenia no se reduce solo a que los músculos “se desgasten” o a que los genes se enciendan o apaguen. También implica una mal edición generalizada de los mensajes de ARN que guían cómo las células musculares fabrican y mantienen su maquinaria, especialmente los sistemas que generan energía y detectan el estrés. Dado que, en principio, el splicing puede corregirse con fármacos basados en ARN diseñados con precisión, los errores de splicing conservados que se han descubierto aquí—particularmente en genes como AKT2 y TCF7L2—ofrecen una nueva serie de pistas para terapias que ayuden a que los músculos envejecidos se mantengan más fuertes durante más tiempo.
Cita: Li, Y., Guo, X., Li, S. et al. Transcriptomic characterization of the aberrant alternative splicing in skeletal muscles of sarcopenia patients. Sci Rep 16, 5334 (2026). https://doi.org/10.1038/s41598-026-35002-w
Palabras clave: sarcopenia, envejecimiento muscular, splicing de ARN, mitocondrias, AKT2