Clear Sky Science · es
Modelo fenomenológico de la estabilización de la transtiretina
Por qué esto importa para pacientes y familias
La amiloidosis por transtiretina es una enfermedad grave en la que una proteína normal de la sangre, la transtiretina (TTR), se descompone y sus fragmentos pueden agruparse en depósitos dañinos en el corazón y los nervios. Nuevos fármacos como tafamidis y acoramidis están diseñados para mantener esta proteína en su forma segura de cuatro partes y ya han mejorado los resultados para muchas personas. Sin embargo, los médicos observan un efecto desconcertante en pacientes tratados: los niveles sanguíneos de TTR aumentan más del 30%, y no está claro por qué. Este artículo utiliza un modelo simplificado basado en matemáticas para explorar lo que podría estar ocurriendo dentro del organismo y lo que ello implica sobre el verdadero modo de acción de estos medicamentos. 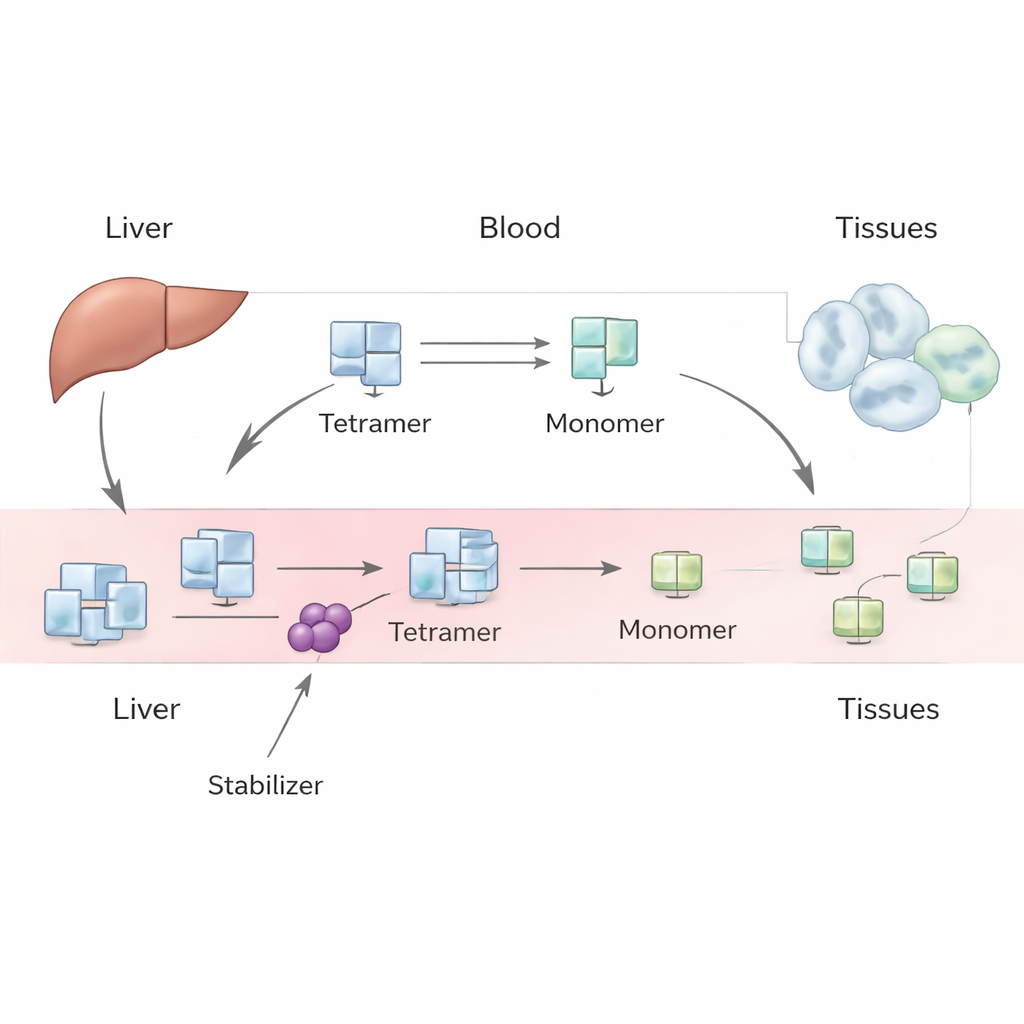
Una proteína que puede ayudar o dañar
La TTR se produce principalmente en el hígado y normalmente circula en sangre como un conjunto estable de cuatro subunidades idénticas, llamado tetrámero. Transporta hormonas tiroideas y vitamina A. En ciertas condiciones, como el envejecimiento o variantes genéticas heredadas, este tetrámero puede disociarse en subunidades individuales, o monómeros. Estos monómeros pueden plegarse mal y agregarse en fibrillas amiloides, que dañan tejidos y provocan amiloidosis por transtiretina en el corazón (miocardiopatía) o en los nervios (neuropatía). Fármacos como tafamidis y acoramidis están diseñados para unirse al tetrámero y dificultar su descomposición, ralentizando la progresión de la enfermedad. Sin embargo, cuando los pacientes comienzan estos tratamientos, los niveles medidos de TTR en sangre aumentan de manera consistente, y este incremento es mayor de lo que indicarían simples experimentos de laboratorio.
Construyendo una imagen simple de un sistema complejo
Los autores abordan este rompecabezas con un modelo fenomenológico—uno que se centra en el comportamiento observable global en lugar de cada detalle microscópico. En su marco, el hígado produce tetrámeros de TTR a una tasa constante, que luego pasan al torrente sanguíneo. Una vez en circulación, los tetrámeros pueden disociarse en monómeros y volver a reunirse, y tanto tetrámeros como monómeros pueden eliminarse de la sangre por captación en tejidos y degradación. Al plantear un par de ecuaciones de balance de masa para tetrámeros y monómeros, el equipo explora distintos escenarios: uno en el que los monómeros mayoritariamente vuelven a formar tetrámeros, otro en el que se eliminan rápidamente, y un caso intermedio donde ambos procesos importan. Utilizan estudios históricos con trazadores en humanos y datos de laboratorio modernos para estimar cantidades clave, como la velocidad de eliminación de tetrámeros, la rapidez con que se rompen y cuánto ralentizan los fármacos esa descomposición.
Por qué solo estabilizar el tetrámero no es suficiente
Con estas estimaciones, los investigadores plantean una pregunta directa: si un fármaco pudiera impedir perfectamente que los tetrámeros se descompongan, ¿cuánto aumentaría el nivel de TTR en sangre? En todos los regímenes plausibles, la respuesta es modesta—del orden del 15% como máximo para valores de parámetros típicos, y con frecuencia menor, dependiendo de cómo se manejen los monómeros. Esto queda muy por debajo del aumento >30% observado en pacientes tratados. La discrepancia persiste incluso si se admite una amplia incertidumbre en los parámetros conocidos. El modelo sugiere por tanto que simplemente ralentizar la ruptura del tetrámero no puede, por sí solo, explicar el efecto clínico completo. Deben estar cambiando también otros procesos que controlan la velocidad de síntesis de TTR, su captación por las células o su degradación cuando están presentes los fármacos estabilizadores. 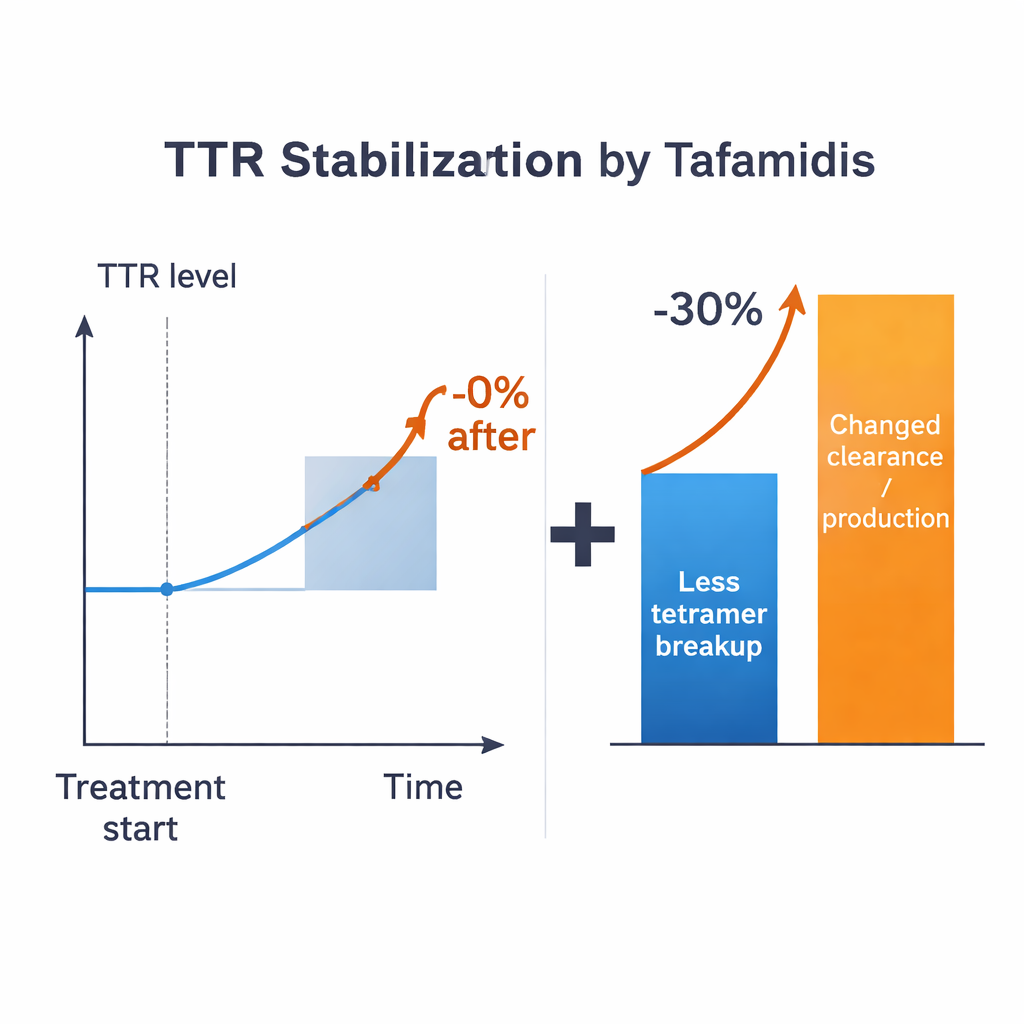
Pistas a partir de los niveles de fármaco y experimentos ingeniosos
Para conectar la exposición al fármaco con el comportamiento de la TTR, los autores combinan un modelo farmacocinético básico de tafamidis (cómo se mueve el fármaco por el cuerpo a lo largo del tiempo) con ensayos especializados de “intercambio de subunidades”. En estos experimentos, tetrámeros de TTR marcados y no marcados se mezclan en plasma humano, y el intercambio gradual de subunidades revela con qué frecuencia se descomponen los tetrámeros. Medir este proceso a distintas concentraciones de fármaco proporciona un vínculo directo y basado en datos entre el nivel de tafamidis y la estabilidad efectiva del tetrámero, sin necesidad de conocer cuánto fármaco está unido a la albúmina o a la hormona tiroidea. Este enlace fenomenológico alimenta el modelo y elude con claridad muchas incógnitas bioquímicas. Aun así, incluso con esta ventaja, los cálculos siguen limitando el aumento esperado de la TTR a aproximadamente la mitad del incremento observado clínicamente, lo que refuerza la idea de que cambios en la eliminación, internalización, degradación o incluso síntesis deben formar parte de la explicación.
Qué significa esto en el futuro
Para no especialistas, el mensaje clave es que es probable que estos fármacos estabilizadores hagan algo más que “pegar” los tetrámeros de TTR. Probablemente también afectan cómo el cuerpo produce, elimina o recicla la proteína. Los autores sostienen que modelos sencillos y transparentes como el suyo son potentes porque dejan al descubierto esas lagunas en nuestro conocimiento y señalan experimentos concretos—por ejemplo, medir directamente la rapidez con que se eliminan los monómeros, con qué velocidad las distintas formas de TTR son captadas por las células, o si la TTR unida al fármaco se maneja de forma distinta que la proteína no unida. Mejores respuestas a estas preguntas no solo refinarían el tratamiento de la amiloidosis por transtiretina, sino que también podrían revelar reglas generales sobre otras enfermedades en las que proteínas normales se convierten en agregados dañinos.
Cita: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
Palabras clave: amiloidosis por transtiretina, estabilización de proteínas, tafamidis, modelado farmacocinético, enfermedades por amiloide