Clear Sky Science · es
La estabilización dirigida del factor inducible por hipoxia 1-alfa (HIF1A) durante la maduración in vitro de complejos cúmulo-oocito bovinos aumenta las tasas de blastocisto
Por qué importa ajustar la detección de oxígeno en los óvulos
La cría moderna de ganado depende en gran medida de embriones fabricados en laboratorio, pero el éxito está lejos de ser seguro: solo alrededor de un tercio de los ovocitos alcanzan la crucial etapa de blastocisto, cuando están listos para ser transferidos a una vaca. Este estudio plantea una pregunta aparentemente simple con amplia relevancia para la reproducción asistida y la mejora animal: si imitamos más de cerca las condiciones de bajo oxígeno que los óvulos experimentan de forma natural dentro del ovario—al potenciar de forma moderada una proteína clave que detecta el oxígeno—, ¿podemos lograr que más embriones se desarrollen con éxito?
La vida comienza en un nicho de baja oxigenación
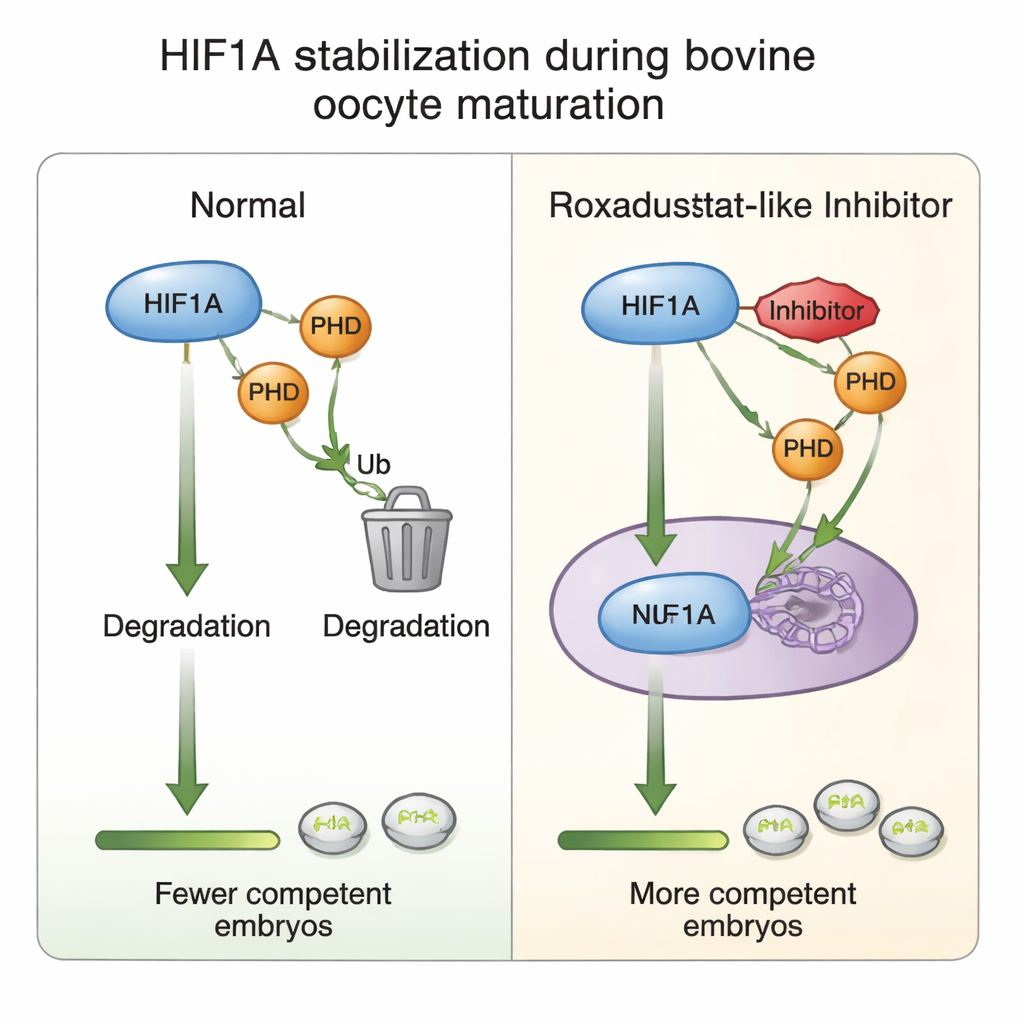
Dentro del ovario, cada ovocito en desarrollo está envuelto en un conjunto de células de soporte conocidas como cúmulo, formando conjuntamente un complejo cúmulo‑ovocito. Aunque el ovario recibe un mayor aporte sanguíneo a medida que los folículos crecen, los vasos sanguíneos no alcanzan el entorno inmediato del ovocito. El oxígeno debe difundirse, creando un bolsillo de oxigenación moderadamente baja, o hipoxia, alrededor del ovocito en maduración. En este nicho, un sensor intracelular llamado HIF1A ayuda a las células a adaptarse ajustando el metabolismo y la producción hormonal. Trabajos anteriores demostraron que bloquear HIF1A perjudica la maduración del ovocito y reduce drásticamente la formación de embriones, lo que sitúa a esta proteína como un coordinador central de la competencia ovocitaria—la capacidad de un óvulo para ser fecundado y desarrollarse hasta un embrión sano.
Usar un fármaco para afinar el sensor de oxígeno del óvulo
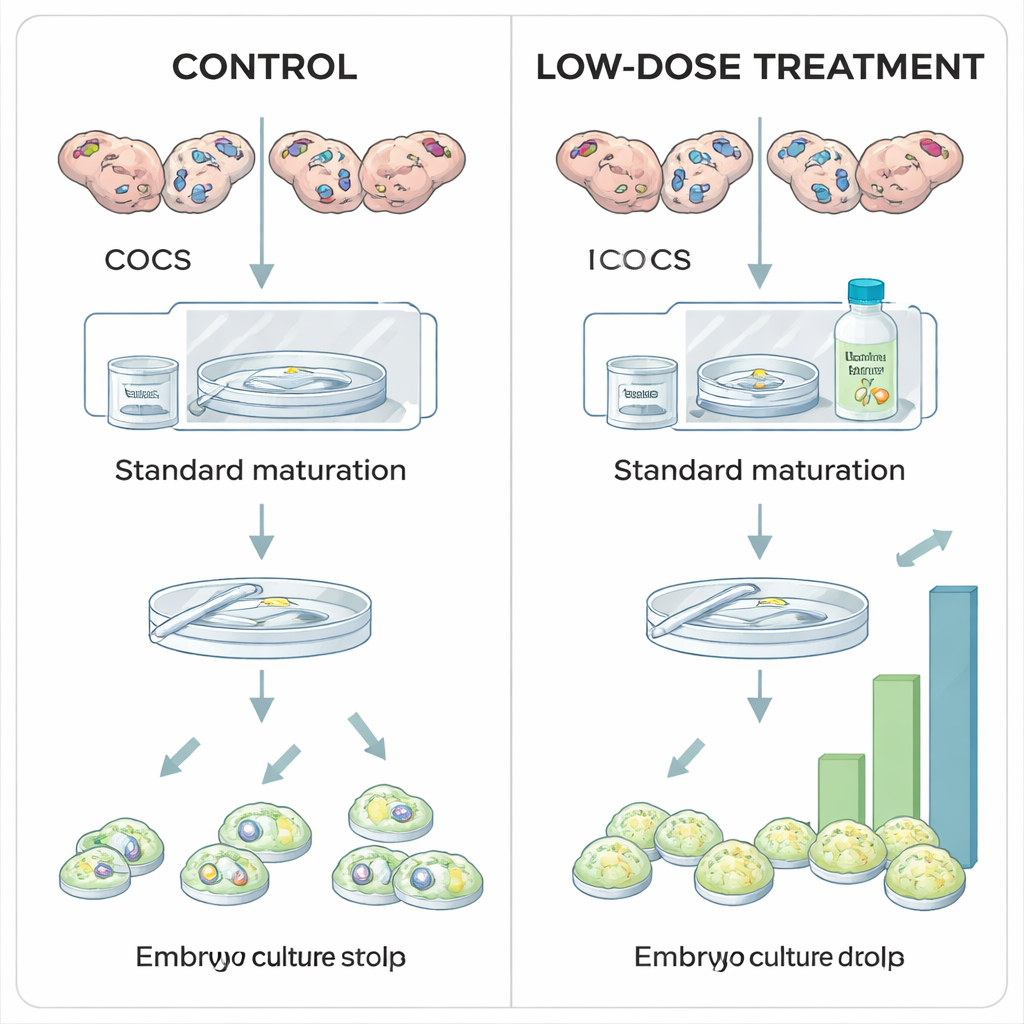
Los autores exploraron si estabilizar moderadamente HIF1A durante la maduración en laboratorio de ovocitos bovinos podría aumentar el rendimiento de embriones. En los protocolos in vitro estándar, los complejos cúmulo‑ovocito se maduran bajo niveles de oxígeno ambientales normales, en gran medida por razones prácticas más que biológicas. Aquí, los ovocitos recogidos de ovarios de matadero se dividieron en grupos y se expusieron durante su periodo de maduración de 24 horas a distintas dosis de Roxadustat, un fármaco ya utilizado en medicina humana para tratar la anemia. Roxadustat actúa bloqueando una familia de enzimas llamadas proil‑hidroxilasas (PHD) que normalmente etiquetan a HIF1A para su destrucción cuando el oxígeno es abundante. Al inhibir las PHD, Roxadustat permite la acumulación de la proteína HIF1A incluso a niveles más altos de oxígeno, recreando parcialmente la señal de hipoxia que el ovocito percibiría in vivo.
Más blastocistos con la dosis adecuada, daño a niveles altos
Al examinar cómo evolucionaron los ovocitos y los embriones tras el tratamiento, emergió un patrón claro. Una dosis baja de Roxadustat (25 micromolar) no cambió cuántos ovocitos completaron la maduración ni cuántos ovocitos fecundados iniciaron la división, pero aumentó significativamente la proporción que alcanzó la etapa de blastocisto. En otras palabras, los pasos iniciales no se vieron afectados, sin embargo más embriones completaron con éxito el exigente proceso hasta convertirse en blastocistos—lo que sugiere que una estabilización moderada de HIF1A mejora la calidad intrínseca del ovocito. En contraste, la dosis más alta (100 micromolar) redujo el porcentaje de ovocitos que maduraron en absoluto, y cuando el mismo inhibidor se aplicó más tarde, durante el periodo de cultivo embrionario de ocho días, las dosis altas recortaron bruscamente la formación de blastocistos sin alterar la división celular temprana. Estos hallazgos indican que "lo justo" de actividad de HIF1A durante la maduración es beneficioso, mientras que un exceso o una activación demasiado prolongada resulta perjudicial.
Qué ocurre dentro de las células de soporte del ovocito
Para entender cómo funciona este ajuste químico, los autores analizaron las células del cúmulo que rodean cada ovocito. Encontraron que la maduración en general eleva la actividad génica de HIF1A, pero añadir Roxadustat paradójicamente redujo el ARN mensajero de HIF1A mientras mantenía estables los niveles de proteína HIF1A—una pista de que las células pueden atenuar la expresión génica una vez que la proteína está suficientemente estabilizada, una especie de freno incorporado contra la sobreactivación. Los niveles de PHD2, la más sensible al oxígeno entre las enzimas PHD, aumentaron en respuesta al fármaco, reforzando su papel como parte del bucle de detección de oxígeno. A dosis más altas del fármaco, los marcadores de proliferación celular y de la matriz adhesiva que ayuda a las células del cúmulo a expandirse alrededor del ovocito se redujeron, en consonancia con la observada caída en la maduración y la formación embrionaria. Todo ello apoya la idea de que una actividad de HIF1A cuidadosamente equilibrada afina el diálogo entre el ovocito y las células del cúmulo que sustenta el éxito del desarrollo posterior.
Implicaciones para la cría animal y más allá
Este trabajo demuestra que estabilizar suavemente el sensor de oxígeno del ovocito durante la breve ventana de maduración in vitro puede aumentar y estabilizar de manera significativa los rendimientos de blastocistos en bovinos, sin alterar la fecundación ni las divisiones tempranas. En términos prácticos, eso podría traducirse en una producción de embriones más fiable para programas de cría, utilizando un fármaco dirigido en lugar de cambios burdos en los niveles de oxígeno o químicos más tóxicos. El estudio también subraya una lección más amplia aplicable a los tratamientos de fertilidad humana: imitar el matizado entorno de baja oxigenación del ovario no es simplemente subir o bajar el oxígeno, sino respetar el delicado equilibrio de moléculas de señalización como HIF1A. Afinar ese equilibrio, en lugar de llevarlo a extremos, puede ser una vía clave hacia embriones más sanos.
Cita: Gübeli, M., Bleul, U. & Kowalewski, M.P. Targeted hypoxia-inducible factor 1-alpha (HIF1A) stabilization during in vitro maturation of bovine cumulus-oocyte complexes increases blastocyst rates. Sci Rep 16, 7554 (2026). https://doi.org/10.1038/s41598-025-33894-8
Palabras clave: producción de embriones in vitro, maduración del ovocito, señalización por hipoxia, estabilización de HIF1A, reproducción bovina