Clear Sky Science · es
Regiones conservadas y clonación molecular de fosfatasas ácidas y alcalinas en Streptomyces sp. MMA-NRC
Por qué el fósforo del suelo importa para nuestros alimentos
La agricultura moderna depende en gran medida del fósforo, un ingrediente clave de los fertilizantes que ayuda a las plantas a construir ADN, almacenar energía y desarrollar raíces fuertes. Sin embargo, gran parte del fósforo que aplicamos al suelo se fija rápidamente en minerales insolubles que las plantas no pueden utilizar, mientras que las reservas mundiales de roca fosfática explotable son finitas y están distribuidas de forma desigual. Este estudio explora una alternativa biológica: aprovechar los microbios del suelo, e incluso bacterias modificadas, para liberar fósforo de la roca fosfática, lo que podría reducir nuestra dependencia de los fertilizantes químicos y mitigar los daños ambientales.
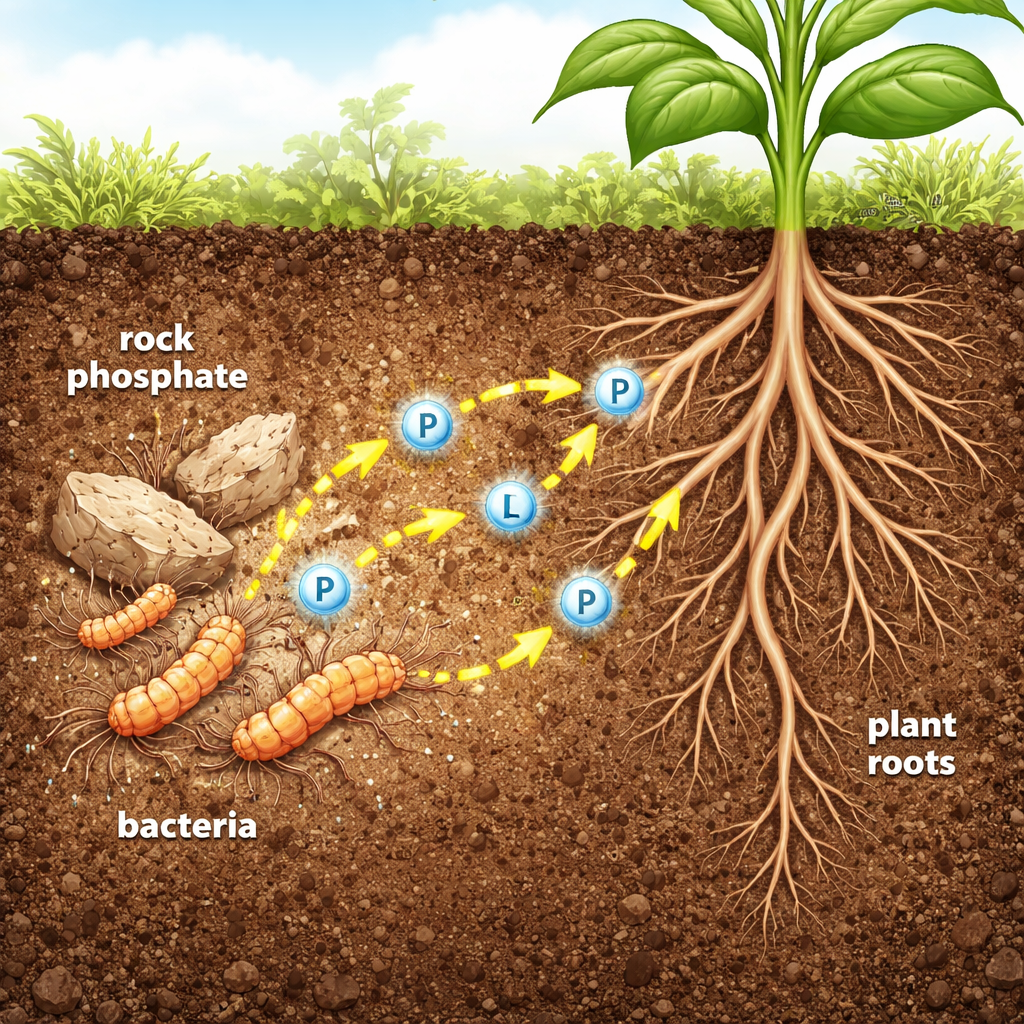
Pequeños ayudantes que liberan nutrientes “atorados”
En muchos suelos, la cantidad total de fósforo es alta, pero sólo una fracción mínima está en una forma que las raíces pueden absorber. El exceso de fertilizante no solo desperdicia dinero, sino que también se filtra hacia ríos y lagos, provocando proliferaciones de algas y zonas muertas. Los autores se centran en un grupo de bacterias del suelo llamadas Streptomyces, ya conocidas por producir antibióticos y enzimas potentes. Una cepa, nombrada Streptomyces sp. MMA-NRC, puede disolver el fosfato de roca, un fertilizante barato pero poco soluble. El equipo se propuso comprender y aprovechar dos de sus enzimas clave, la fosfatasa ácida y la fosfatasa alcalina, herramientas moleculares que cortan grupos que contienen fósforo de compuestos que de otro modo serían inutilizables.
Leer y modelar los planos de las enzimas
Primero, los investigadores aislaron los genes que codifican estas dos fosfatasas en la cepa MMA-NRC. Amplificaron y secuenciaron los genes, que resultaron codificar proteínas de 488 y 560 bloques constructores (aminoácidos), y depositaron las secuencias en bases de datos públicas. Con herramientas bioinformáticas, compararon estas proteínas con enzimas relacionadas de otras bacterias, mostrando que las versiones de MMA-NRC están estrechamente relacionadas —alrededor del 99% de similitud— con las de otra cepa de Streptomyces. Luego construyeron modelos tridimensionales detallados por ordenador de las enzimas, verificando su calidad con métodos establecidos que evalúan si cada aminoácido ocupa una posición realista. Los modelos superaron estas pruebas con puntuaciones altas, lo que sugiere que las estructuras virtuales se asemejan mucho a las reales.
Evaluar cuán bien las enzimas se adhieren al fosfato de roca
Con los modelos 3D en mano, los científicos realizaron simulaciones de “docking” para ver cuán fuertemente podrían unirse las enzimas al fosfato de roca, su sustrato objetivo. En estas simulaciones, la enzima y el mineral se reúnen en muchas orientaciones posibles, y un ordenador estima qué disposiciones son las más estables. Tanto las fosfatasas ácida como alcalina de MMA-NRC mostraron energías de unión predichas muy fuertes al fosfato de roca, lo que indica que deberían interactuar firmemente con la superficie mineral. Aminoácidos específicos en las enzimas formaron enlaces de hidrógeno y contactos hidrofóbicos con el modelo de fosfato de roca, delineando probables sitios activos donde tendrían lugar las reacciones químicas para liberar fósforo.
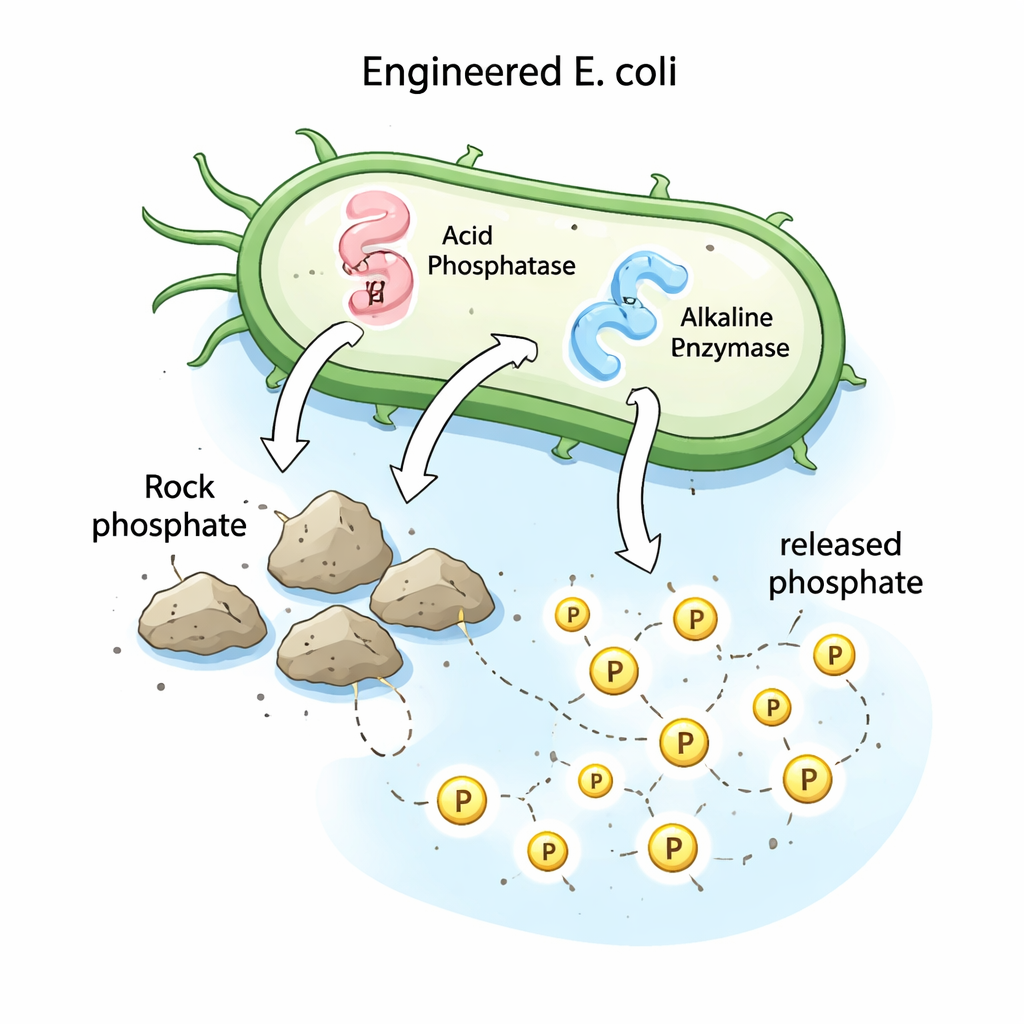
Convertir una bacteria de laboratorio en liberadora de fósforo
Para poner a prueba estas ideas experimentalmente y crear una herramienta práctica, el equipo trasladó los genes de las fosfatasas desde Streptomyces a una bacteria de laboratorio bien estudiada, Escherichia coli DH5α. Insertaron cada gen en un vector de clonación estándar y transformaron los plásmidos en E. coli, seleccionando colonias que incorporaron correctamente el ADN nuevo. Estas cepas recombinantes se cultivaron luego en un medio que contenía fosfato de roca como única fuente de fósforo. Mientras que la E. coli no modificada no pudo liberar fósforo medible, las cepas recombinantes que producían la fosfatasa ácida o alcalina liberaron alrededor de 53 y 57 miligramos de fósforo soluble por litro tras siete días, cifras muy superiores a las de la cepa original de Streptomyces, que liberó aproximadamente 35 miligramos por litro en las mismas condiciones.
Qué podría significar esto para una agricultura más verde
Para el público general, la conclusión es clara: al comprender y reutilizar las propias enzimas de la naturaleza, los científicos pueden convertir el fosfato de roca barato y poco soluble en una fuente de nutrientes más accesible para los cultivos. La alta actividad de las fosfatasas modeladas y clonadas sugiere que cepas como Streptomyces sp. MMA-NRC, o bacterias modificadas que porten sus genes, podrían convertirse en componentes de biofertilizantes que reduzcan la dependencia de los fertilizantes fosfatados convencionales. Tales soluciones biológicas podrían ayudar a los agricultores a mantener rendimientos mientras disminuyen la contaminación y alivian la presión sobre las limitadas reservas mundiales de fósforo, apoyando sistemas de producción de alimentos más sostenibles y resilientes.
Cita: Abd El-Aziz, N.M. Conserved regions and molecular cloning of Acid and Alkaline phosphatases in Streptomyces sp. MMA-NRC. Sci Rep 16, 7493 (2026). https://doi.org/10.1038/s41598-025-33881-z
Palabras clave: bacterias solubilizadoras de fosfato, biofertilizante, Streptomyces, enzima fosfatasa, fosfato de roca