Clear Sky Science · es
Hacia gemelos digitales de la electrofisiología cardíaca con un solucionador eficiente, de código abierto y escalable en clústeres GPU
Por qué importa construir corazones virtuales
Cuando los médicos tratan problemas del ritmo cardíaco, a menudo trabajan en parte a oscuras: pueden medir señales eléctricas en la superficie del cuerpo pero no pueden ver fácilmente cómo se propagan esas señales en el interior del corazón. Este estudio describe nuevas herramientas informáticas potentes que pueden simular el latido del corazón de una persona con gran detalle, y con la suficiente rapidez como para explorar muchos escenarios de “qué pasaría si”. Al combinar una anatomía cardíaca realista con procesadores gráficos de última generación, los autores nos acercan a experimentos virtuales seguros y de bajo coste sobre copias digitales de corazones individuales de pacientes.
De modelos simples a gemelos digitales
Las simulaciones cardíacas modernas pueden representar la actividad desde el nivel de células individuales hasta el órgano completo, pero reproducir fielmente cómo se mueve la electricidad por el corazón es tanto matemáticamente complejo como computacionalmente costoso. Un objetivo clave para la medicina es el “gemelo digital cardíaco”: un modelo informático personalizado que imite el corazón de un paciente específico y que pueda usarse para probar fármacos, dispositivos o estrategias de estimulación antes de aplicarlas en la clínica. Para que esto sea factible, el software que ejecuta estas simulaciones debe ser rápido y preciso, debe incluir estructuras anatómicas importantes y debe ser de acceso abierto para que investigadores de todo el mundo puedan verificarlo, mejorarlo y reutilizarlo.
Capturando el cableado oculto del corazón
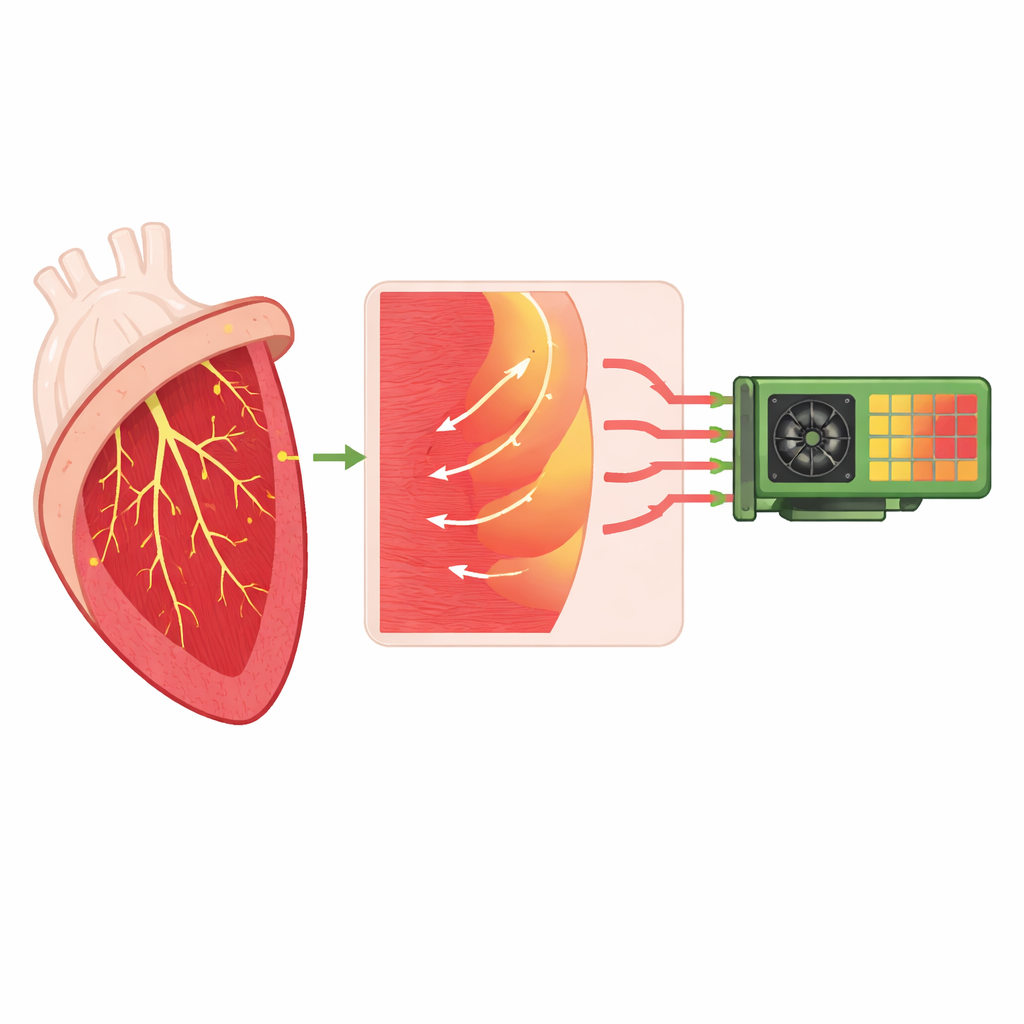
El trabajo se centra en un simulador de código abierto llamado monoalg3d, que modela cómo viajan las señales eléctricas a través del músculo cardíaco y su red de cableado especializada. Esa red, conocida como sistema de Purkinje, entrega rápidamente la señal desencadenante del latido desde las rutas de conducción superiores a muchos puntos de conexión diminutos repartidos por la superficie interna de los ventrículos. En cada una de estas junturas, una delgada fibra de Purkinje debe excitar una masa de músculo mucho mayor, lo que introduce un retraso natural y, en algunas condiciones, un riesgo de bloqueo o conducción anómala. Los autores mejoran monoalg3d para que represente este cableado y sus uniones de forma más realista, incluida la asimetría entre las señales que viajan de Purkinje a músculo y las que vuelven del músculo a la red.
Convertir supercomputadoras y GPU en laboratorios cardíacos
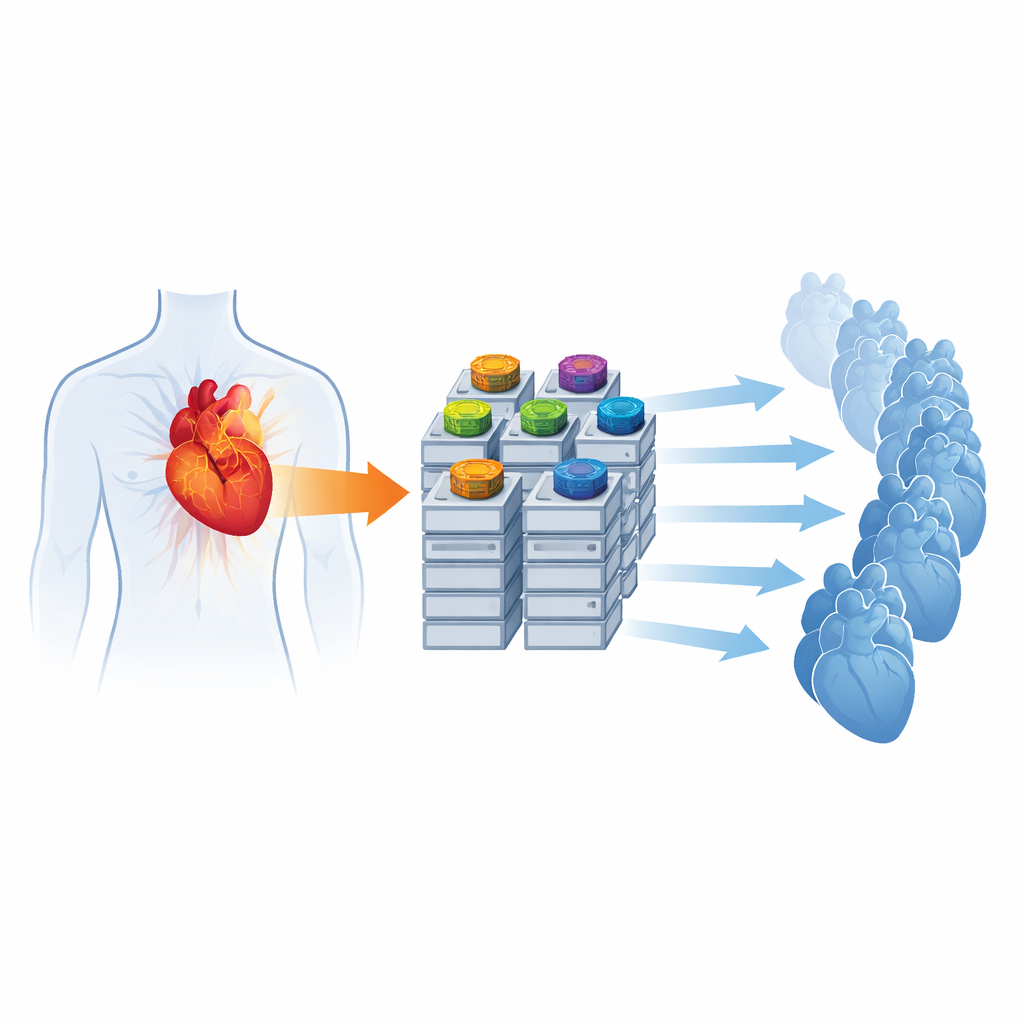
Para ejecutar modelos tan detallados con rapidez, el equipo reingeniería cómo el simulador usa el hardware. Rediseñan el núcleo numérico para que tanto la dinámica local de las células como la propagación del voltaje en el corazón se resuelvan directamente en unidades de procesamiento gráfico (GPUs), dispositivos creados originalmente para renderizar imágenes pero hoy ampliamente usados en computación científica. Organizando cuidadosamente los datos para las bibliotecas de GPU y evitando transferencias frecuentes entre CPU y GPU, muestran que una configuración completamente basada en GPU puede acelerar una prueba estándar casi once veces en comparación con una versión tradicional solo en CPU. También introducen un nuevo formato de salida compacto para reducir drásticamente las necesidades de almacenamiento y una función de paso de mensajes que puede lanzar cientos de simulaciones en paralelo en un superordenador, cada una explorando un conjunto distinto de parámetros fisiológicos.
Enseñar a los corazones virtuales a parecerse a pacientes reales
Más allá de la velocidad bruta, los autores prueban si su solucionador mejorado puede soportar simulaciones realistas y específicas de pacientes. Usando una reconstrucción tridimensional de un corazón humano a partir de imágenes médicas, añaden una red de Purkinje sintética y ajustan parámetros clave de las junturas: la resistencia en cada conexión y cuántas regiones musculares vecinas excita cada terminal de Purkinje. Barran automáticamente cientos de combinaciones de estos valores, ejecutando simulaciones que comienzan con un estímulo en el haz de conducción principal, y miden tanto los pequeños retrasos en cada juntura como las señales resultantes del electrocardiograma (ECG) en el pecho. Para una malla cardíaca de alta resolución, identifican elecciones de parámetros que producen tiempos de activación fisiológicamente plausibles y formas de onda del ECG que correlacionan bien con las grabaciones de un paciente real, todo ello manteniendo los tiempos de simulación individuales dentro de unas pocas horas incluso cuando se ejecutan 512 corridas concurrentes.
Muchos corazones posibles que se parecen por fuera
Un resultado intrigante es que diferentes configuraciones internas de cableado y fuerzas de las junturas pueden conducir a ECG muy similares en la superficie del cuerpo. En otras palabras, varios corazones digitales distintos pueden parecer igualmente consistentes con los mismos datos clínicos. Los autores muestran que algunas junturas de Purkinje son especialmente influyentes, con retrasos locales que varían sustancialmente entre simulaciones que encajan igualmente bien, mientras que el tiempo global de activación en los ventrículos se mantiene estable. Esta no unicidad sugiere que futuros marcos de gemelos digitales necesitarán datos o restricciones adicionales—como imágenes más detalladas o mediciones invasivas—para determinar una única configuración interna más probable para un paciente dado.
Qué significa esto para la atención futura
En resumen, este estudio entrega un simulador de acceso gratuito acelerado por GPU que puede manejar anatomía cardíaca detallada, cableado de conducción realista y grandes lotes de simulaciones personalizadas en clústeres informáticos modernos. Para no especialistas, el mensaje clave es que se está volviendo práctico ejecutar experimentos virtuales cardíacos rápidos y de alta fidelidad que se parecen a pacientes individuales, incluidos los retrasos sutiles en las junturas del cableado interno del corazón. Aunque se necesita más trabajo para personalizar por completo estos modelos y resolver las incertidumbres internas, las herramientas aquí presentadas constituyen un bloque de construcción importante para futuros diagnósticos, evaluación de riesgo y planificación de tratamientos basados en gemelos digitales en cardiología.
Cita: Berg, L.A., Oliveira, R.S., Camps, J. et al. Toward cardiac electrophysiology digital twins with an efficient open source scalable solver on GPU clusters. Sci Rep 16, 9619 (2026). https://doi.org/10.1038/s41598-025-33709-w
Palabras clave: gemelo digital cardíaco, simulación de la electrofisiología cardíaca, sistema de conducción de Purkinje, computación en GPU, cardiología personalizada