Clear Sky Science · es
Visualización in vivo de la dinámica extracelular de adenosina cardíaca y su modulación farmacológica en modelos de insuficiencia cardíaca en pez cebra
Por qué importa esta historia del corazón de un pez
La insuficiencia cardíaca sigue siendo una de las principales causas de muerte en todo el mundo, y muchos pacientes empeoran a pesar de los mejores fármacos disponibles. Los científicos saben que las células cardíacas estresadas liberan señales químicas de "auxilio" a su entorno, pero ha sido difícil observar estas señales en acción dentro de un corazón que late. Este estudio utiliza peces cebra transparentes, cuyos diminutos corazones imitan estrechamente rasgos clave de los corazones humanos, para observar esas señales de peligro en tiempo real y probar una nueva forma de atenuarlas.
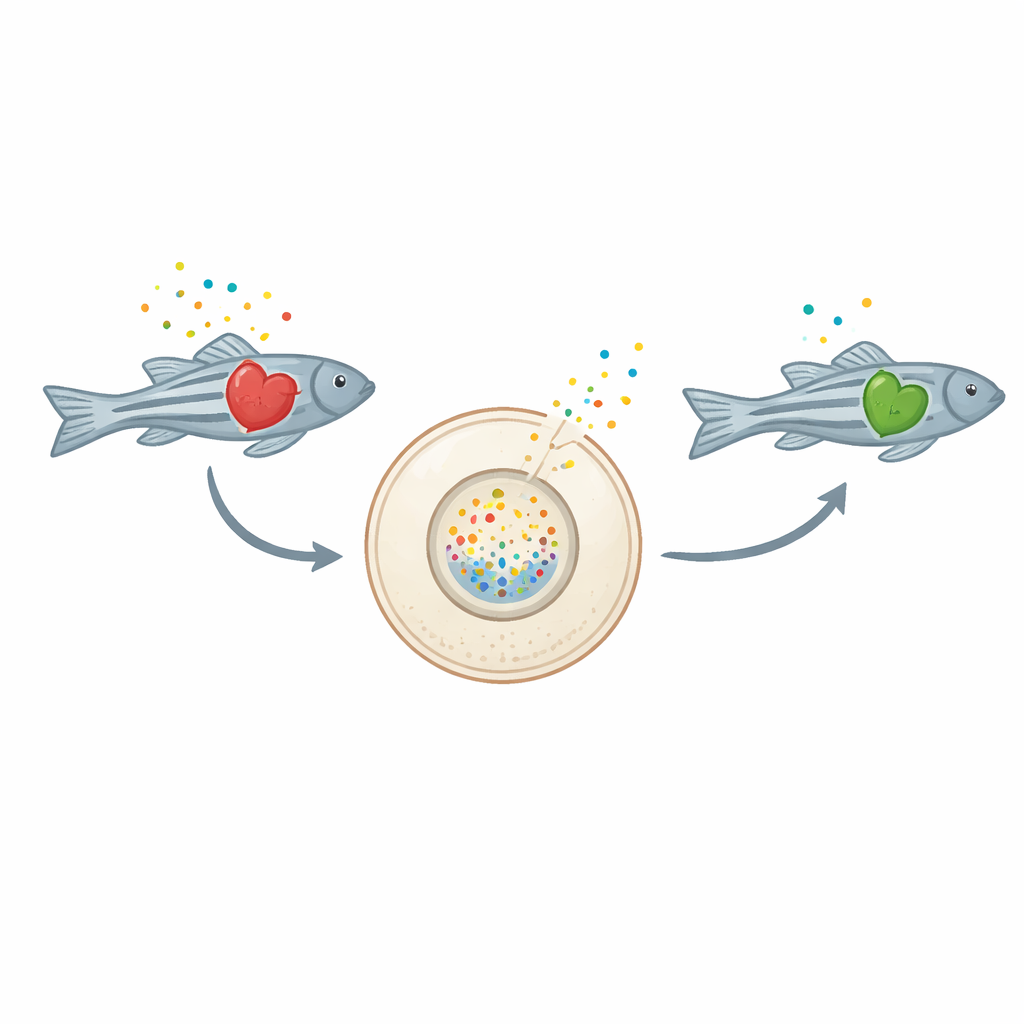
Señales de un corazón que sufre
Cuando las células cardíacas resultan dañadas, liberan moléculas portadoras de energía como el ATP y su producto de degradación, la adenosina, al espacio extracelular. Fuera de la célula, estas mismas moléculas dejan de actuar como combustible y se comportan como mensajes urgentes que pueden avivar la inflamación. En la insuficiencia cardíaca crónica, esa respuesta inflamatoria puede sobreactivarse y dañar aún más el corazón. Hasta ahora, sin embargo, los investigadores carecían de evidencia directa, en el propio organismo, de cómo se comportan estas moléculas a lo largo del tiempo en un corazón en fallo.
Convertir al pez cebra en una cámara química viva
El equipo diseñó peces cebra cuyas células cardíacas producen en su superficie una proteína sensor fluorescente especial llamada GRABAdo. Cuando la adenosina se acumula fuera de las células, este sensor emite un brillo verde más intenso, convirtiendo efectivamente cada pequeño corazón en una cámara química viva. Los investigadores provocaron luego insuficiencia cardíaca en los peces con terfenadina, un fármaco conocido por alterar el ritmo cardíaco y debilitar el bombeo. A medida que los peces mostraron signos claros de insuficiencia —latidos más lentos, ventrículos agrandados y debilitados, edema alrededor del corazón y peor capacidad de nado—, los sensores cardíacos se encendieron, revelando un aumento marcado de adenosina extracelular. Medidas químicas en larvas completas confirmaron que los niveles totales de adenosina eran más altos en los corazones fallidos.
Cerrando la válvula de salida
Los científicos se preguntaron si reducir estas señales de peligro podría proteger el corazón. Se centraron en VNUT, un transportador que carga ATP en pequeñas vesículas celulares para su liberación al exterior. Usando clodronato, un fármaco que bloquea VNUT, disminuyeron la liberación de ATP y, de forma indirecta, la acumulación de adenosina alrededor de las células cardíacas. En peces cebra con insuficiencia cardíaca inducida por fármaco, la inhibición de VNUT preservó la morfología cardíaca, redujo la dilatación de las cámaras, mejoró la frecuencia y la fuerza de contracción y mantuvo un mejor flujo sanguíneo. El sensor de adenosina brillante se atenuó, mostrando que había menos señal de auxilio fuera de las células. Efectos protectores similares se observaron en ejemplares adultos con una forma aguda y de rápido desarrollo de insuficiencia cardíaca.
Varios frenos protectores que actúan en conjunto
La insuficiencia cardíaca implica más de una vía, por lo que los investigadores analizaron cómo la inhibición de VNUT interactúa con otros actores conocidos. Fármacos que bloquean ciertos receptores de adenosina y receptores de ATP, así como un compuesto que limita la fuga pasiva de ATP a través de canales de membrana, ayudaron por separado a los corazones de pez cebra. Cuando se combinaron con la inhibición de VNUT, muchos de estos tratamientos produjeron beneficios aditivos, lo que sugiere que reducir la señalización de purinas en varios puntos puede ser especialmente potente. La inhibición de VNUT también contribuyó a restaurar el equilibrio del calcio en las células cardíacas, esencial para un latido normal, y redujo tanto la muerte celular como la actividad de genes asociados a la inflamación. En conjunto, estos resultados sitúan a VNUT como un interruptor central que enlaza la liberación de ATP, la inflamación, el desorden en el manejo del calcio y el daño cardíaco progresivo.
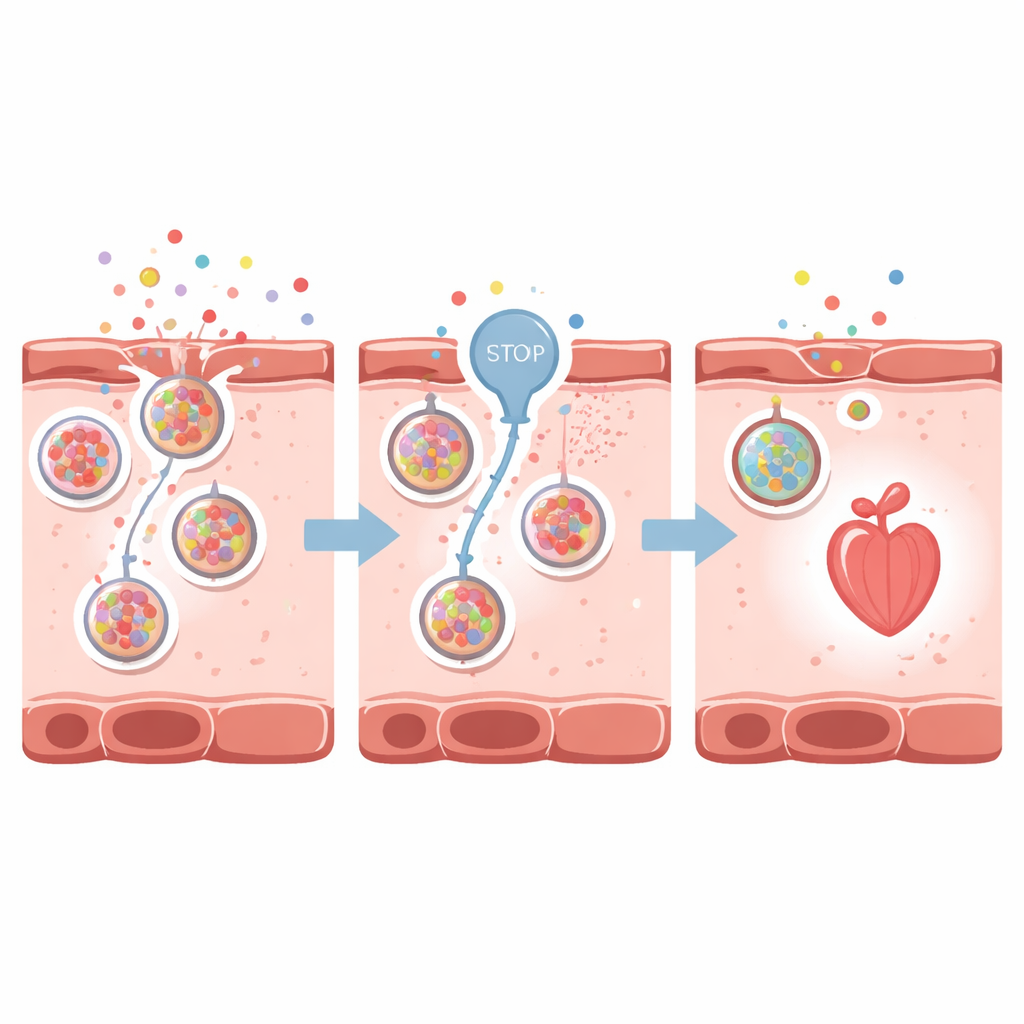
De los tanques de peces a futuras terapias
Para el público no especializado, el mensaje clave es que el estudio visualiza directamente una señal química de estrés que aumenta en corazones en fallo y demuestra que bloquear su liberación puede proteger la función cardíaca en un animal vivo. Aunque los corazones de pez cebra son más simples que los humanos, comparten suficiente biología para ofrecer un banco de pruebas potente para nuevas ideas. Al revelar a VNUT como un objetivo prometedor en la intersección entre inflamación e inestabilidad eléctrica, este trabajo sugiere que las futuras terapias para la insuficiencia cardíaca podrían hacer más que apoyar el flujo sanguíneo: podrían calmar activamente las conversaciones celulares nocivas que empujan al corazón hacia el fallo.
Cita: Phurpa, P., Apolinario, M.E.C., Umeda, R. et al. In vivo visualization of cardiac extracellular adenosine dynamics and its pharmacological modulation in zebrafish heart failure models. Sci Rep 16, 8220 (2026). https://doi.org/10.1038/s41598-025-30303-y
Palabras clave: insuficiencia cardíaca, señalización de adenosina, modelo de pez cebra, inflamación, protección cardíaca