Clear Sky Science · es
Intermedios de G-cuádruplex teloméricos revelados por análisis complejo de redes de Markov
Nudos ocultos en los extremos de nuestro ADN
En las puntas de nuestros cromosomas se encuentran unas tapas protectoras llamadas telómeros, a menudo comparadas con los remates de plástico de los cordones de las zapatillas. En estas regiones, el ADN puede plegarse sobre sí mismo formando nudos inusuales de cuatro hebras conocidos como G-cuádruplexes. Estas diminutas estructuras pueden influir en el comportamiento de nuestros genes y en cómo envejecen las células o se vuelven cancerosas. Este estudio mira entre bastidores cómo uno de esos nudos se deshace gradualmente, usando simulaciones informáticas detalladas y un análisis de datos avanzado para revelar formas fugaces que casi es imposible captar en experimentos.
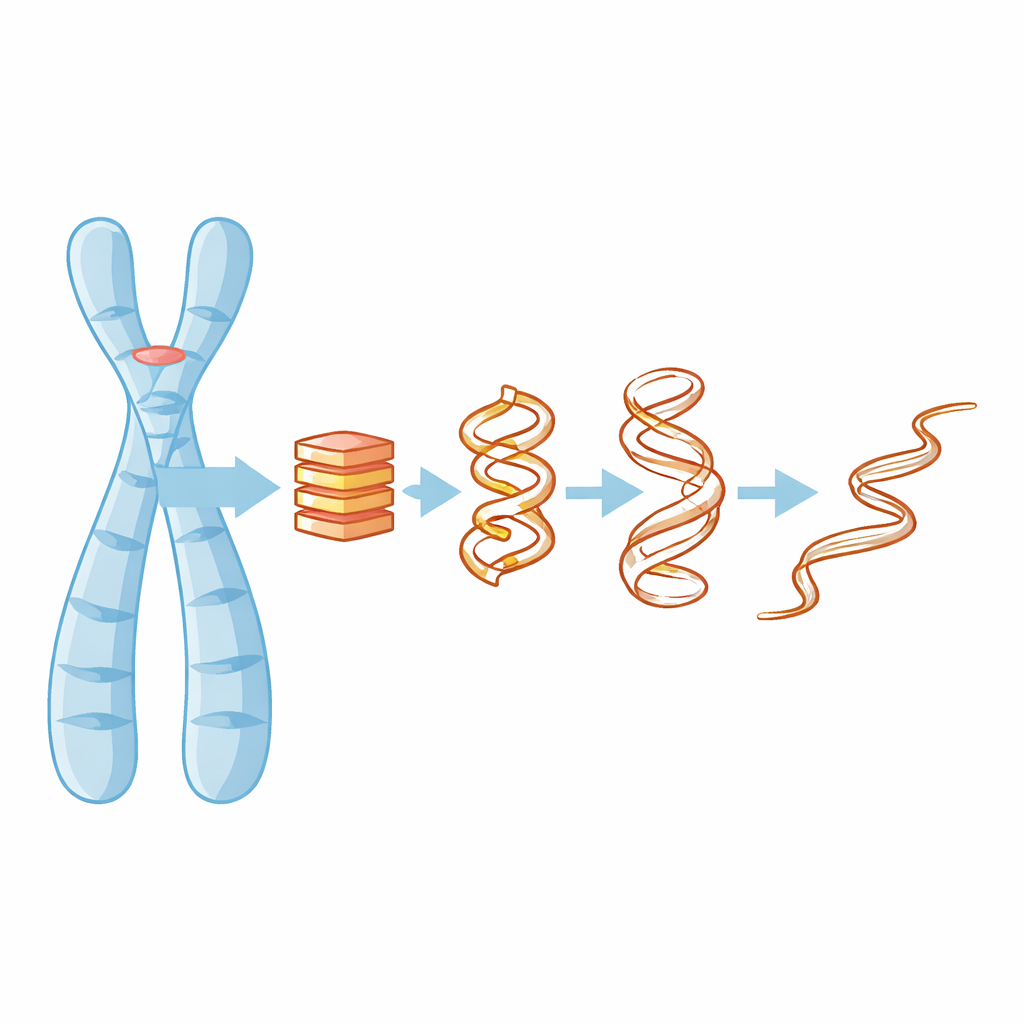
Por qué importan los nudos de ADN de cuatro hebras
La mayoría aprendemos que el ADN es una doble hélice, pero en tramos ricos en guanina —como los de los telómeros— la molécula puede plegarse en pilas compactas de cuatro hebras llamadas G-cuádruplexes. Estas pilas se mantienen gracias a capas planas de bases de guanina y a pequeños iones con carga positiva, como el potasio, que se sitúan en el centro y ayudan a pegar todo. Cuando un G-cuádruplex se forma o se deshace, puede bloquear o exponer partes del genoma, afectando la actividad génica, la replicación del ADN e incluso cómo las células cancerosas mantienen sus telómeros. Entender cómo estas estructuras pierden su forma es por tanto clave para diseñar fármacos que las apunten o para predecir cuándo pueden fallar.
Observando cómo se deshace un nudo molecular
Los investigadores se centraron en un G-cuádruplex telomérico humano en el que cuatro segmentos de una misma hebra de ADN se alinean en paralelo y se apilan formando una columna compacta. Usaron simulaciones de dinámica molecular con todos los átomos —experimentos virtuales que siguen el movimiento de cada átomo— para calentar ocho copias de esta estructura a temperaturas cercanas a su punto de fusión. Para ayudar al sistema a explorar distintas conformaciones, emplearon una estrategia llamada intercambio de réplicas, donde simulaciones a diferentes temperaturas intercambian configuraciones ocasionalmente. En siete de los ocho casos el G-cuádruplex permaneció unido; en uno, se desplegó por completo. Ese raro evento de desdoblamiento se convirtió en un estudio de caso detallado, mostrando no solo el antes y el después, sino toda una secuencia de formas intermedias a lo largo del proceso.
El papel crucial de los iones diminutos
Un hallazgo central es que los iones pequeños dentro del G-cuádruplex actúan como pasadores. Mientras al menos un ion quede anidado entre las capas de guanina, la estructura se mantiene mayormente intacta, quizá algo aflojada pero todavía reconocible. Sin embargo, cuando ambos iones abandonan finalmente el canal central, la pila se desestabiliza rápidamente. Las capas de guanina se deforman y hebras individuales se desprenden, y el ADN en conjunto se vuelve más extendido y flexible. Otras moléculas simuladas que perdieron solo un ion entraron en estados tambaleantes pero aún parcialmente ordenados, lo que sugiere que el desdoblamiento completo exige la pérdida de ambos iones estabilizadores —una pista de por qué algunos G-cuádruplexes son tan tenazmente robustos en la célula.
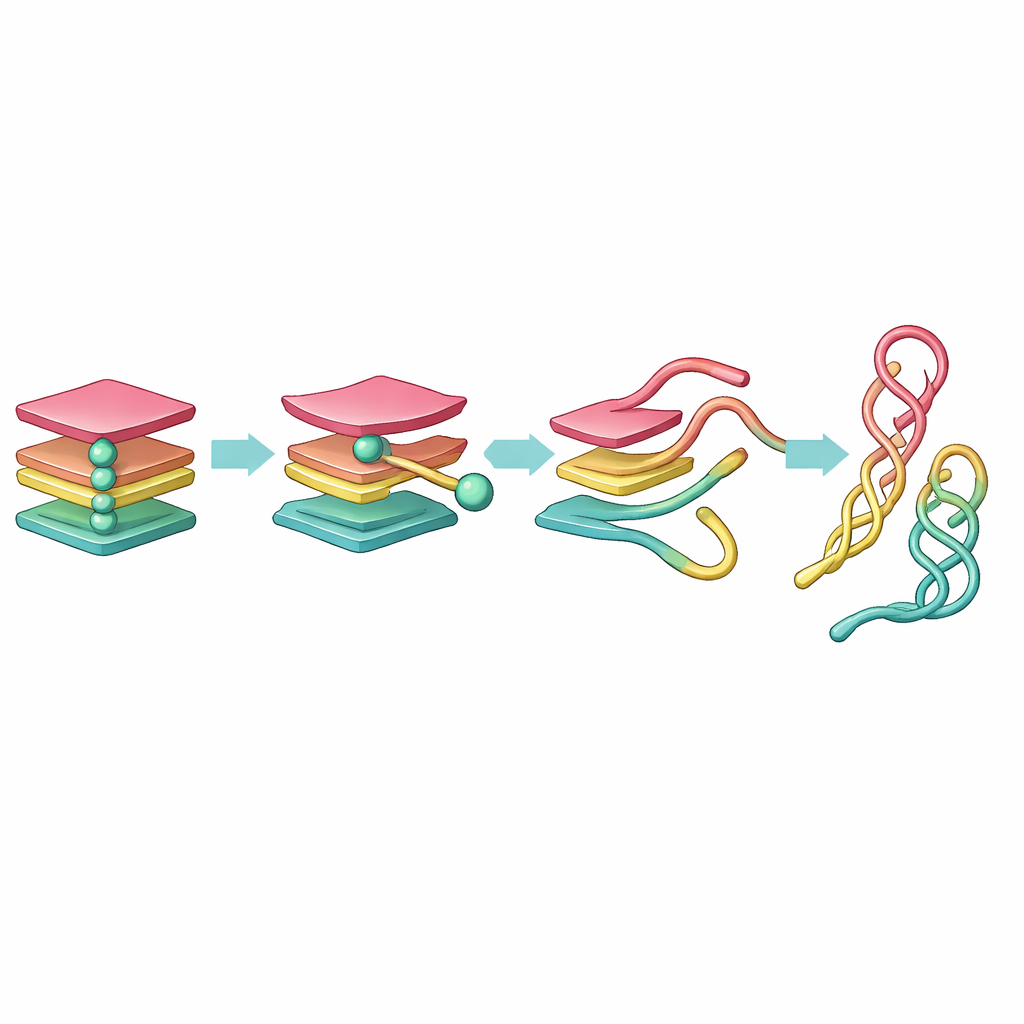
Descubriendo puntos intermedios ocultos en el recorrido
La simulación en bruto produjo una cantidad enorme de datos, demasiado complejos para interpretarlos a simple vista. Para domarlos, el equipo primero simplificó el ADN representando cada base como una única perla, y luego usó herramientas matemáticas para reducir el movimiento a solo unas pocas coordenadas clave. Aplicaron dos métodos: Análisis de Componentes Principales (PCA), que destaca las direcciones de mayor movimiento, y Análisis de Componentes Tiempo-independientes (tICA), que filtra los cambios lentos y duraderos que marcan verdaderos desplazamientos estructurales. A partir de estas coordenadas reducidas construyeron las llamadas redes conformacionales de Markov, en las que cada nodo es una forma típica del ADN y los enlaces muestran cómo la molécula salta de una forma a otra.
Una ruta preferente del nudo a la hebra suelta
Esta visión en forma de red reveló una vía clara de desdoblamiento. Partiendo de un G-cuádruplex completamente plegado, una hebra se desprende primero, formando un estado de tres hebras denominado «tríplex». Ese tríplex luego se reorganiza en una «horquilla» de dos hebras y en un conjunto de hebras sueltas cercanas. La horquilla y una disposición relacionada en «cruz-horquilla» resultan sorprendentemente longevas, actuando como puntos de parada estables en el viaje desde un nudo apretado hasta una configuración de ADN más relajada. Mientras que PCA dividió esta progresión en muchos estados de aspecto similar, tICA la destiló en un conjunto pequeño de pasos distintos y con significado cinético, mostrando que las formas tipo tríplex son de corta duración, mientras que las tipo horquilla perduran mucho más.
Qué significa esto para la biología y la medicina
Para un público no especializado, el mensaje clave es que los G-cuádruplexes teloméricos no pasan simplemente de plegados a desplegados. En su lugar, se funden a través de una serie de formas de vida corta y de mayor duración, con pequeños iones que actúan como guardianes de la estabilidad. Las simulaciones sugieren que los intermedios de tres hebras son efímeros, mientras que las horquillas de dos hebras y las formas en cruz son puntos de reposo más estables. Dado que estos estados intermedios también pueden aparecer en la dirección inversa, de plegamiento, probablemente sean cruciales en cómo los G-cuádruplexes se forman, cambian e interactúan con fármacos potenciales. Cartografiar este paisaje oculto de formas acerca a los científicos un paso más a diseñar moléculas que estabilicen o desestabilicen selectivamente estos nudos de ADN en la lucha contra el cáncer y otras enfermedades.
Cita: Sáinz-Agost, A., Falo, F. & Fiasconaro, A. Telomeric G-quadruplex intermediates unveiled by complex Markov network analysis. Sci Rep 16, 8308 (2026). https://doi.org/10.1038/s41598-025-29993-1
Palabras clave: G-cuádruplex, ADN telomérico, dinámica molecular, plegado de ADN sin proteínas, terapéuticas contra el cáncer