Clear Sky Science · es
Un conjunto de datos transcriptómicos unicelulares que perfila la lesión cerebral traumática y la terapia génica basada en NeuroD1 en ratones
Por qué las lesiones cerebrales nos importan a todos
Cada año, millones de personas reciben golpes en la cabeza por caídas, choques, deportes o combate. Estas lesiones cerebrales traumáticas pueden dejar secuelas duraderas en la memoria, el movimiento y el estado de ánimo, y los tratamientos actuales en su mayoría gestionan los síntomas en lugar de reparar verdaderamente el cerebro. Este estudio explora un enfoque prometedor basado en genes en ratones que pretende no solo limitar el daño, sino ayudar al cerebro a reconstruirse desde dentro, y cartografía estos cambios célula por célula para crear un recurso público útil para terapias futuras.
Mirando dentro del cerebro lesionado
Cuando el cerebro se lesiona, no se magulla simplemente como un músculo. Se desencadena una cadena de reacciones complejas: las neuronas mueren, el flujo sanguíneo se altera y células de soporte llamadas astrocitos y células inmunitarias acuden al lugar. Los astrocitos normalmente ayudan a nutrir a las neuronas y a mantener el equilibrio de la señalización cerebral, pero tras un trauma pueden formar una cicatriz densa e impulsar una inflamación persistente. Los autores usaron una herida por cuchillada controlada en la corteza de ratones para imitar ciertas formas de lesión penetrante del cerebro y luego examinaron cómo respondió cada tipo celular importante del tejido afectado a lo largo del tiempo. Aplicaron una técnica llamada secuenciación de ARN unicelular, que lee qué genes están activados en decenas de miles de células individuales, permitiendo un censo detallado de cómo cambia la comunidad celular del cerebro tras la lesión.
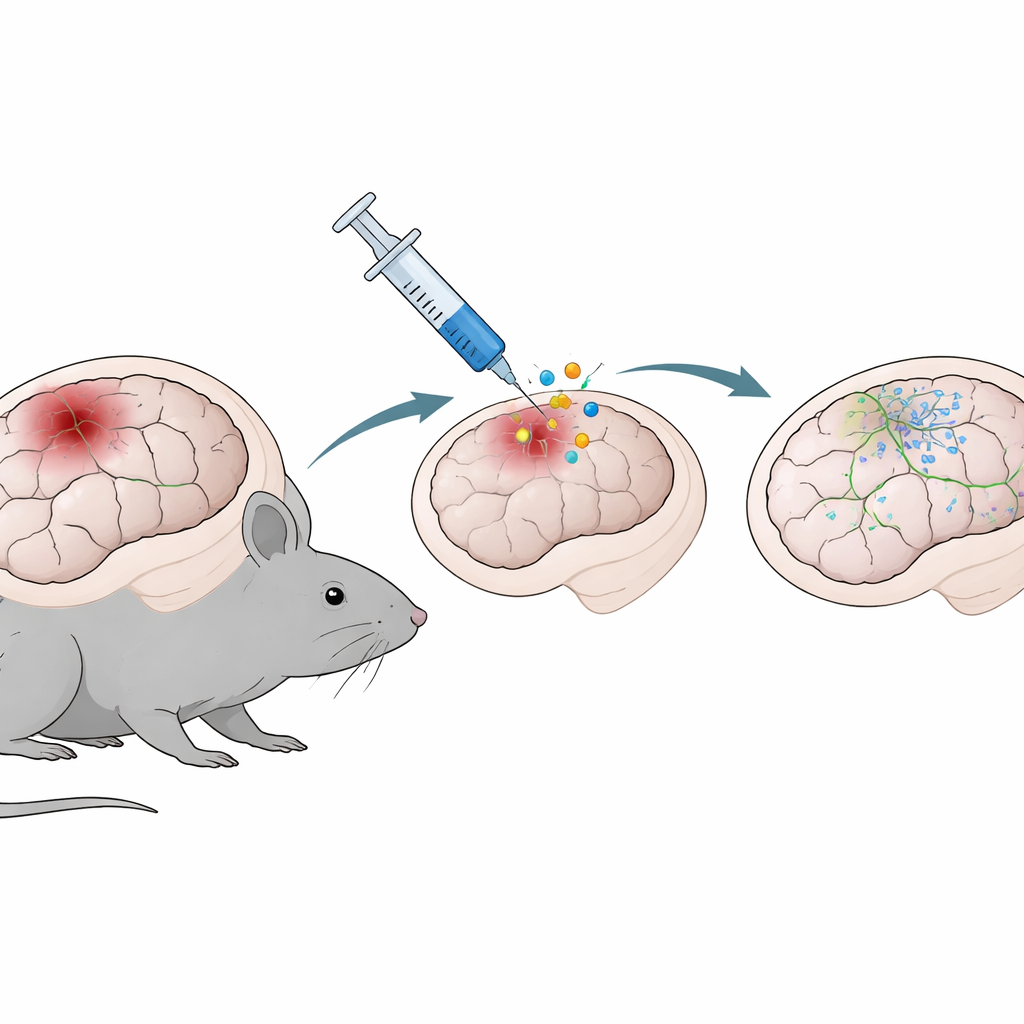
Una terapia génica que recluta células de soporte del cerebro
Dado que los astrocitos son abundantes y están presentes justo en el sitio de la lesión, son objetivos atractivos para estrategias de reparación. El equipo probó una terapia génica basada en NeuroD1, un gen conocido por impulsar a las células hacia un estado similar al neuronal. Usando un vector viral inofensivo inyectado en la zona cortical dañada tres días después de la lesión, administraron o bien un marcador neutral (GFP) o NeuroD1 a los astrocitos. Al examinar los cerebros una y dos semanas después, los ratones que recibieron NeuroD1 mostraron cavidades tisulares más pequeñas donde había ocurrido el daño y menos células inmunitarias activadas llamadas microglía alrededor de la lesión. En otras palabras, la terapia no solo redujo el daño estructural visible, sino que también apaciguó la respuesta inflamatoria local.
Rastreando los tipos celulares uno por uno
Para entender qué había detrás de estas mejoras, los investigadores compararon tres grupos de muestras corticales: ratones sanos, ratones lesionados que recibieron el virus de control y ratones lesionados que recibieron el virus con NeuroD1. Secuenciaron más de 97 000 células individuales en total y las agruparon según sus patrones de actividad genética en residentes cerebrales familiares, incluyendo neuronas, astrocitos, oligodendrocitos (que aíslan las fibras nerviosas), microglía y células que recubren los vasos sanguíneos y las cavidades cerebrales. Solo la lesión desplazó este equilibrio hacia más astrocitos y microglía y menos neuronas y células formadoras de mielina, reflejando cicatrización e inflamación. Con el tratamiento con NeuroD1, este sesgo empezó a revertirse: aumentaron las fracciones de neuronas, oligodendrocitos y células epiteliales del plexo coroideo, mientras que los astrocitos y la microglía dejaron de dominar tanto en la zona lesionada.
El trabajo oculto de los subtipos de astrocitos
Resultó que los astrocitos no son una población uniforme. Al reanalizarlos por separado, el equipo identificó siete subclústeres astrocitarios distintos, cada uno con su propia firma génica y comportamiento a lo largo de las tres condiciones. Algunos subclústeres eran comunes en tejido sano pero casi desaparecían tras la lesión, mientras que otros aparecían solo después del trauma. En cerebros lesionados tratados con el virus de control, varios grupos de astrocitos activaron programas relacionados con la construcción y remodelado de sinapsis —las uniones donde las neuronas se comunican— mientras reducían genes vinculados a la producción de energía en las mitocondrias. Este patrón sugiere que, tras la lesión, los astrocitos promovían cambios anómalos en el cableado mientras funcionaban con menor potencia metabólica.
Cómo NeuroD1 reequilibra la energía y el cableado celular
El tratamiento con NeuroD1 reconfiguró estos subclústeres astrocitarios en una dirección diferente. En varios grupos de astrocitos asociados a la lesión, se restauraron genes relacionados con la actividad mitocondrial, la respiración celular y el metabolismo energético general, mientras que se atenuaron genes ligados a la construcción excesiva de sinapsis y al remodelado de la mielina. En otras palabras, NeuroD1 pareció reactivar los motores energéticos de estas células y moderar los intentos descontrolados de reconfiguración que podrían contribuir a la disfunción. Algunos subtipos de astrocitos que se habían expandido drásticamente tras la lesión se redujeron en presencia de NeuroD1, mientras que otros asociados a funciones más saludables aumentaron. Estos cambios detallados aportan pistas sobre qué estados astrocitarios son perjudiciales y cuáles podrían favorecer la reparación.
Qué significa esto para la reparación cerebral futura
Este trabajo aún no ofrece una cura lista para usar para la lesión cerebral humana, pero aporta dos avances importantes. Primero, muestra en un cerebro mamífero vivo que una terapia génica dirigida puede disminuir la pérdida de tejido y la inflamación al tiempo que empuja a las poblaciones celulares y al uso de energía hacia un estado más saludable. Segundo, pone a disposición un rico conjunto de datos unicelulares público que otros científicos pueden explotar para identificar tipos celulares, genes y vías concretas que impulsan el daño o la recuperación tras el trauma. Para los lectores fuera del laboratorio, el mensaje clave es que las propias células de soporte del cerebro pueden ser reclutadas y reprogramadas potencialmente para ayudar a reconstruir circuitos lesionados, acercándonos un paso más a tratamientos que restauren, en lugar de simplemente estabilizar, la función cerebral tras un golpe traumático.
Cita: Chen, R., Zhang, S., Liu, S. et al. A single-cell transcriptomic dataset profiling traumatic brain injury and NeuroD1-based gene therapy in mice. Sci Data 13, 406 (2026). https://doi.org/10.1038/s41597-026-06788-1
Palabras clave: lesión cerebral traumática, terapia génica, astrocitos, secuenciación unicelular, NeuroD1