Clear Sky Science · es
Conjunto de imágenes histológicas a gran escala con metadatos sobre el microambiente del cáncer colorrectal
Por qué importa cartografiar el vecindario oculto del cáncer
Cuando los médicos observan un tumor de colon al microscopio, no solo ven células cancerosas; ven un vecindario activo de grasa, células inmunitarias, tejido conectivo y más. Esta mezcla de tipos celulares, denominada microambiente tumoral, influye de forma determinante en cómo responde un paciente al tratamiento y en su supervivencia. Sin embargo, las herramientas informáticas que podrían ayudar a los médicos a interpretar estas escenas complejas se han visto limitadas por un problema sencillo: no han contado con suficientes imágenes bien etiquetadas para aprender. Este estudio presenta una de las colecciones de imágenes de tejido colorrectal mejor anotadas y de mayor tamaño jamás reunidas, diseñada específicamente para entrenar y evaluar sistemas modernos de inteligencia artificial.
Construyendo una enorme biblioteca de imágenes de tumores de colon
Los investigadores crearon un recurso que denominan HMU-CRC-Hist550K, construido a partir de muestras de tejido de 500 pacientes tratados por cáncer colorrectal en un gran hospital oncológico de China. El tumor de cada paciente se conservó, se tiñó según el método estándar utilizado en laboratorios de patología y se escaneó como una lámina digital de alta resolución. A partir de estas láminas, el equipo recortó automáticamente pequeñas baldosas cuadradas de imagen, cada una del tamaño aproximado de lo que un patólogo puede ver a la vez bajo el microscopio. En total, produjeron alrededor de 550 000 baldosas, ofreciendo a los modelos de inteligencia artificial un conjunto enorme y variado de ejemplos para aprender cómo se ven los distintos tejidos.
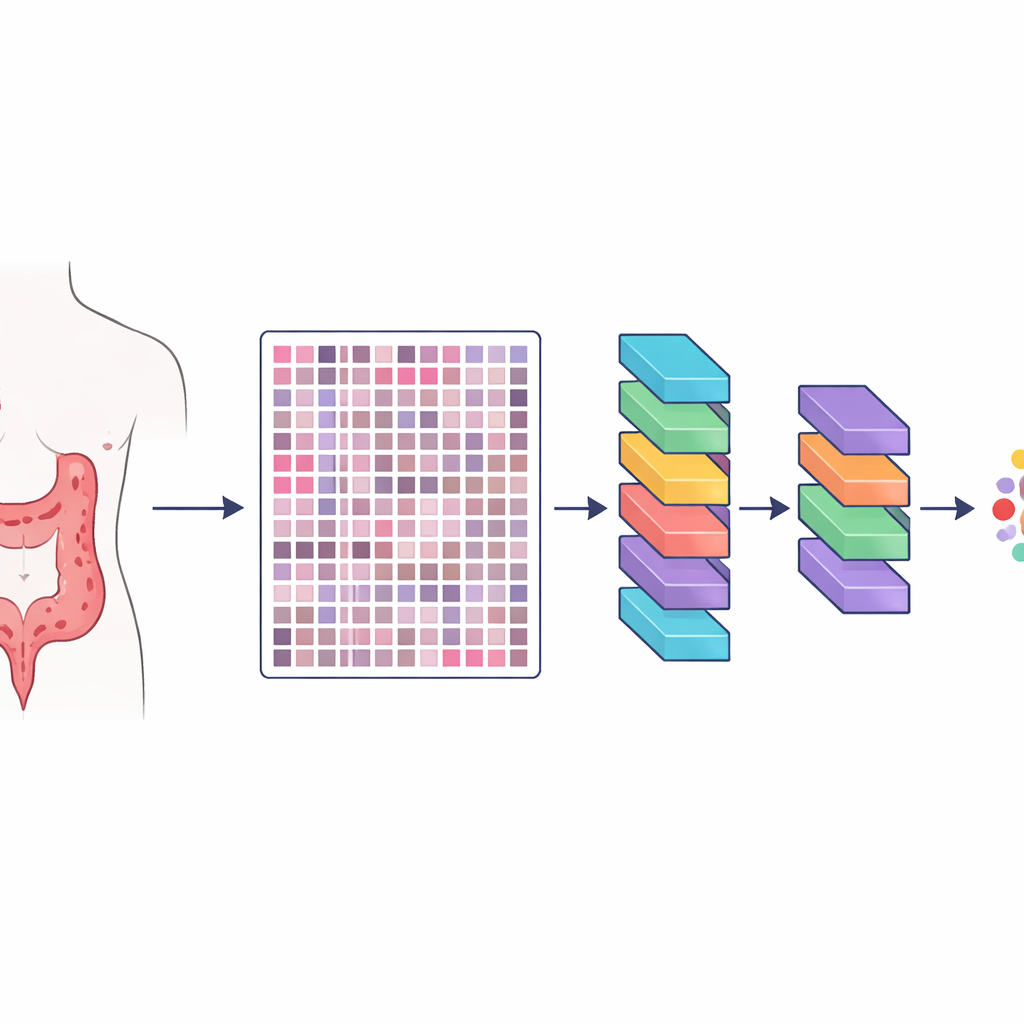
Etiquetado humano cuidadoso del paisaje tumoral
Crear una gran biblioteca de imágenes no basta; las imágenes deben estar etiquetadas con precisión. Tres patólogos experimentados trabajaron conjuntamente mediante un proceso de tres pasos para señalar ocho componentes clave del entorno del tumor: tejido adiposo, detritos celulares, células inmunitarias llamadas linfocitos, moco, músculo liso, mucosa normal del colon, tejido conectivo de sostén alrededor del tumor y las propias células cancerosas. Dos patólogos dibujaron primero regiones en las láminas grandes de forma independiente y luego revisaron el trabajo del otro. Un especialista sénior realizó una revisión final, resolviendo desacuerdos y excluyendo áreas poco claras. Esta comprobación cruzada redujo considerablemente el sesgo personal y produjo etiquetas altamente consistentes y detalladas, de modo que cada baldosa queda vinculada a un tipo de tejido concreto dentro del vecindario tumoral.
Conectando las vistas del microscopio con la historia clínica
Lo que hace a este conjunto de datos especialmente potente es que las imágenes están emparejadas con información clínica rica para cada paciente. Para cada caso, el equipo recogió datos básicos como edad y sexo, así como estadio tumoral, localización del tumor a lo largo del colon y recto, el grado de anormalidad de las células cancerosas, si hubo invasión de nervios o ganglios linfáticos y cuánto tiempo sobrevivió el paciente tras el tratamiento. También registraron resultados de pruebas de laboratorio comunes que reflejan la composición genética y proteica del tumor. Se eliminaron todos los identificadores personales para que los pacientes no puedan ser reconocidos. Al combinar los patrones tisulares con estas características clínicas, los investigadores pueden explorar cómo determinadas configuraciones del microambiente se relacionan con resultados reales, como qué pacientes evolucionan mejor o peor.
Poniendo a prueba la IA con el nuevo conjunto de datos
Para demostrar la utilidad del conjunto de datos, los científicos entrenaron tres modelos distintos de aprendizaje profundo —sistemas modernos de reconocimiento de patrones que destacan en tareas de imagen— para identificar los ocho tipos de tejido en las baldosas. Emplearon reglas estrictas para dividir a los pacientes entre los grupos de entrenamiento y de prueba, de modo que los modelos fueran evaluados con pacientes que nunca habían visto antes. Los modelos, que incluyen tanto redes de imagen clásicas como un diseño más reciente de «transformador de visión», alcanzaron todos una precisión muy alta, con puntuaciones de rendimiento cercanas a la perfección en varios conjuntos de prueba. El equipo también comparó los resultados con otros métodos avanzados de segmentación de imagen y encontró un rendimiento igualmente sólido. Se emplearon herramientas visuales para resaltar las partes del tejido en las que los modelos se apoyaron, confirmando que se centraron en regiones con significado médico en lugar de patrones aleatorios.
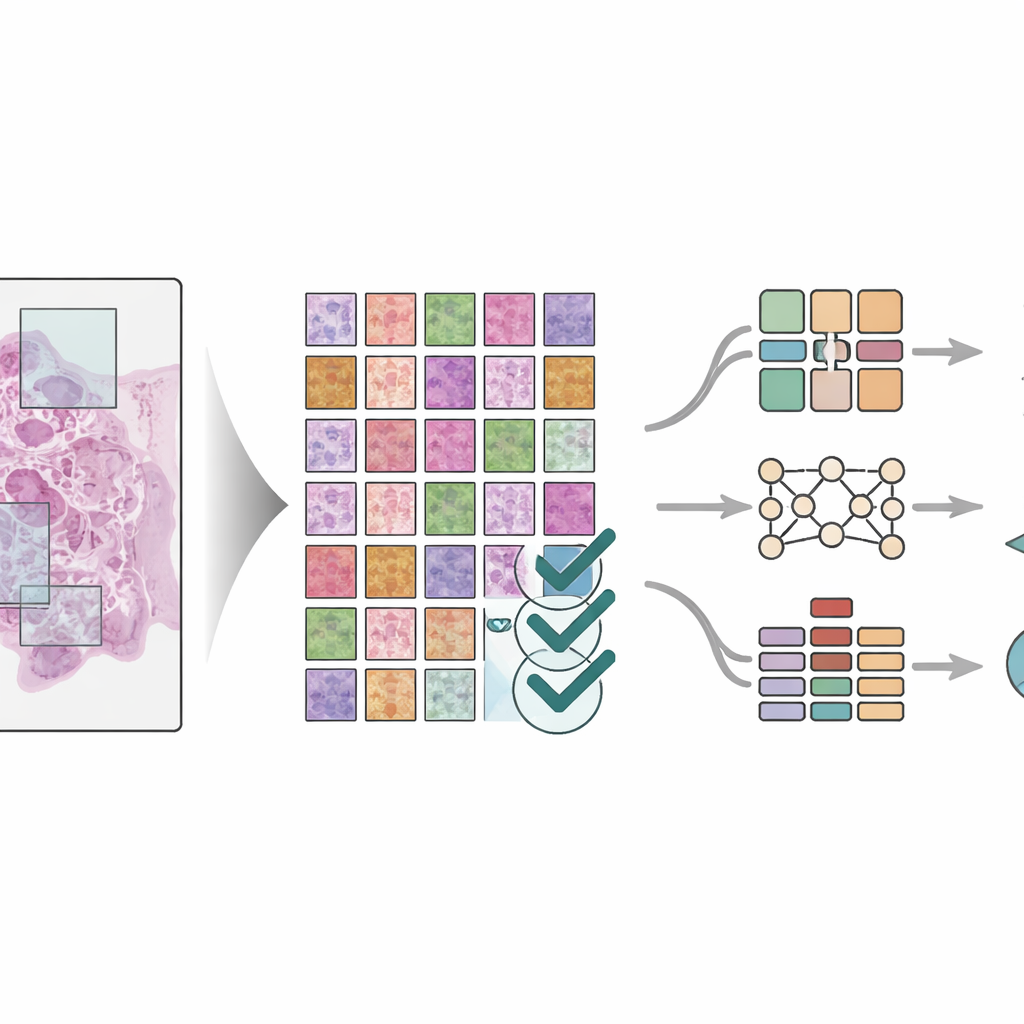
Qué significa esto para la atención del cáncer en el futuro
Para no especialistas, el mensaje clave es que este trabajo no introduce un nuevo tratamiento, sino una base poderosa para diagnósticos y pronósticos más inteligentes. Al compartir una biblioteca de imágenes grande, bien organizada y de acceso abierto vinculada a historiales clínicos detallados, los autores permiten a investigadores de todo el mundo desarrollar y comparar herramientas de inteligencia artificial sobre un terreno común y sólido. Tales herramientas podrían, en el futuro, ayudar a los patólogos a cartografiar el vecindario tumoral de forma más rápida y coherente, predecir qué pacientes tienen mayor riesgo y sugerir estrategias de tratamiento más personalizadas. Aunque los datos actuales capturan solo puntos temporales individuales en lugar de cambios a lo largo de meses o años, este recurso es un paso importante hacia el uso de la patología digital y la IA para comprender mejor y, en última instancia, tratar con mayor eficacia el cáncer colorrectal.
Cita: Wang, H., Li, H., Xue, J. et al. Large-Scale Histological Image Dataset with Metadata for Colorectal Cancer Microenvironment. Sci Data 13, 431 (2026). https://doi.org/10.1038/s41597-026-06675-9
Palabras clave: cáncer colorrectal, microambiente tumoral, patología digital, aprendizaje profundo, conjunto de datos de imágenes médicas