Clear Sky Science · es
Perfil transcriptómico exhaustivo de carcinomas medulares de tiroides esporádicos
Por qué importa este raro cáncer de tiroides
El carcinoma medular de tiroides es una forma poco frecuente de cáncer tiroideo que suele comportarse de forma más agresiva que la mayoría de los tumores de tiroides y con frecuencia afecta a las personas cuando la enfermedad ya está avanzada. Al ser poco común, los médicos e investigadores disponían de datos limitados para comprender por qué algunos tumores crecen y se diseminan más rápido que otros, o por qué algunos pacientes responden mejor al tratamiento. Este estudio aborda esa laguna mediante un análisis profundo y a escala genómica de la actividad de miles de genes en 72 tumores, creando uno de los retratos moleculares más completos hasta la fecha de esta enfermedad.
Mirando dentro de las células tumorales
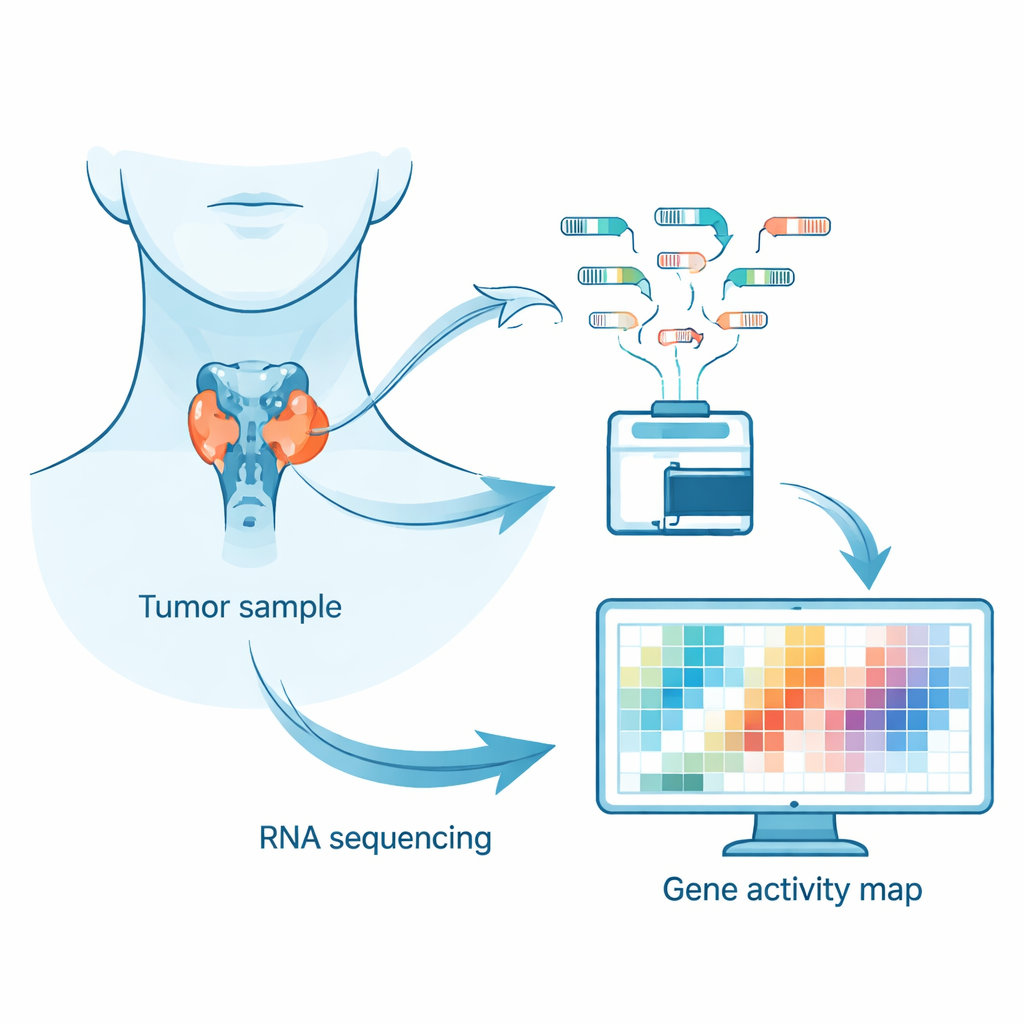
En lugar de centrarse solo en las mutaciones del ADN, los investigadores examinaron el “transcriptoma” del tumor: el conjunto completo de mensajeros de ARN producidos por los genes activos en las células cancerosas. Estos mensajeros de ARN actúan como informes de estado en tiempo real sobre lo que hace la célula. Al secuenciar ARN de muestras tumorales congeladas en fresco, el equipo pudo ver qué genes estaban más activados, cuáles estaban reprimidos y cómo se ensamblaban los mensajeros. Este enfoque ayuda a revelar patrones ocultos que las pruebas genéticas clásicas pueden pasar por alto, como cambios en la regulación génica o en la combinación de fragmentos de mensaje.
Quiénes se estudiaron y qué se midió
El equipo analizó tumores de 72 personas con carcinoma medular de tiroides esporádico (no familiar). Algo más de la mitad eran mujeres y la mediana de edad en el momento de la cirugía fue de 61 años. Aproximadamente el 58% de los tumores presentaban alteraciones en un gen llamado RET y alrededor del 24% tenían mutaciones en genes de la familia RAS, ambos impulsores conocidos de este cáncer. Los científicos comprobaron primero que las muestras tumorales eran de alta calidad y relativamente libres de tejido tiroideo normal o de contaminación por células inmunes, analizando marcadores clave como la calcitonina, que es alta en estos cánceres, y la tiroglobulina, propia de las células tiroideas normales y que se mantuvo baja. A continuación usaron herramientas computacionales bien establecidas para alinear las lecturas de ARN al genoma humano, cuantificar la actividad génica y buscar diferencias entre grupos clínicos y genéticos.
Actividad génica ligada al estadio y a la mutación
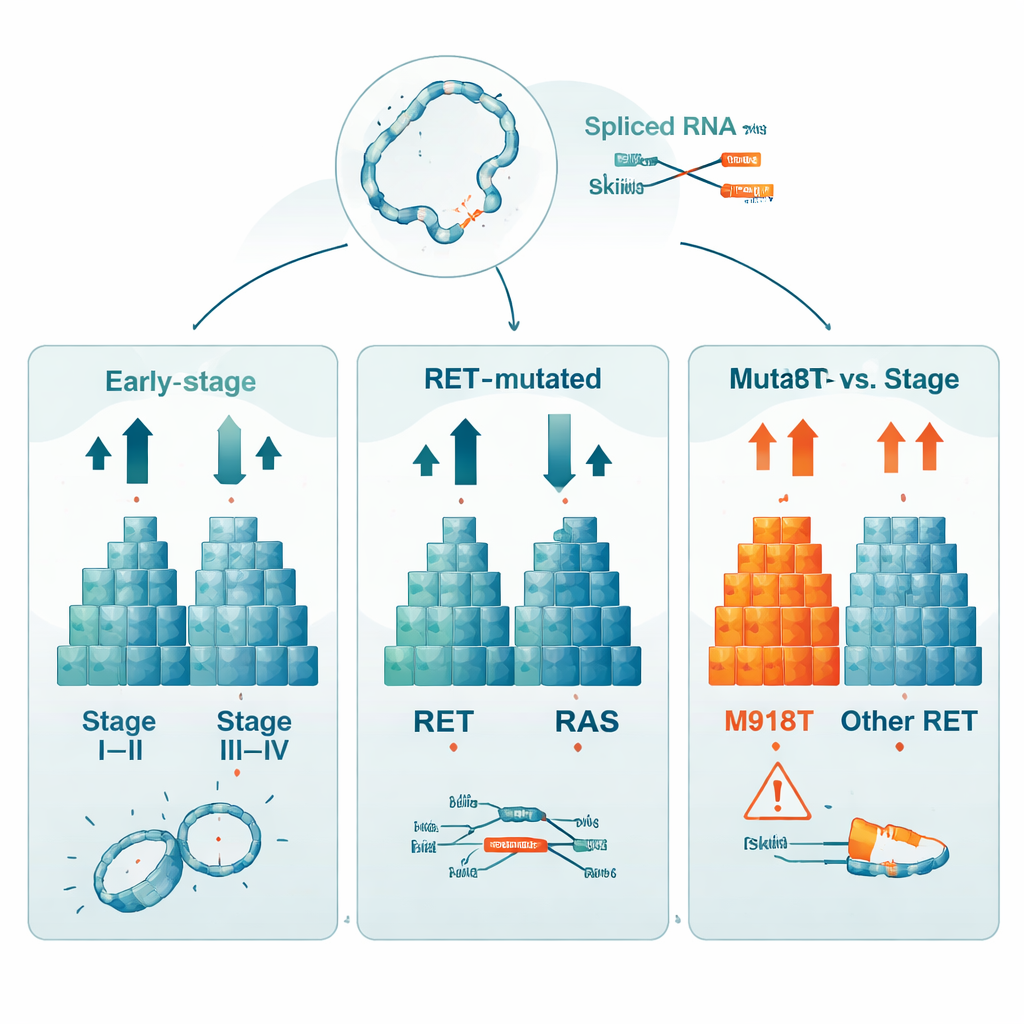
Al comparar tumores en estadios tempranos (I–II) con los más avanzados (III–IV), los investigadores hallaron 760 genes cuyos niveles de actividad diferían claramente entre ambos grupos. Esto indica que los patrones de expresión génica aportan pistas sólidas sobre el grado de avance del cáncer. También compararon tumores con mutaciones en RET o RAS con aquellos que no presentaban ninguna de las dos, descubriendo más de 1.200 genes con actividad alterada. Un análisis separado se centró en tumores con una alteración específica de RET, denominada M918T, que desde hace tiempo se asocia con peores resultados. En estos tumores, 529 genes mostraron actividad diferencial frente a cánceres con RET normal, y el propio gen RET se expresó a niveles más altos, lo que subraya hasta qué punto este cambio único remodela el comportamiento celular.
Reordenamientos ocultos y reconfiguración de los mensajeros
Más allá de los simples cambios de encendido/apagado de los genes, el estudio buscó formas más profundas de disrupción del ARN. El equipo detectó 59 transcritos de fusión génica distintos, donde fragmentos de genes diferentes se unen de forma anómala a nivel del ARN. La mayoría fueron raros, y la fusión más frecuente podría representar un artefacto técnico, pero el catálogo demuestra que estos reordenamientos pueden extraerse de manera sistemática a partir de estos datos. Los investigadores también cartografiaron miles de eventos de splicing alternativo, en los que segmentos de los mensajeros génicos se omiten, intercambian o retienen. Aunque cada comparación clínica (por estadio, tipo de mutación o estatus M918T) mostró conteos globales similares de estos cambios de splicing, los eventos específicos diferían en gran medida, lo que sugiere múltiples vías, en parte independientes, mediante las cuales las células tumorales reconfiguran sus mensajes génicos.
Qué ofrece este recurso a pacientes y científicos
Para los pacientes, este trabajo todavía no se traduce en un fármaco o prueba nueva inmediata, pero sienta bases esenciales. Al poner todos los datos procesados de secuenciación de ARN a disposición pública, los autores proporcionan un recurso rico que otros científicos pueden explorar para descubrir nuevos biomarcadores que predigan el pronóstico, refinar la clasificación de los carcinomas medulares de tiroides o detectar vulnerabilidades que puedan ser atacadas por futuras terapias, incluida la nueva generación de inhibidores selectivos de RET. En términos sencillos, este estudio ofrece un “mapa de actividad” detallado de los genes tumorales en numerosos casos reales, dando a los investigadores las herramientas necesarias para entender mejor por qué este cáncer raro se comporta tan diferente de una persona a otra y cómo la atención podría, algún día, personalizarse con mayor precisión.
Cita: Palumbo, D., Melone, V., Palo, L. et al. Comprehensive Transcriptome Profiling of Sporadic Medullary Thyroid Carcinomas. Sci Data 13, 234 (2026). https://doi.org/10.1038/s41597-026-06550-7
Palabras clave: carcinoma medular de tiroides, genómica del cáncer, secuenciación de ARN, mutación RET, oncología personalizada