Clear Sky Science · es
El metabolismo de la vitamina B2 promueve la estabilidad de FSP1 para prevenir la ferroptosis
Cómo una vitamina común ayuda a las células a decidir entre la vida y la muerte
Nuestras células caminan constantemente por la cuerda floja entre la supervivencia y la autodestrucción. Una forma dramática de muerte celular, denominada ferroptosis, ha llamado la atención porque puede eliminar selectivamente células cancerosas que resisten otros tratamientos. Este estudio revela que un nutriente cotidiano —la vitamina B2, o riboflavina— inclina discretamente la balanza al estabilizar una proteína protectora clave. Comprender esta conexión oculta entre la dieta, el metabolismo celular y la muerte de células cancerosas podría ayudar a los investigadores a diseñar terapias más inteligentes y a afinar futuras recomendaciones nutricionales.
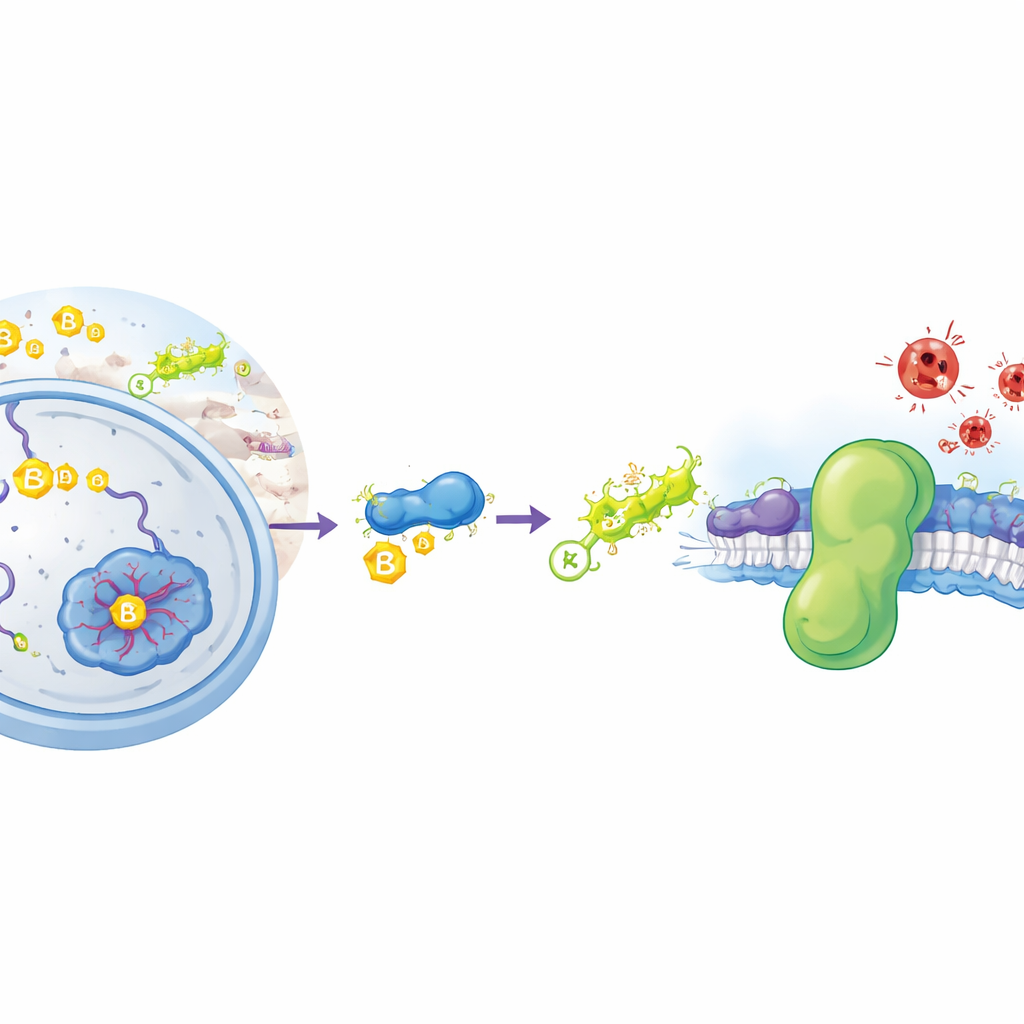
Un tipo especial de oxidación dentro de las células
La ferroptosis es un tipo de muerte celular impulsada por un proceso químico parecido a la oxidación de metales: la oxidación descontrolada de los lípidos en las membranas celulares. Cuando estas grasas se degradan, las membranas pierden integridad y las células estallan. Nuestras células normalmente despliegan varias defensas para evitar que esto ocurra. Un escudo importante es una enzima llamada GPX4, que utiliza una pequeña molécula, el glutatión, para desintoxicar los peróxidos lipídicos dañinos. Un segundo escudo paralelo es una proteína llamada FSP1, que se localiza en las membranas celulares y usa pequeñas moléculas lipídicas para interceptar radicales destructivos antes de que se propaguen. Las células cancerosas con frecuencia aumentan la expresión de FSP1 para evitar la ferroptosis, lo que convierte a esta proteína en un objetivo principal para nuevos fármacos anticancerígenos. Sin embargo, hasta ahora los científicos no sabían cómo controlan las células la cantidad de FSP1 que se produce ni cuánto tiempo dura.
Construyendo un “indicador de combustible” celular para un bloqueador de la muerte
Para descubrir los gestores ocultos de FSP1, los investigadores primero diseñaron células humanas de cáncer óseo que llevaban un informe fluorescente. Etiquetaron la proteína FSP1 natural con una señal verde y la vincularon a una señal azul que informa de cuánto mensaje de FSP1 produce la célula. Este ingenioso diseño les permitió distinguir cambios en la actividad génica (azul) de cambios en la estabilidad de la proteína (verde). Con este sistema bicolor, usaron CRISPR–Cas9 para interrumpir sistemáticamente casi todos los genes del genoma y luego separaron las células con niveles altos o bajos de FSP1. Al comparar qué ARN guía estaban enriquecidos en cada grupo, cartografiaron cientos de genes que aumentan o disminuyen FSP1, actuando a nivel del control génico o del recambio proteico.
El trabajo oculto de la vitamina B2: crear un asa estabilizadora
Entre los descubrimientos más llamativos figuraban dos enzimas, la riboflavina quinasa (RFK) y la sintasa de FAD (FLAD1), que convierten la vitamina B2 en un cofactor llamado FAD. FSP1 es una flavoproteína que normalmente une FAD con firmeza para llevar a cabo sus reacciones químicas. Cuando se eliminaron RFK o FLAD1, o cuando las células se cultivaron en medio deficiente en vitamina B2, los niveles de proteína FSP1 cayeron drásticamente aunque la actividad de su gen se mantuviera similar. El equipo mostró que esta pérdida hacía a las células mucho más vulnerables a la ferroptosis cuando GPX4 estaba bloqueada. Es importante señalar que la vitamina B2 en sí no actuó como un antioxidante clásico: en una prueba sensible in vitro no logró detener la oxidación lipídica, a diferencia de la vitamina E. En cambio, añadir FAD (y en parte su precursor FMN) a las células deficientes restauró tanto los niveles de FSP1 como la resistencia a la muerte por ferroptosis, mientras que un exceso de vitamina B2 por sí sola no ayudó si faltaban las enzimas procesadoras.
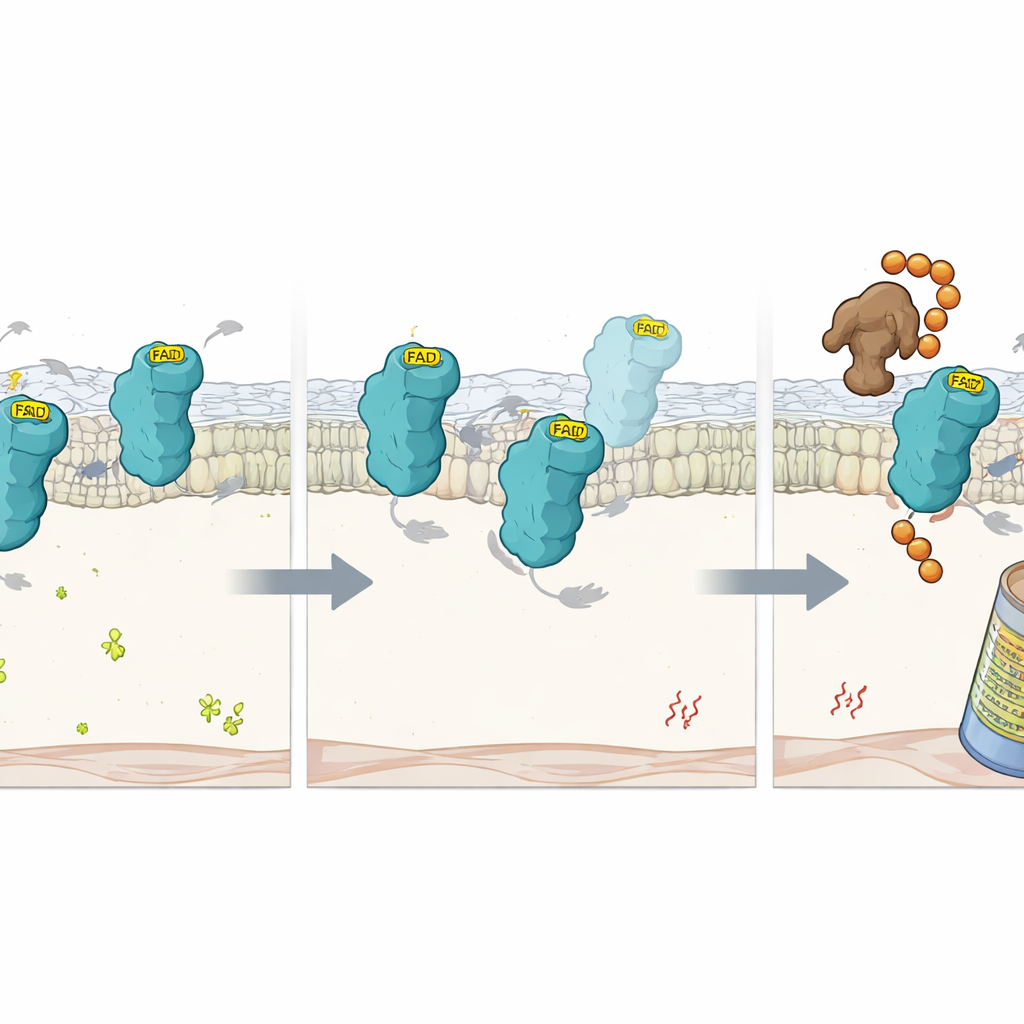
Qué ocurre cuando falta el cofactor
Para profundizar, los científicos estudiaron mutaciones precisas en FSP1 que incapacitan su capacidad de retener FAD. Estas proteínas mutantes todavía se plegaban en formas mayoritariamente normales pero perdían su FAD y su actividad catalítica. Dentro de las células, se degradaban mucho más rápido que la FSP1 normal, a menos que se bloquease el proteasoma —la maquinaria celular de trituración de proteínas—. Esto sugirió que la unión al FAD actúa como un asa estabilizadora que protege a FSP1 de ser etiquetada como defectuosa. Usando otra pantalla CRISPR enfocada en condiciones de bajo FAD, el equipo identificó una ligasa E3 llamada RNF8 como un factor clave que reconoce la FSP1 sin FAD. Cuando se eliminó RFK, RNF8 añadía cadenas de ubiquitina a la proteína vacía, marcándola para su destrucción por el proteasoma. Eliminar RNF8 ralentizó el recambio de FSP1 en células pobres en FAD, aunque no pudo restaurar su función protectora perdida sin el cofactor.
De la circuitería molecular a ideas terapéuticas contra el cáncer
Al juntar estas piezas, los autores proponen un modelo simple pero poderoso. La vitamina B2, después de convertirse en FAD por RFK y FLAD1, se une a FSP1 y es esencial tanto para su actividad bioquímica como para su longevidad. Cuando el suministro de vitamina B2 o su procesamiento falla, la FSP1 recién sintetizada no puede asegurar FAD, es señalada por RNF8 y se desmonta rápidamente por el proteasoma, dejando a las células más expuestas al daño por ferroptosis. Los datos sobre cáncer sugieren que los tumores con mayor expresión de RFK son más resistentes a los fármacos inductores de ferroptosis, lo que subraya la relevancia real de esta vía. Para los no especialistas, el mensaje clave es que una vitamina familiar hace mucho más que actuar como un simple antioxidante: ayuda a decidir si una potente proteína anti-muerte permanece en guardia o es barrida. Al ajustar el metabolismo de la vitamina B2 o la estabilidad de FSP1, los tratamientos futuros podrían aprovechar mejor la ferroptosis para eliminar células cancerosas preservando el tejido sano.
Cita: Deol, K.K., Harris, C.A., Tomlinson, S.J. et al. Vitamin B2 metabolism promotes FSP1 stability to prevent ferroptosis. Nat Struct Mol Biol 33, 525–536 (2026). https://doi.org/10.1038/s41594-026-01759-x
Palabras clave: ferroptosis, vitamina B2, FSP1, muerte de células cancerosas, metabolismo celular