Clear Sky Science · es
Cartografía, origen y papel de los quimeras elemento transponible–gen en la mejora de la plasticidad del transcriptoma
Pasajeros ocultos en nuestro ADN
Gran parte de nuestro ADN está compuesto por estafadores virales ancestrales llamados elementos transponibles: fragmentos de código genético que en su día se movían por los genomas como parásitos que hacen autoestop. Este estudio muestra que esos viejos fragmentos virales no son mero material basura silencioso: pueden empalmarse con nuestros propios genes para crear mensajes híbridos, ayudar a las células a adaptarse a condiciones cambiantes y, a veces, alimentar enfermedades. Al cartografiar estos híbridos durante el desarrollo, el envejecimiento y el cáncer, los autores revelan una manera sorprendente en la que el ADN viral sigue moldeando la biología humana hoy.
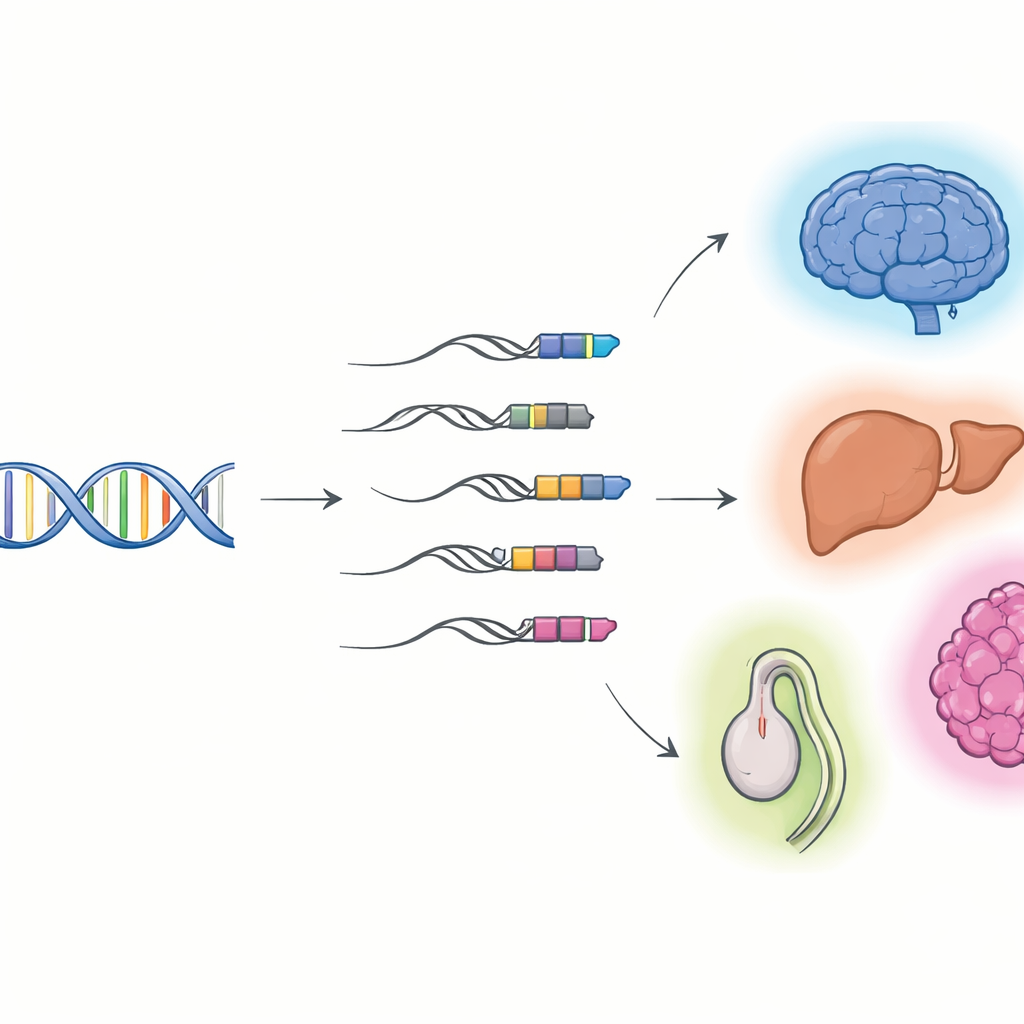
Cuando el ADN viral se convierte en parte de nuestros genes
Los investigadores se centraron en los “quimeras TE–gen”: moléculas de ARN que comienzan en un elemento transponible y continúan en un gen huésped. Usando secuenciación de lecturas largas, que puede capturar moléculas de ARN enteras de extremo a extremo, combinada con la secuenciación convencional de lecturas cortas, construyeron catálogos detallados de estos híbridos en células y órganos de ratón y humano. Encontraron miles de transcritos quiméricos previamente desconocidos, la mayoría de ellos ARN no codificantes más que planos para proteínas. Muchos se inician en una clase de restos virales llamados repeticiones terminales largas (LTR), que a menudo se sitúan delante de los genes y pueden actuar como conmutadores alternativos de encendido/apagado. Tejidos y órganos distintos usan distintos conjuntos de estos quimeras, con actividad especialmente rica en el cerebro, el hígado y el testículo, y su uso cambia a medida que los tejidos se desarrollan de etapas fetales a adultas.
Quimeras en el envejecimiento y el cáncer
Para ver cómo se comportan estos híbridos viral–huésped en poblaciones reales, el equipo examinó grandes conjuntos de datos humanos que abarcan docenas de tejidos de cientos de personas, así como muestras tumorales. Identificaron varios cientos de quimeras de alta confianza que se repiten entre individuos. Su expresión varía no solo entre órganos, sino también con la edad: en tejidos como la sangre y el cerebro, algunas quimeras impulsadas por LTR disminuyen en adultos mayores, mientras que en ciertos tejidos periféricos aumentan. En muchos tipos de cáncer, estos híbridos basados en LTR están generalmente sobreactivados en los tumores comparados con el tejido normal circundante, y los pacientes cuyos tumores expresan más de ellos tienden a tener peor pronóstico. En conjuntos de datos de personas resistentes a quimioterapia o inmunoterapia, los genes afectados por nuevos exones impulsados por LTR frecuentemente participan en vías relacionadas con el modo de acción de esos fármacos, lo que sugiere que los quimeras TE pueden ayudar a los tumores a reconfigurarse bajo la presión del tratamiento.
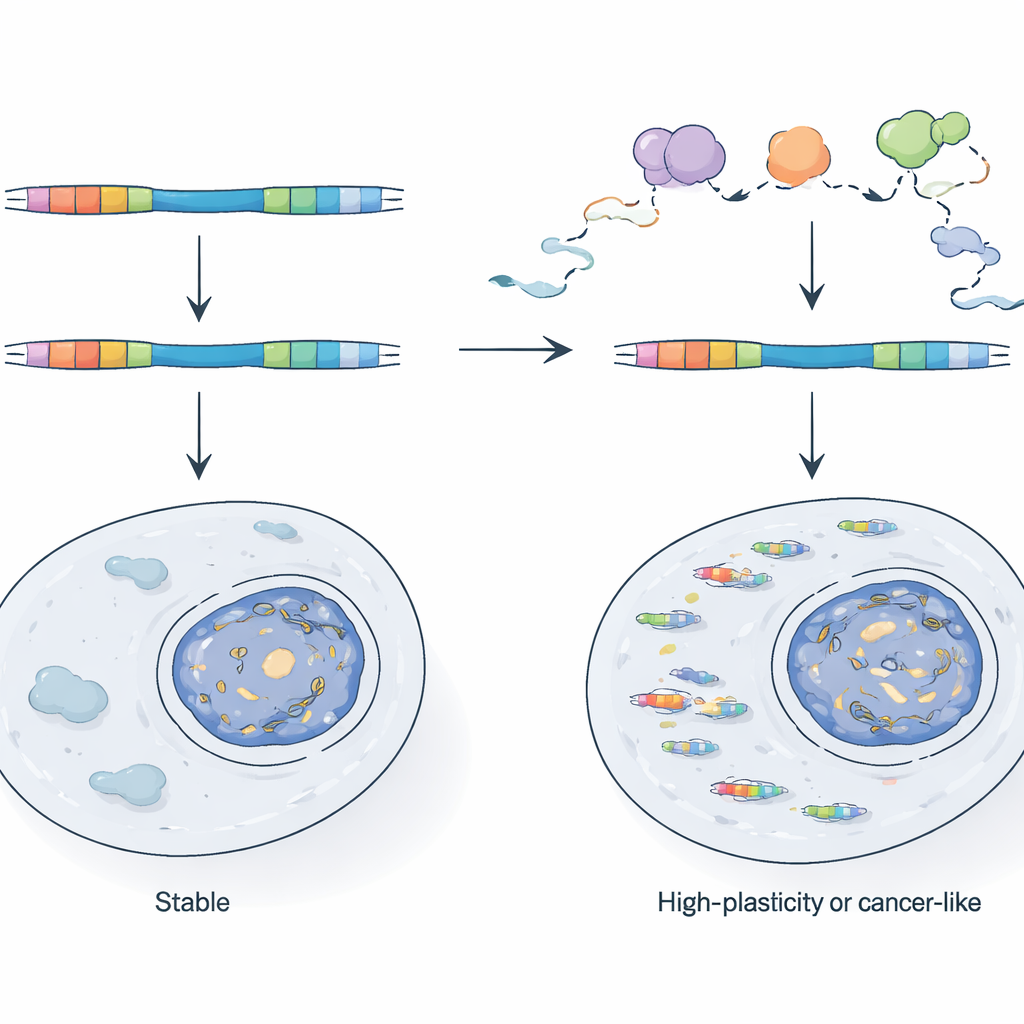
Cómo las células controlan los híbridos virales
Dada su potencia, ¿por qué los quimeras TE no desbordan las células normales? Los autores muestran que las células dependen de un sistema de control de calidad del ARN, centrado en el complejo nuclear exosoma, para patrullar y destruir muchos de estos transcritos mientras se producen. Cuando inutilizan genéticamente un componente clave del exosoma en células madre de ratón, los promotores impulsados por LTR se vuelven mucho más activos y los ARN quiméricos se disparan. Al comparar ARN recién sintetizado con ARN estable, muestran que algunos LTRs están normalmente controlados porque sus transcritos se degradan rápidamente, mientras que otros se regulan a nivel de la frecuencia de inicio de la transcripción. Estos LTR activos tienden a ubicarse en regiones del genoma que ya son accesibles y con frecuencia transcritas, lo que indica que el mero hecho de estar cerca de un gen activo o de un transcrito en antisentido puede ayudar a un fragmento viral a escapar del silenciamiento epigenético tradicional.
Splicing, plasticidad de las células madre y un “interruptor maestro” viral
La historia se vuelve más intrincada cuando se perturba la maquinaria de empalme de la célula. Los autores reducen la expresión de varios factores centrales del empalme o inhiben químicamente el espliceosoma y observan un resultado común al de la pérdida del exosoma: un fuerte aumento en los quimeras impulsados por LTR y en genes cortos con pocos intrones. Entre los beneficiados está MERVL, un retrovirus endógeno activo en embriones de ratón en etapas muy tempranas. Cuando se regulan al alza la secuencia interna de MERVL y los factores de transcripción aguas abajo, las células madre se desplazan hacia un estado más parecido a la totipotencia, semejante a las células embrionarias tempranas capaces de formar todos los tejidos. Por el contrario, degradar el ARN de MERVL con oligonucleótidos antisentido atenúa este cambio y reduce la actividad de los promotores LTR, lo que indica que MERVL actúa como un interruptor maestro que puede desencadenar una red más amplia de quimeras TE y de plasticidad del estado celular.
Innovación viral a lo largo de la evolución
Al analizar muchos genomas de mamíferos, el equipo traza cuándo distintas familias de TE empezaron a donar exones a genes huéspedes. En humanos y ratones, las familias de LTR relativamente jóvenes son especialmente propensas a formar quimeras en la orientación “sentido” que puede leerse como parte de los transcritos del huésped. Este patrón sugiere que nuevas oleadas de inserciones de TE han aportado repetidamente materia prima a las redes reguladoras génicas a lo largo del tiempo evolutivo. En lugar de ser puramente dañinas, estas inserciones pueden ser puestas a prueba por la maquinaria de transcripción y degradación celular: la mayoría se silencian o degradan, pero una minoría se encuentra en el lugar y contexto adecuados para ser cooptada como elementos regulatorios útiles o nuevos inicios génicos.
Por qué importan estos restos virales
Para un público no especializado, este trabajo muestra que una porción amplia y antaño descartada de nuestro genoma está activamente moldeando cómo se leen los genes, cómo las células cambian de identidad y cómo progresan las enfermedades. Las secuencias virales ancestrales pueden convertirse en “puertas delanteras” alternativas de los genes, produciendo ARN híbridos que normalmente son controlados por los sistemas de limpieza celular. Cuando ese control o el empalme normal fallan, estos híbridos pueden dispararse, empujando a las células madre hacia estados más flexibles o ayudando a los tumores a adaptarse y resistir la terapia. Durante millones de años, la evolución ha jugueteado repetidamente con estos fragmentos virales, convirtiendo muchos de parásitos genómicos en componentes de la complejidad reguladora, y dejándonos un transcriptoma mucho más plástico y dinámico de lo que una simple lista de genes sugeriría.
Cita: Cheon, Y., Alvstad, E.G., Torre, D. et al. Transposable element–gene chimera cartography, origination and role in enhancing transcriptome plasticity. Nat Struct Mol Biol 33, 448–463 (2026). https://doi.org/10.1038/s41594-026-01757-z
Palabras clave: elementos transponibles, transcritos quiméricos, vigilancia del ARN, plasticidad de las células madre, evolución del cáncer