Clear Sky Science · es
Adaptación al estrés de la importación de proteínas mitocondriales mediante la degradación de DNAJC15 mediada por OMA1
Cómo se las arreglan nuestras células cuando sus centrales energéticas están bajo estrés
Cada célula de su cuerpo depende de unas diminutas estructuras llamadas mitocondrias para convertir los alimentos en energía utilizable. Como fábricas en miniatura, las mitocondrias importan continuamente piezas nuevas —proteínas recién sintetizadas en otras partes de la célula— para mantener su maquinaria en funcionamiento. Este artículo revela cómo, cuando las mitocondrias están estresadas o dañadas, la célula reduce deliberadamente esta vía de importación de proteínas. Al hacerlo, se protegen de la sobrecarga y coordinan una respuesta de estrés más amplia que involucra no solo a las mitocondrias, sino también a otro compartimento clave: el retículo endoplásmico.
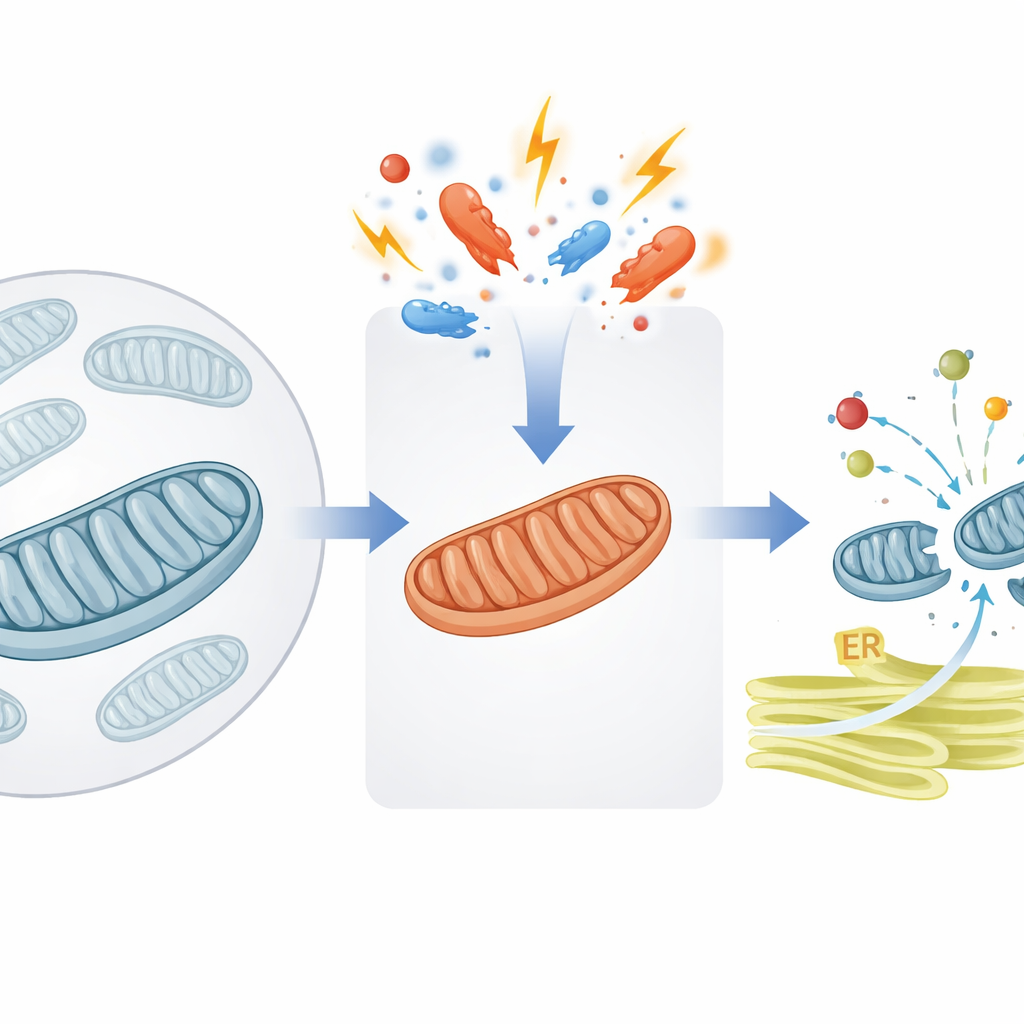
Una válvula de seguridad para el tráfico de proteínas mitocondriales
Las mitocondrias dependen de miles de proteínas que se sintetizan primero en el compartimento principal de la célula y luego se envían a ellas. Los autores se centran en una puerta de entrada crucial en la membrana interna mitocondrial, asistida por una proteína auxiliar llamada DNAJC15. En condiciones normales, DNAJC15 ayuda a «tirar» los paquetes de proteínas a través del canal de importación hacia el interior mitocondrial, donde muchas de ellas se integran en la maquinaria productora de energía conocida como fosforilación oxidativa (OXPHOS). El estudio muestra que cuando las mitocondrias experimentan estrés —como una producción de energía deficiente o cambios en las propiedades de la membrana— la célula activa un interruptor molecular que modula cuánto está dispuesta la organela a importar proteínas.
OMA1: la tijera activada por el estrés
En el centro de este interruptor se encuentra una enzima sensible al estrés llamada OMA1, ubicada en la membrana interna mitocondrial. Cuando las mitocondrias encuentran problemas, OMA1 se activa y corta a DNAJC15 en una posición específica cerca de su extremo N-terminal. Este corte genera una versión más corta de DNAJC15 que es rápidamente digerida por otro complejo enzimático mitocondrial llamado proteasa m-AAA. Como resultado, se pierde la forma completa y competente para la importación de DNAJC15. Los autores muestran que las células que carecen de DNAJC15, o en las que DNAJC15 se destruye rápidamente tras la activación de OMA1, tienen una capacidad reducida para incorporar proteínas nuevas en las mitocondrias, especialmente aquellas necesarias para construir y mantener los complejos de la OXPHOS.
Ralentizar el ensamblaje energético para ajustar la salud mitocondrial
Mediante mediciones proteómicas a gran escala y ensayos de importación, el equipo encontró que DNAJC15 es particularmente importante para suministrar al interior mitocondrial proteínas implicadas en la expresión génica y en el ensamblaje de la cadena respiratoria. Cuando falta DNAJC15, estas proteínas se acumulan más lentamente dentro de las mitocondrias y la capacidad de los orgánulos para consumir oxígeno y sostener la producción de energía —medida en mitocondrias aisladas— disminuye, especialmente en el complejo I de la cadena respiratoria. Otro componente del canal de importación, TIMM17A, funciona mano a mano con DNAJC15: la pérdida de ambos provoca defectos especialmente marcados en los niveles de proteínas ribosomales mitocondriales y componentes de la OXPHOS. En conjunto, estos hallazgos sugieren que la destrucción de DNAJC15 mediada por OMA1 es una manera de frenar temporalmente la construcción de nueva maquinaria energética hasta que la organela se recupere.
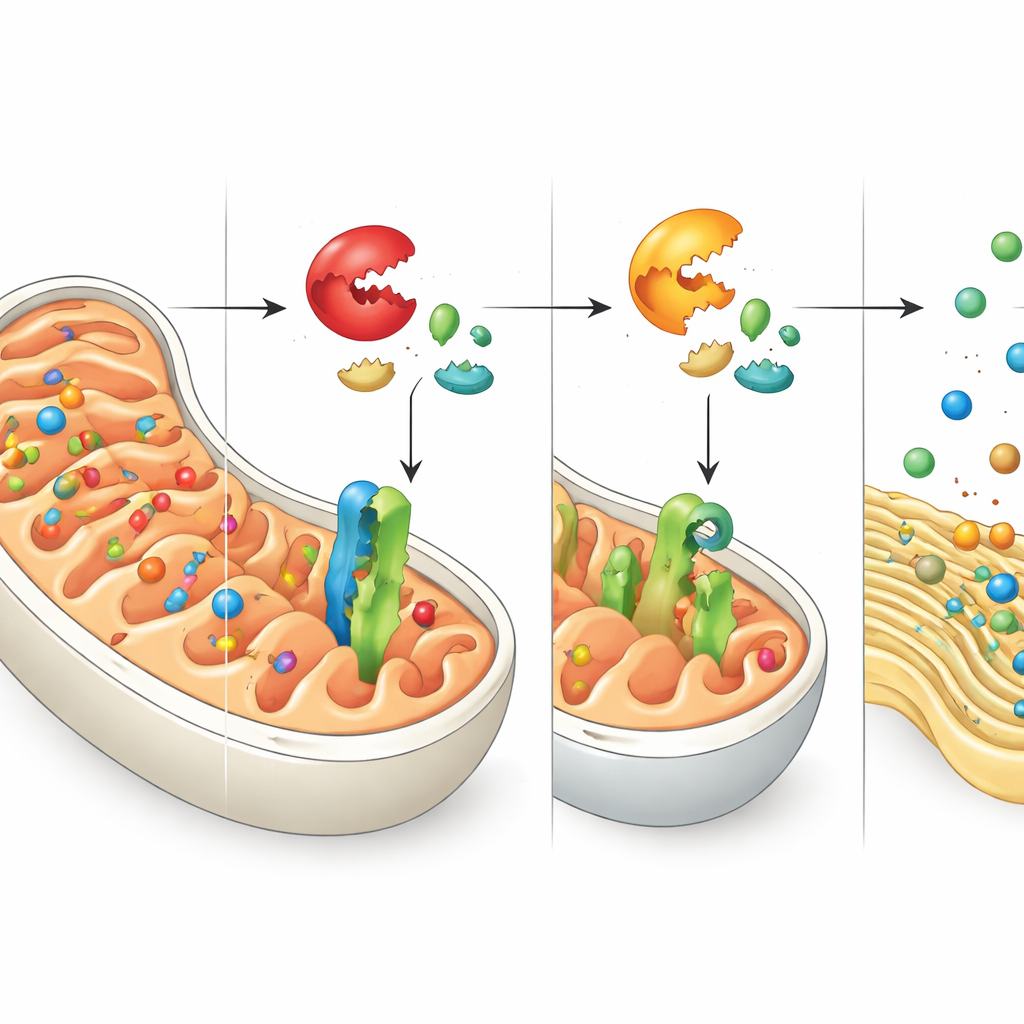
Paquetes mal dirigidos y un llamado de auxilio desde el RE
Apagar DNAJC15 no impide que la célula sintetice proteínas mitocondriales: principalmente evita que lleguen a su destino previsto. Los autores rastrearon adónde van estas proteínas varadas y encontraron que muchas terminan en el retículo endoplásmico (RE), una red de membranas que normalmente ayuda a plegar y procesar otros conjuntos de proteínas. Estas proteínas mitocondriales desviadas se insertan en las membranas del RE, alterando el equilibrio de control de calidad del propio RE. En respuesta, la célula activa un programa protector conocido como la respuesta a proteínas desplegadas, específicamente a través de una rama controlada por el sensor ATF6. Esta respuesta aumenta la capacidad del RE para manejar proteínas mal plegadas o mal localizadas, revelando una estrecha coordinación entre los sistemas de estrés mitocondrial y del RE.
Una desaceleración coordinada para proteger la célula
En conjunto, el estudio dibuja la imagen de un sistema de frenos incorporado para la biogénesis mitocondrial. Cuando las mitocondrias están estresadas, OMA1 recorta e indirectamente destruye DNAJC15, reduciendo el flujo de proteínas nuevas relacionadas con la energía hacia orgánulos comprometidos. Algunas de estas proteínas son temporalmente retenidas en el RE, que monta su propia respuesta protectora. Al acoplar la capacidad de importación mitocondrial al estado de salud del orgánulo y al utilizar el RE como sitio de almacenamiento temporal para el excedente de proteínas, las células pueden evitar la obstrucción de mitocondrias dañadas y ganar tiempo para repararlas o eliminarlas por completo. Para un observador profano, este trabajo muestra lo profundamente integrados que están nuestros sistemas de control de calidad celular: incluso las fallas más pequeñas en un compartimento son detectadas y compensadas por otros para mantener en marcha la producción de energía —y la vida misma—.
Cita: Kroczek, L., Nolte, H., Lasarzewski, Y. et al. Stress adaptation of mitochondrial protein import by OMA1-mediated degradation of DNAJC15. Nat Struct Mol Biol 33, 499–511 (2026). https://doi.org/10.1038/s41594-026-01756-0
Palabras clave: estrés mitocondrial, importación de proteínas, control de calidad celular, fosforilación oxidativa, retículo endoplásmico