Clear Sky Science · es
Estructura y mecanismo del retrón antifago Eco2
Cómo las bacterias usan un “autodestrucción” incorporado para combatir virus
Los virus que infectan bacterias, llamados fagos, están en todas partes —desde los océanos hasta nuestro propio intestino. Este estudio revela cómo un diminuto engranaje genético dentro de algunas bacterias, conocido como el retrón Eco2, les ayuda a sobrevivir al ataque de fagos. Al desvelar la estructura 3D de Eco2 y cómo se activa, el trabajo explica un nuevo tipo de defensa de emergencia: cuando se detecta la infección, la célula apaga deliberadamente su propia producción de proteínas para impedir que el virus se propague.
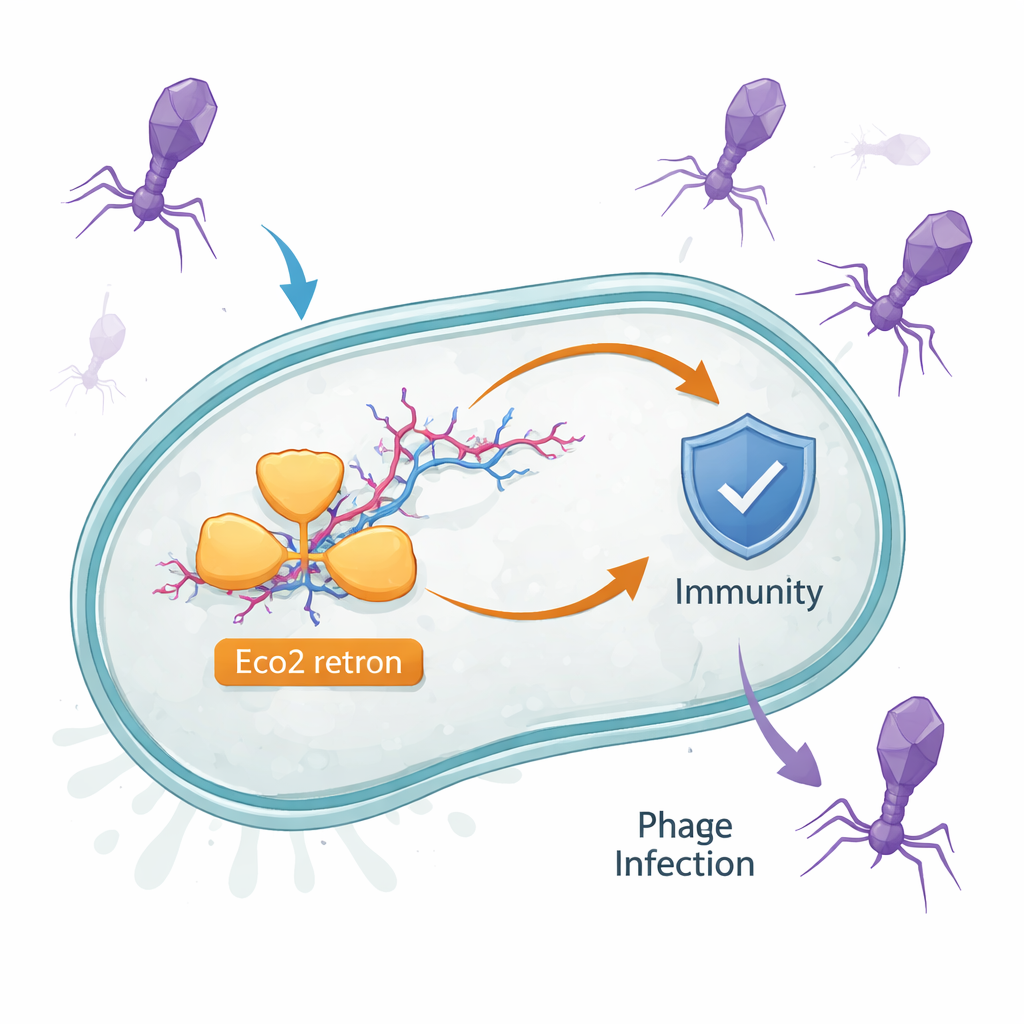
Un artilugio oculto de ADN–ARN en las células bacterianas
Las bacterias poseen muchos pequeños sistemas de defensa que solo entran en acción durante la infección. Eco2 es uno de ellos. Vive en Escherichia coli y consta de una única proteína que tanto copia ARN en ADN como puede cortar ácidos nucleicos. Esta proteína trabaja junto con una extraña molécula llamada msDNA, un híbrido de ARN y ADN monocatenario que se bifurca como una pequeña ramita. Pistas anteriores sugerían que retrones como Eco2 defienden frente a fagos, pero no se entendía cómo una sola proteína y su compañera msDNA detectan la infección y responden.
Protección amplia frente a muchos virus
Los investigadores preguntaron primero qué tan bien protege Eco2 a las bacterias frente a una amplia gama de fagos. Al desafiar células portadoras de Eco2 con una colección grande y diversa de virus, encontraron que Eco2 bloquea muchas familias de fagos, pero no todas. Cuando algunos fagos lograron escapar, sus genomas mostraron mutaciones en genes que codifican enzimas virales cortadoras de ADN, especialmente una llamada DenB. Este patrón sugiere que Eco2 se activa por nucleasas virales específicas: cuando esas enzimas quedan inactivadas por mutación, el virus puede eludir la defensa.
Un escudo molecular de tres brazos
Para ver cómo está construido Eco2, el equipo usó microscopía crioelectrónica para visualizar el complejo con detalle cercano al atómico. Eco2 no actúa solo: tres copias de la proteína Eco2 se ensamblan en una estructura de tres brazos, semejante a una estrella arrojadiza. La msDNA ramificada se enhebra a través y alrededor de estas tres proteínas, uniéndolas. Al hacerlo, la msDNA forma una intersección triple en el centro y “enjaula” físicamente la parte nucleasa de Eco2, bloqueando su sitio de corte. Experimentos de intercambio hidrógeno–deuterio, que rastrean qué regiones son flexibles, mostraron que la unión de msDNA endurece y estabiliza el complejo. En este estado de reposo, Eco2 queda efectivamente bloqueado en la posición APAGADA.
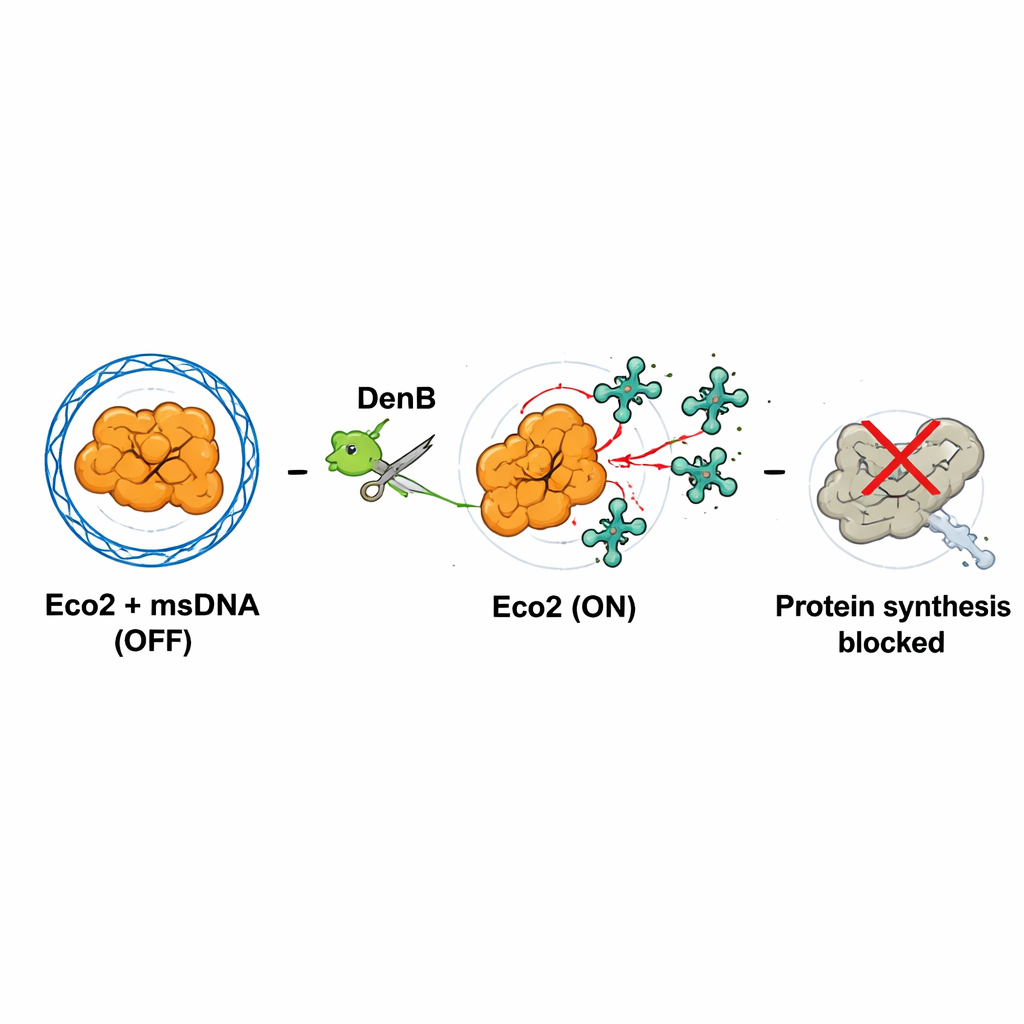
El ataque viral activa el sistema
La clave para la activación es la destrucción de la msDNA. La enzima viral DenB, que normalmente ayuda al fago a procesar ADN, también corta dentro de la msDNA que encierra a Eco2. Los autores imitaron este proceso usando tanto DenB purificada como una enzima estándar cortadora de ADN y observaron que, una vez que la msDNA se corta, el sitio nucleasa de Eco2 queda expuesto y se reorganiza hacia una configuración activa. Estructuras de alta resolución de este “estado ENCENDIDO” mostraron que un aminoácido crítico en el bolsillo nucleasa se desplaza a una posición donde puede coordinar correctamente un ión magnesio, esencial para cortar ARN. Así, la actividad nucleasa viral, destinada a remodelar el ADN del huésped, sin querer saca el pasador de seguridad de Eco2.
Cortar los propios ARNt de la célula para detener el virus
¿Qué corta Eco2 activado? Usando sistemas celulares libres, marcaje radiactivo y secuenciación de ARN durante infecciones reales, el equipo descubrió que Eco2 principalmemente hace nicks en los ARN de transferencia (ARNt), las moléculas adaptadoras que aportan aminoácidos al ribosoma. Eco2 recorta estos ARNt cerca de sus extremos en cola, especialmente en sitios ricos en la base citosina. Cuando muchos ARNt quedan dañados, los ribosomas de la célula ya no pueden sintetizar proteínas con eficiencia. En presencia de DenB y Eco2 activo, la producción de proteína fluorescente verde cayó drásticamente, y tanto los ARN bacterianos como los virales fueron degradados. Este apagado probablemente representa una “infección abortada”: la célula bacteriana infectada sacrifica su propio crecimiento para que el virus no pueda replicarse y propagarse con éxito.
Por qué importa esto más allá de las bacterias
Este trabajo muestra cómo un retrón mínimo puede detectar una enzima viral, pasar de una forma inactiva a una activa y luego paralizar la síntesis proteica al dirigirse a los ARNt. Para un público general, la idea clave es que las bacterias a veces vencen a los virus no mediante objetivos de precisión, sino desenchufando su propia maquinaria celular en el momento justo. Más allá de profundizar en nuestra comprensión de la inmunidad microbiana, las estructuras detalladas de Eco2 y su andamiaje de msDNA ofrecen un plano para ingenieros que esperan reutilizar retrones como herramientas para la edición del genoma y la biología sintética.
Cita: Jasnauskaitė, M., Juozapaitis, J., Liegutė, T. et al. Structure and mechanism of antiphage retron Eco2. Nat Struct Mol Biol 33, 330–340 (2026). https://doi.org/10.1038/s41594-026-01754-2
Palabras clave: inmunidad frente a bacteriófagos, retrón Eco2, defensa antiviral bacteriana, corte de ARNt, msDNA