Clear Sky Science · es
Estructura y función del supercomplejo sensor de aminoácidos SEAC–EGOC en levadura
Cómo deciden las células cuándo crecer
Cada célula debe decidir constantemente si puede permitirse crecer o si debe conservar recursos. Esa decisión depende en gran medida de los aminoácidos, los bloques constructores de las proteínas y una fuente clave de nitrógeno. Este artículo revela, con notable detalle estructural, cómo las células de levadura detectan la disponibilidad de aminoácidos a través de un ensamblaje molecular gigantesco y usan esa información para activar o desactivar un controlador principal del crecimiento, llamado TORC1. Dado que la misma circuitería está conservada en células humanas y se vincula al cáncer y al metabolismo, los hallazgos en levadura ofrecen una ventana sobre cómo nuestras propias células juzgan cuándo las condiciones son adecuadas para el crecimiento.
Un centro intrincado en el centro de reciclaje celular
En la levadura, un complejo central de toma de decisiones llamado SEAC se sitúa en la membrana de la vacuola, un orgánulo que actúa como centro de reciclaje de la célula. Allí se encuentra con otro complejo, EGOC, que transmite información sobre los niveles de aminoácidos. Juntos envían señales a TORC1, el interruptor principal del crecimiento. SEAC tiene dos mitades funcionales: SEACIT, que puede apagar TORC1, y SEACAT, que se había pensado durante mucho tiempo que mantenía a SEACIT bajo control. Los autores utilizaron crioelectrón microscopia de alta resolución para visualizar el SEAC completo unido a EGOC, capturando una instantánea de este centro molecular exactamente donde se produce la señalización, en la superficie de la vacuola. 
Viendo de cerca la arquitectura molecular
La estructura revela a SEAC como un gran núcleo compuesto por subunidades de SEACAT, del que se extienden dos “alas” flexibles de SEACIT. Cada ala puede enlazar un complejo EGOC, lo que significa que un único SEAC puede recibir dos entradas de señal simultáneamente. De forma llamativa, EGOC se une solo a las alas y no al núcleo, y la forma general de SEAC apenas cambia cuando EGOC está presente. Esto muestra que SEACAT no bloquea físicamente el sitio activo de SEACIT ni impide la unión de EGOC. La orientación del complejo en la membrana de la vacuola también coloca al núcleo de SEAC frente al citoplasma, donde puede interactuar con reguladores adicionales, mientras que las alas quedan cerca de la membrana, idealmente situadas para contactar con EGOC y otros socios anclados a la membrana.
Cómo SEAC selecciona la señal adecuada
Los autores se centraron en los contactos entre SEAC y EGOC y encontraron que SEAC reconoce únicamente la versión “activa” de EGOC, en la que una de sus pequeñas GTPasas, Gtr1, porta un nucleótido similar a GTP, mientras que su pareja, Gtr2, tiene GDP. SEACIT aporta un “dedo” catalítico que alcanza el bolsillo de nucleótidos de Gtr1 y acelera la hidrólisis de GTP, convirtiendo a EGOC de un estado activo a uno inactivo. Mapas detallados de crio-EM y experimentos de mutación muestran que este dedo catalítico y un residuo auxiliar vecino son esenciales para la interacción y para leer correctamente el estado del nucleótido. Cuando los autores alteraron estos residuos clave, SEAC dejó de localizarse correctamente en la vacuola y EGOC no pudo engancharse de forma productiva.
Control rápido frente a control lento del interruptor de crecimiento
Para entender qué significa esto en la célula viva, los investigadores siguieron la actividad de TORC1 en el tiempo cuando se eliminaron y luego se reintrodujeron aminoácidos. En células normales, TORC1 se apaga rápidamente en pocos minutos tras la privación de nitrógeno y vuelve a encenderse con rapidez cuando regresan los aminoácidos. Cuando el dedo catalítico en SEACIT se desactivó, o se eliminaron subunidades de SEACIT, TORC1 apenas respondió en esta ventana temporal temprana. Lo mismo ocurrió al eliminar tanto Gtr1 como Gtr2, lo que demuestra que el par SEAC–EGOC es la vía dominante y rápida para el control por aminoácidos de TORC1. Sin embargo, a tiempos más tardíos—en torno a media hora—la actividad de TORC1 se ajustó lentamente incluso en estos mutantes, lo que indica que existe una vía separada y más lenta hacia TORC1, independiente de este sistema de GTPasas, que también opera en las células.
Un papel sorprendente para una subunidad alejada
Un hallazgo particularmente intrigante concierne a Sea2, una componente de SEACAT con un dominio flexible en forma de “hélice” o “propela” que sobresale del núcleo. Eliminar Sea2, o solo su propela, produjo defectos de señalización casi idénticos a los observados cuando se pierde la actividad catalítica de SEAC: TORC1 respondió con lentitud tanto a la retirada como a la reintroducción de aminoácidos. Sin embargo, Sea2 se encuentra lejos del sitio catalítico y no toca directamente el ala de SEACIT, lo que hace poco probable un mecanismo simple de bloqueo. Experimentos genéticos que combinaron la pérdida de Sea2 con una variante catalíticamente inactiva de SEAC sugirieron que tener la actividad GAP completamente encendida o completamente apagada interfiere con la respuesta rápida, mientras que se necesita una regulación intermedia. Los autores proponen que la propela de Sea2 actúa como una plataforma de acoplamiento para un factor desconocido que modera la actividad de SEACIT, permitiendo a las células afinar TORC1 en lugar de apagarlo permanentemente.
Qué implica esto para las decisiones de crecimiento celular
En conjunto, el estudio replantea a SEAC no como dos ensamblajes opuestos sino como una única máquina integrada cuya ala catalítica (SEACIT) y núcleo estructural (SEACAT) trabajan juntos para detectar aminoácidos y ajustar rápidamente el interruptor de crecimiento TORC1. La acción enzimática de SEACIT sobre EGOC proporciona el control rápido y preciso, mientras que la propela de Sea2 probablemente recluta reguladores que modulan esta actividad. Al mismo tiempo, vías paralelas más lentas aseguran que TORC1 refleje finalmente el estado de los nutrientes incluso si el sensor primario está alterado. Dado que complejos estrechamente relacionados realizan la misma función en células humanas, estos conocimientos procedentes de la levadura iluminan cómo nuestras propias células equilibran el crecimiento con el suministro de nutrientes, con implicaciones para comprender enfermedades en las que la señalización de TORC1 falla.
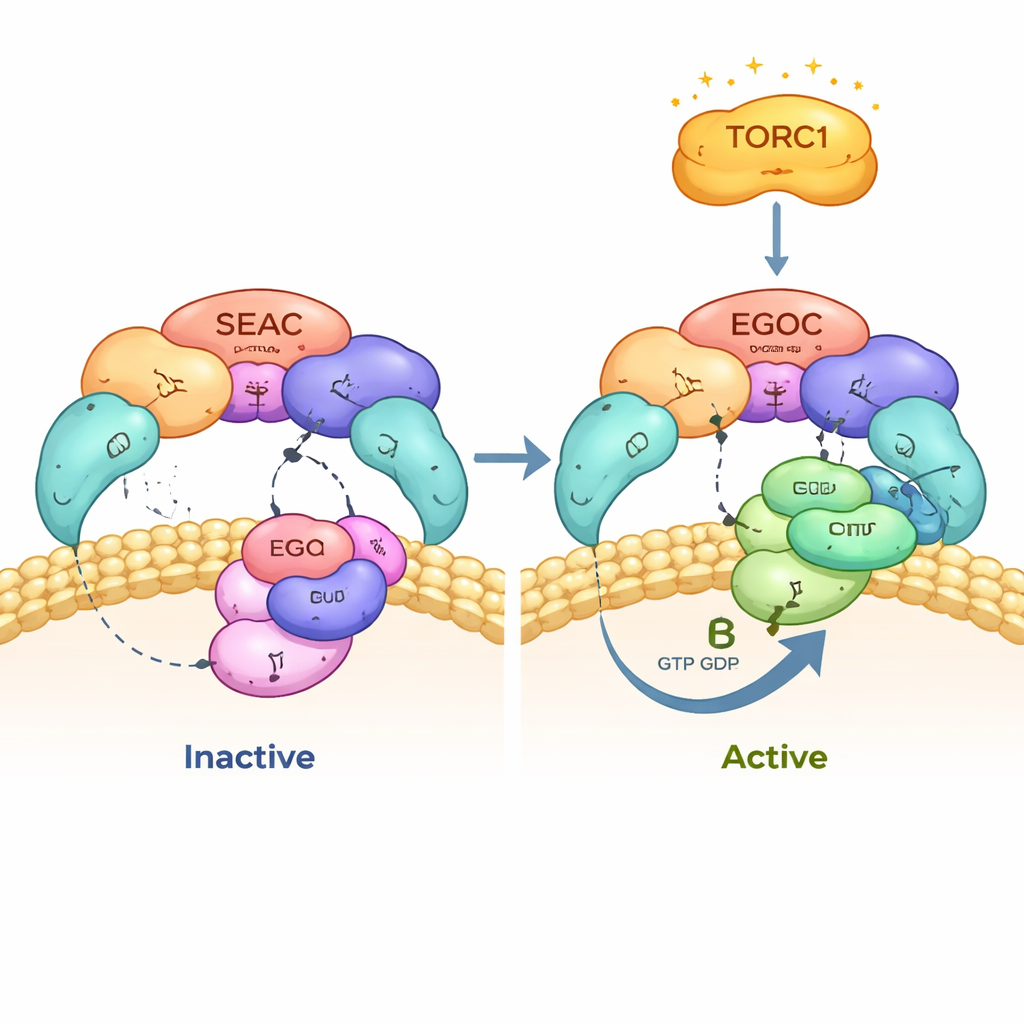
Cita: Tafur, L., Bonadei, L., Zheng, Y. et al. Structure and function of the yeast amino acid-sensing SEAC–EGOC supercomplex. Nat Struct Mol Biol 33, 488–498 (2026). https://doi.org/10.1038/s41594-026-01746-2
Palabras clave: detección de aminoácidos, señalización TORC1, complejo SEAC GATOR, control del crecimiento celular, crioelectrón microscopia