Clear Sky Science · es
Mecanismo y reconstitución de la transcripción circadiana en cianobacterias
Por qué importan los relojes biológicos, incluso en bacterias
Todos los seres vivos, desde los humanos hasta los microbios más pequeños, mantienen un ritmo temporal. Estos relojes internos ayudan a los organismos a anticipar el amanecer y el anochecer, programando actividades como la alimentación, la reparación y el crecimiento. Este artículo explora cómo una bacteria fotosintética sencilla, Synechococcus elongatus, utiliza un reloj proteico para activar y desactivar genes con una precisión notable a lo largo de un ciclo de 24 horas. Al reconstruir este sistema temporal en un tubo de ensayo, los investigadores revelan una versión depurada de un reloj biológico que podría inspirar nuevas herramientas para la biotecnología y la biología sintética.
Un reloj diminuto que funciona con química
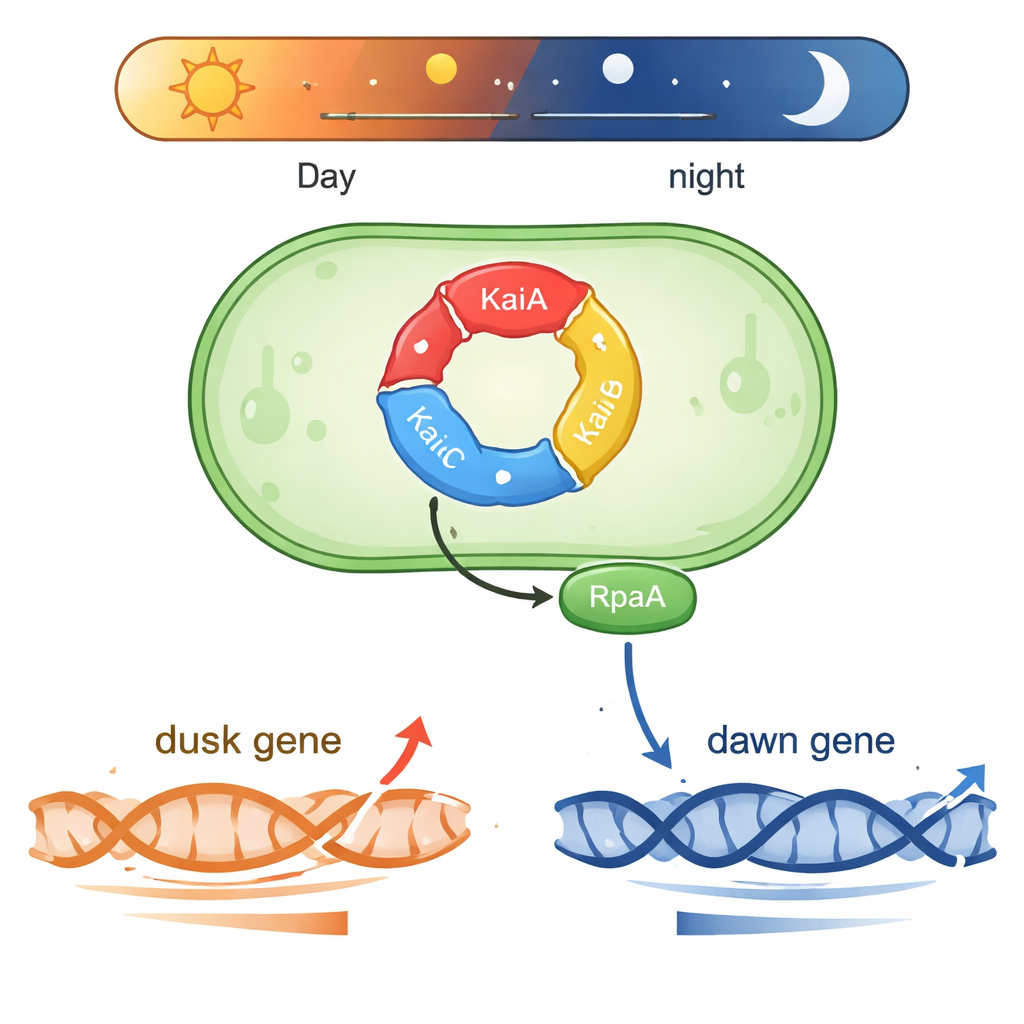
Synechococcus vive en aguas iluminadas por el sol y necesita predecir los cambios diarios en la luz. En su núcleo hay una máquina proteica de tres componentes formada por KaiA, KaiB y KaiC. Estas proteínas intercambian grupos fosfato en un ciclo repetitivo que dura alrededor de 24 horas, formando un «tren de engranajes» bioquímico que mantiene el tiempo incluso fuera de la célula. Otras dos proteínas, SasA y CikA, leen el estado de fosforilación de KaiC y lo utilizan para controlar otra proteína, RpaA. Cuando RpaA está fosforilada, se une al ADN y actúa como un interruptor maestro para cientos de genes que suben y bajan ya sea en torno al “amanecer” o al “anochecer” subjetivos en luz constante.
Una proteína, dos programas génicos opuestos
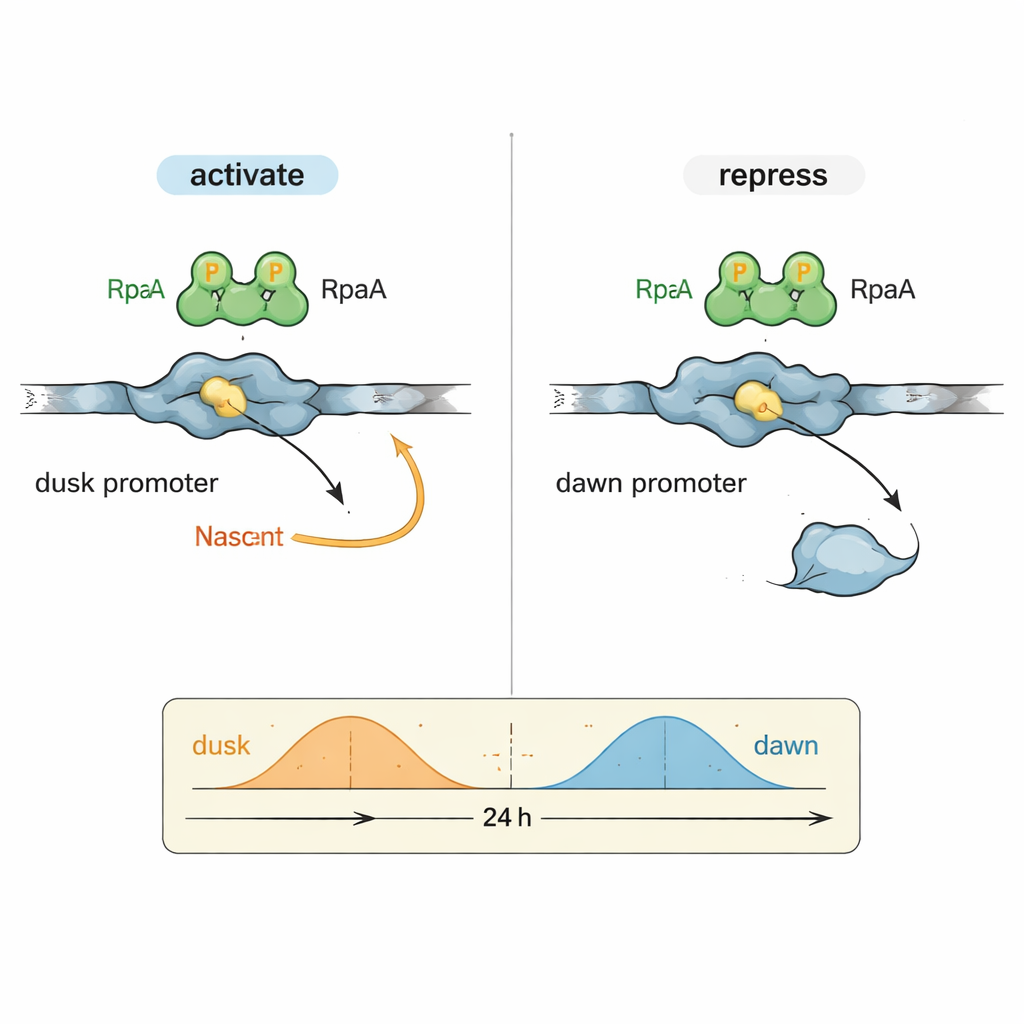
Un enigma en biología circadiana ha sido cómo un factor de salida, RpaA, puede coordinar genes que alcanzan su pico en momentos muy distintos del día. Los autores se centraron en dos regiones representativas de control del ADN (promotores): kaiBC, que es más activo al anochecer, y purF, que alcanza su pico al amanecer. En reacciones controladas usando ARN polimerasa cianobacteriana purificada y RpaA, demostraron que RpaA fosforilada aumenta la transcripción desde el promotor kaiBC mientras que, al mismo tiempo, reduce la transcripción desde el promotor purF. Experimentos detallados de footprinting mapearon exactamente dónde se une RpaA en cada fragmento de ADN, revelando que su posición relativa a los elementos promotores estándar determina si actúa como acelerador o freno.
Ver el interruptor del reloj a detalle atómico
Para entender este comportamiento dual a nivel molecular, el equipo empleó criomicroscopía electrónica de alta resolución para capturar la estructura de RpaA unido al promotor kaiBC junto con la ARN polimerasa. Las imágenes muestran a RpaA sujetando el ADN como un par asimétrico y contactando dos partes clave de la enzima: la cola de la subunidad alfa y una región del factor sigma que normalmente reconoce las secuencias promotoras. Estos contactos doblan el ADN y ayudan a posicionar la ARN polimerasa en un sitio de inicio de transcripción ligeramente redefinido. Mutaciones seleccionadas que debilitan cualquiera de estos puntos de contacto reducen o abolén la activación de kaiBC, tanto in vitro como en células vivas, confirmando que el reclutamiento físico de la ARN polimerasa es la base de la activación génica en fase de anochecer.
Construir un gen impulsado por el reloj desde cero
Como la ARN polimerasa nativa de las cianobacterias es compleja y difícil de mantener activa durante días, los investigadores recurrieron a la mucho más simple polimerasa del bacteriófago T7, ampliamente usada en laboratorios. RpaA no puede reclutar a esta enzima no relacionada, pero aún puede bloquearla al sentarse sobre el ADN. El equipo diseñó una plantilla de ADN sintética donde un promotor T7 dirige un reportero de ARN fluorescente “Broccoli”, con un sitio de unión de RpaA colocado aguas abajo. Cuando combinaron esta plantilla con el reloj KaiA–KaiB–KaiC, la quinasa/fosfatasa CikA, RpaA y la polimerasa T7 en un único tampón optimizado, observaron tasas de transcripción que aumentaban y disminuían con un periodo de aproximadamente 24 horas. El ritmo pudo reiniciarse cambiando la relación ATP/ADP y se mantuvo con casi el mismo periodo en un rango de temperaturas: rasgos clásicos de un verdadero reloj circadiano.
De relojes simples a cronometraje diseñado
El estudio muestra que solo seis proteínas son suficientes para conectar un marcapasos químico con una lectura génica rítmica: las tres proteínas del reloj Kai, CikA, RpaA y una ARN polimerasa. Al cambiar dónde se ubica RpaA en el ADN, la misma molécula puede hacer que algunos genes alcancen su pico al anochecer y otros al amanecer, lo que ayuda a explicar las complejas olas de actividad génica observadas en las cianobacterias. Dado que el diseño basado en represión funciona incluso con una polimerasa ajena como la T7, debería ser posible trasplantar este módulo de reloj mínimo a otros microbios o sistemas sin células, permitiendo a los científicos programar genes para que se activen y desactiven con ritmos diarios para investigación, producción industrial o futuras aplicaciones terapéuticas.
Cita: Fang, M., Gu, Y., Leanca, M. et al. Mechanism and reconstitution of circadian transcription in cyanobacteria. Nat Struct Mol Biol 33, 275–281 (2026). https://doi.org/10.1038/s41594-025-01740-0
Palabras clave: reloj circadiano, cianobacterias, regulación de la transcripción, RpaA, biología sintética