Clear Sky Science · es
Distribución masiva de azitromicina y resistencia a antibióticos en el intestino y la nasofaringe: un ensayo aleatorizado por conglomerados
Por qué importa dar una pastilla a muchos niños
En partes de África Occidental, un único antibiótico, la azitromicina, se ha utilizado en campañas masivas para reducir el número de niños pequeños que mueren por infecciones. La estrategia funciona, pero plantea una preocupación seria: ¿estamos fomentando silenciosamente gérmenes más resistentes a los medicamentos en el organismo de los niños? Este estudio, realizado en cientos de aldeas en Níger, examina de cerca el interior de los intestinos y las fosas nasales de los niños para ver cómo los tratamientos repetidos a nivel comunitario remodelan su mundo microbiano oculto y la resistencia a los antibióticos.
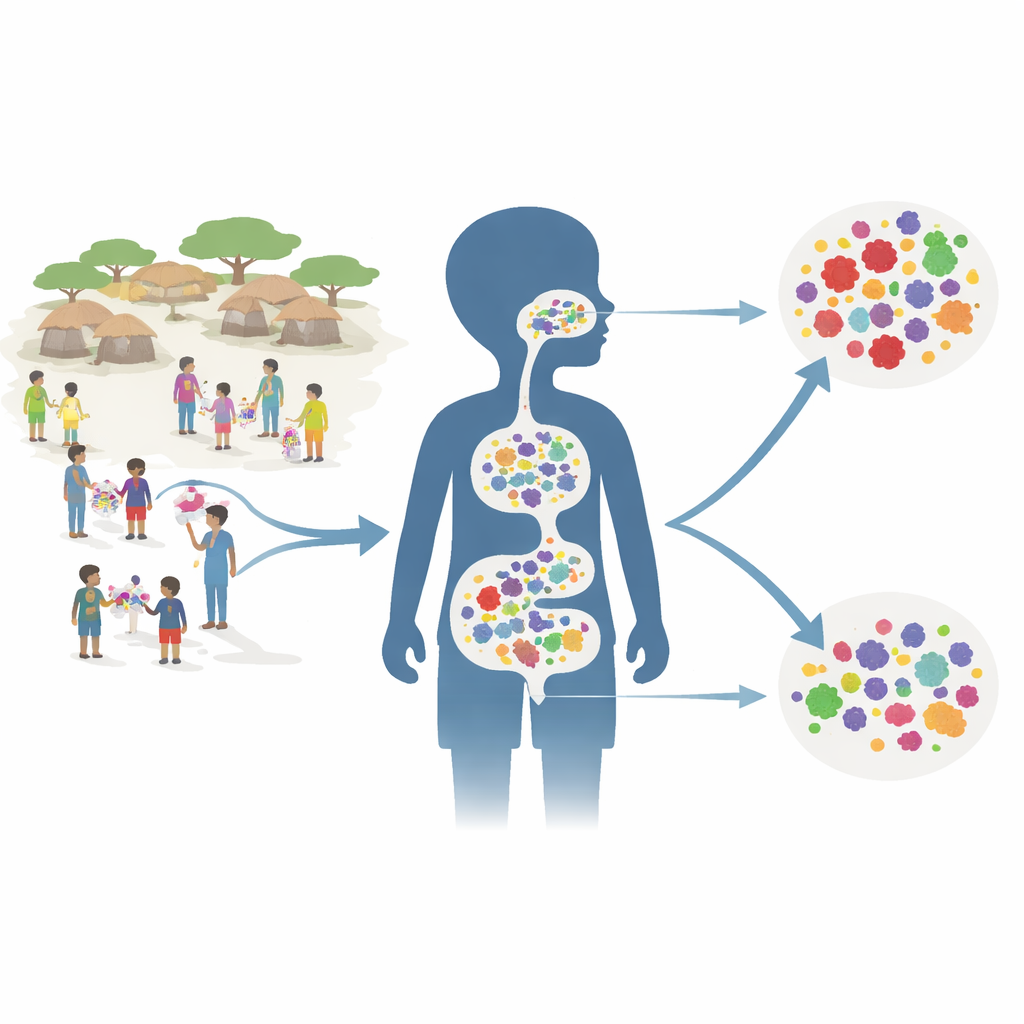
Evaluando un plan de medicación comunitaria
Los investigadores integraron su trabajo dentro de un gran ensayo llamado AVENIR, que ya había mostrado que administrar azitromicina cada seis meses a todos los niños de 1 a 59 meses podía reducir las muertes en este grupo etario. Para el estudio de resistencia se centraron en 150 aldeas seleccionadas al azar. Cada aldea pertenecía a uno de tres grupos: todos los niños pequeños recibieron azitromicina; solo los lactantes hasta 11 meses recibieron azitromicina mientras que los niños mayores recibieron placebo; o todos los niños recibieron placebo. Dos años después del inicio del programa—seis meses tras la cuarta ronda de tratamiento—el equipo recogió hisopos rectales y nasales profundos de aproximadamente 30 niños por aldea.
Mirando dentro del intestino y la nariz
En lugar de cultivar gérmenes en el laboratorio, los científicos agruparon las muestras de cada aldea y utilizaron secuenciación de ADN moderna. Esto les permitió catalogar qué bacterias estaban presentes y contar marcadores genéticos que señalan resistencia a distintas familias de antibióticos. Prestaron especial atención a los macrólidos—la familia de fármacos que incluye la azitromicina—mientras también rastreaban la resistencia a muchos otros tipos de antibióticos de uso común, como los similares a la penicilina. Se examinaron el intestino y la nasofaringe (la parte superior de la garganta detrás de la nariz) porque ambos son reservorios importantes donde los genes de resistencia pueden acumularse y potencialmente difundirse.
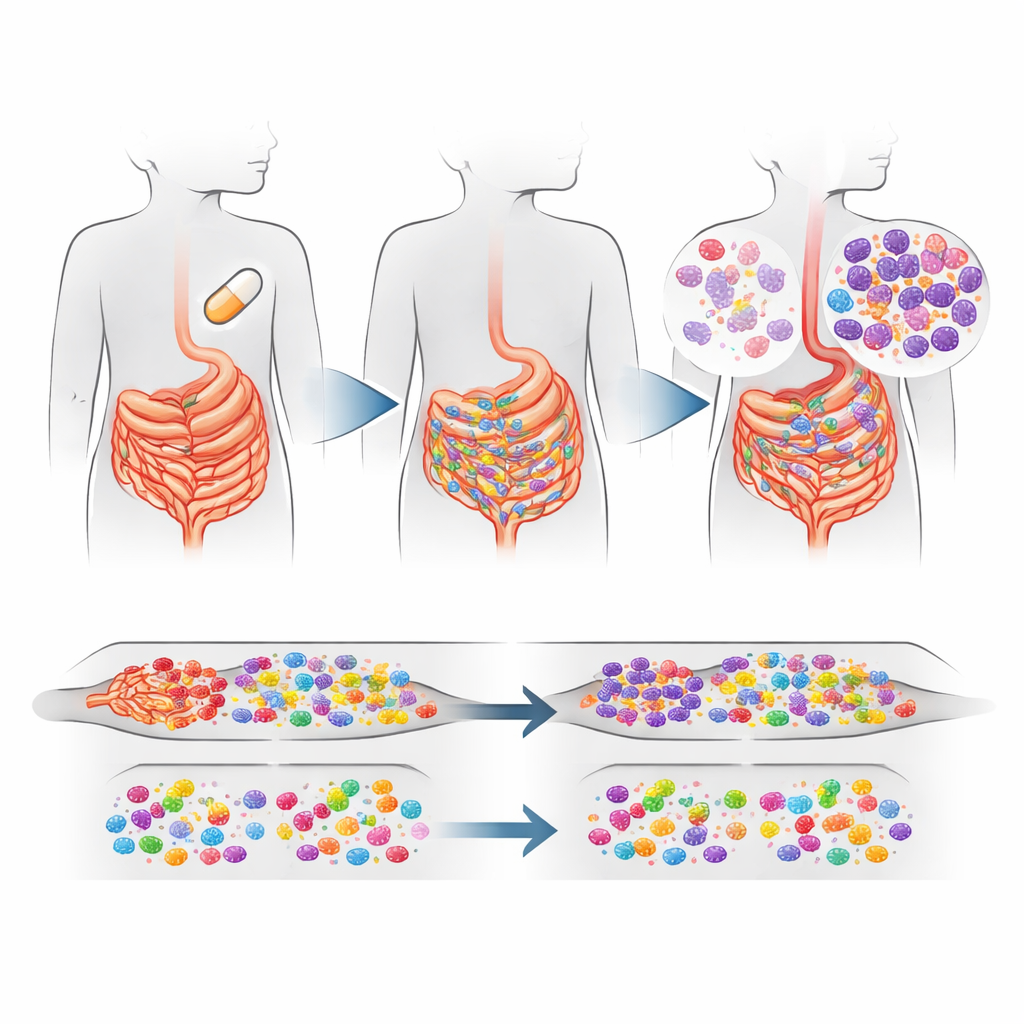
Qué cambió dentro del intestino de los niños
La señal más clara provino del intestino. En las aldeas donde todos los niños recibieron azitromicina hubo un aumento modesto pero estadísticamente fiable—aproximadamente un 16% más en conjunto—de genes de resistencia a macrólidos en las bacterias intestinales en comparación con las aldeas con placebo. El aumento estuvo impulsado en gran medida por un gen de resistencia llamado ermF, que ayuda a proteger a las bacterias frente a los macrólidos. Este gen suele ser llevado por bacterias intestinales comunes como Bacteroides y Prevotella, que normalmente viven de forma inofensiva en los intestinos pero que a veces pueden causar enfermedad. De forma interesante, los genes de resistencia contra otras familias importantes de antibióticos no aumentaron, y la composición y diversidad general de las bacterias intestinales se mostró en términos generales similar entre los grupos de tratamiento, aunque algunas especies concretas se hicieron más o menos comunes.
Qué permaneció igual en la nariz
En contraste, las vías nasales contaron una historia más tranquila. El estudio no encontró diferencias claras y estadísticamente sólidas en los genes de resistencia a macrólidos entre los grupos de tratamiento en la nasofaringe, ni evidencia de que se estuviera seleccionando resistencia a otras clases de antibióticos allí. Los residentes típicos de la nariz—géneros como Moraxella, Haemophilus y Streptococcus—siguieron dominando. Algunas bacterias relacionadas con la boca vinculadas a enfermedades de las encías se hicieron más comunes en las comunidades tratadas con azitromicina, y algunas de estas también pueden portar genes de resistencia, pero la carga general de resistencia en la nariz no cambió de la misma manera que en el intestino.
Equilibrar las ganancias de hoy con los riesgos de mañana
En conjunto, los hallazgos muestran que administrar azitromicina a todos los niños pequeños de una comunidad puede salvar vidas, pero también empuja a las bacterias intestinales hacia una mayor resistencia a esta familia de fármacos, principalmente mediante la expansión de genes de resistencia específicos como ermF. El estudio no observó un desbordamiento hacia resistencia frente a otros tipos de antibióticos en la ventana de dos años, ni cambios fuertes en el reservorio nasal, pero los autores advierten que las bacterias intestinales resistentes y sus genes pueden propagarse con el tiempo y entre personas. Argumentan que cualquier programa amplio de antibióticos para la supervivencia infantil debería incorporar un seguimiento cuidadoso y a largo plazo de la resistencia para que las autoridades sanitarias puedan seguir ponderando el beneficio inmediato de menos muertes infantiles frente al costo más lento y menos visible de fortalecer microbios resistentes a los fármacos.
Cita: Doan, T., Yan, D., Arzika, A.M. et al. Mass azithromycin distribution and antibiotic resistance in the gut and nasopharynx: a cluster-randomized trial. Nat Med 32, 859–868 (2026). https://doi.org/10.1038/s41591-026-04217-9
Palabras clave: azitromicina, mortalidad infantil, resistencia a antibióticos, microbioma intestinal, administración masiva de fármacos