Clear Sky Science · es
Atlas unicelular de la corteza cerebral en desarrollo en el síndrome de Down
Por qué importa esta investigación
El síndrome de Down es la causa genética más común de discapacidad intelectual, pero aún sabemos poco sobre cómo altera el cerebro humano en desarrollo antes del nacimiento. Este estudio se acerca hasta el nivel de células individuales en la corteza fetal —la región cerebral clave para el pensamiento y la memoria— para cartografiar qué falla, cuándo comienza y qué interruptores moleculares podrían ser dianas terapéuticas.
Un vistazo detallado al cerebro en crecimiento
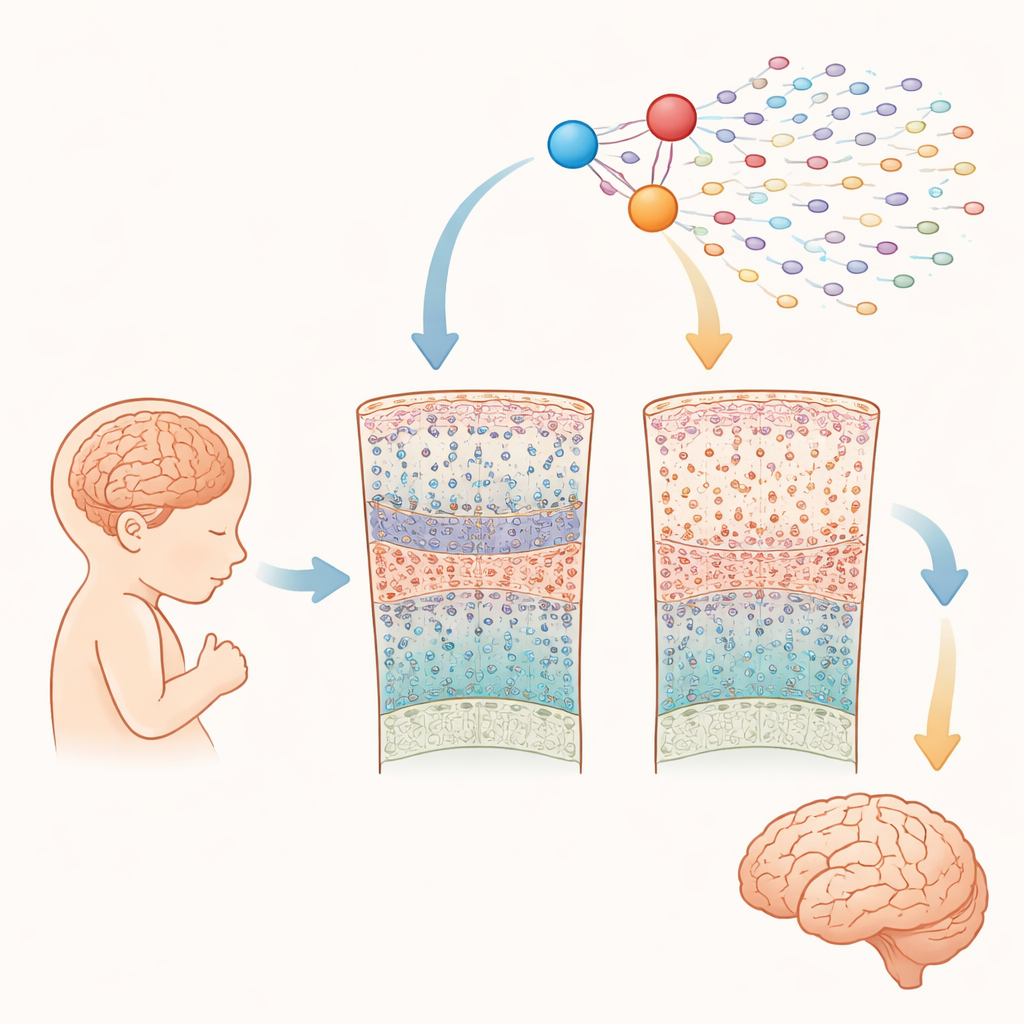
Los investigadores analizaron casi un cuarto de millón de células tomadas de la corteza cerebral de 15 fetos con síndrome de Down y 15 sin él, entre las 10 y las 20 semanas tras la concepción. Empleando métodos avanzados de "una sola célula", midieron tanto qué genes estaban activos como la accesibilidad del ADN en cada célula. Esto les permitió identificar todos los tipos celulares principales presentes en esta etapa de gestación media —como células progenitoras con rasgos de células madre, distintos tipos de neuronas excitadoras e inhibitorias y glía en etapas tempranas— y comparar su abundancia y actividad génica entre cerebros con síndrome de Down y cerebros típicos.
Cambios tempranos en células clave del pensamiento
La mayoría de las clases celulares amplias estaban presentes en números similares en ambos grupos durante esta ventana temprana. Sin embargo, el equipo encontró un déficit llamativo y selectivo de un tipo particular de neurona excitadora que normalmente ocupa la capa 4 de la corteza y es importante para procesar la información entrante. Estas neuronas se definen por las proteínas RORB y FOXP1. En fetos con síndrome de Down, las neuronas RORB–FOXP1 ya estaban reducidas a mitad de la gestación, especialmente entre las semanas 16 y 20, mientras que otros tipos neuronales parecían relativamente preservados. Esto sugiere que los problemas en la generación o maduración de este subconjunto celular comienzan in utero y pueden contribuir directamente a las dificultades cognitivas posteriores.
Programas genéticos alterados e interruptores maestros
Más allá del recuento celular, el estudio reveló que cientos de genes estaban sutilmente desregulados, particularmente en las neuronas excitadoras y sus progenitores. Muchos de estos genes participan en la construcción del prosencéfalo, la modelación de las ramas neuronales, la formación de conexiones y el soporte de funciones cerebrales superiores. En lugar de que solo las copias extras de unas ~200 genes del cromosoma 21 actúen de forma aislada, los datos apuntan a una red perturbada de regulación génica. Mediante un enfoque que combina la actividad génica con la accesibilidad del ADN, los autores trazaron circuitos regulatorios y destacaron tres factores de transcripción —BACH1, PKNOX1 y GABPA— codificados en el cromosoma 21 como "nodos" sensibles a la dosis. Estas moléculas parecen influir en otros reguladores críticos del desarrollo cortical, incluidos factores ya vinculados a la discapacidad intelectual, y ayudan a explicar cómo un aumento modesto de 1,5 veces en la dosis génica puede propagarse a través de programas de desarrollo completos.
Probar estrategias de rescate en células y cerebros vivos
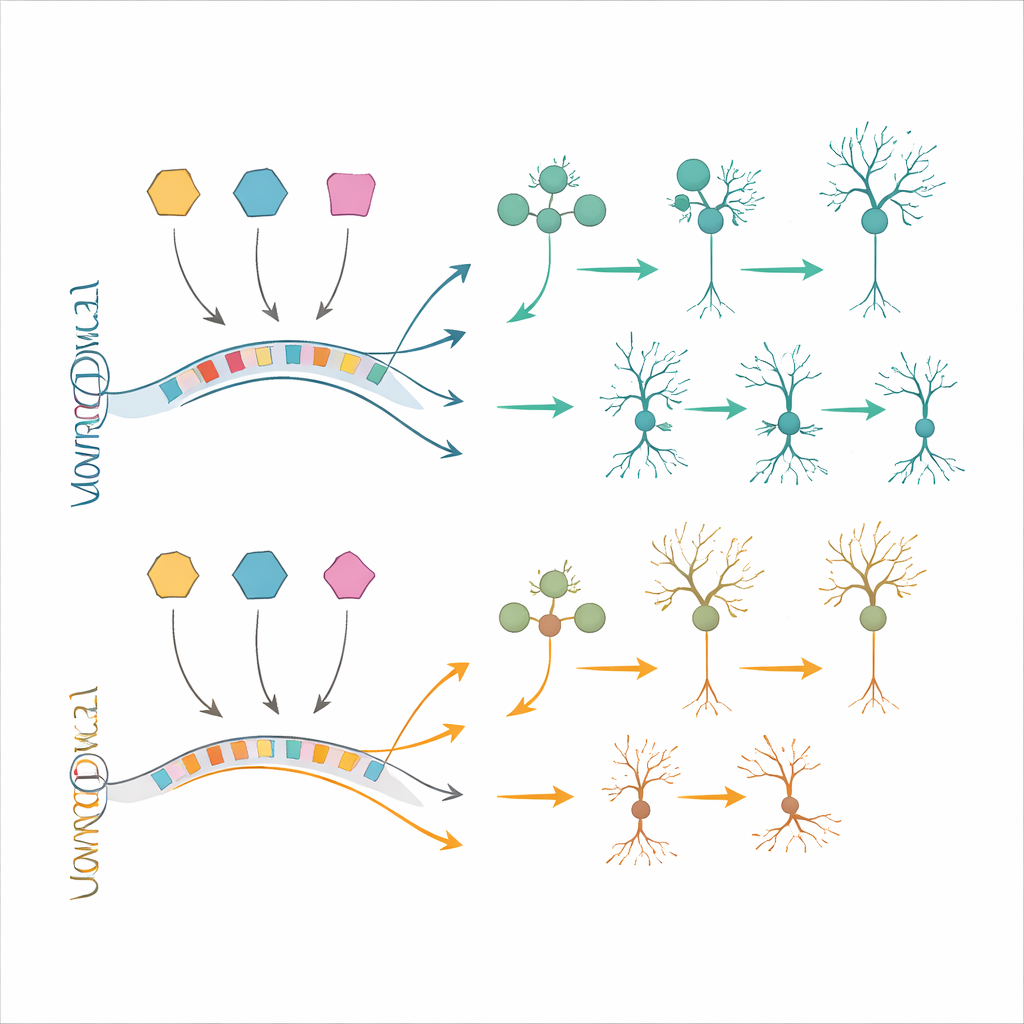
Para evaluar si estos cambios moleculares podían corregirse, el equipo recurrió a modelos con células madre. Generaron progenitores neuronales y neuronas a partir de células madre pluripotentes inducidas portadoras de trisomía 21 y de células control emparejadas. Muchos de los cambios en la expresión génica observados en tejido fetal reaparecieron en estas células cultivadas en el laboratorio, confirmando la relevancia de los modelos. Los investigadores usaron entonces oligonucleótidos antisentido —cadenas cortas de material similar al ADN diseñado— para reducir BACH1, PKNOX1 o GABPA hacia niveles normales. Esta normalización parcial de los factores de transcripción sobreexpresados condujo a una recuperación parcial de varios genes downstream, incluidos algunos ya conocidos por participar en la discapacidad intelectual y la diferenciación neuronal. En un enfoque complementario, trasplantaron células neuronales humanas con trisomía 21 en cerebros de ratón y las dejaron madurar in vivo. Estos injertos reprodujeron rasgos adicionales semejantes al síndrome de Down, como un balance alterado entre neuronas y glía y cambios genéticos que no se captaban por completo en cultivo, ofreciendo un banco de pruebas potente para futuras terapias.
Qué significa esto para el futuro
En conjunto, el trabajo ofrece un atlas detallado de cómo el síndrome de Down remodela el paisaje genético de la corteza en desarrollo con resolución unicelular. Para un lector general, el mensaje clave es que el cromosoma extra no solo añade unos cuantos genes problemáticos; empuja muchos interruptores moleculares interconectados, lo que conduce a déficits tempranos y selectivos de ciertas neuronas relacionadas con el pensamiento. Al identificar un pequeño grupo de factores de transcripción del cromosoma 21 como actores centrales —y al mostrar que sus efectos pueden revertirse parcialmente en células humanas—, el estudio abre la puerta a estrategias más dirigidas para mejorar el desarrollo y la función cerebral en el síndrome de Down.
Cita: Lattke, M., Tan, W.L., Sukumaran, S.K. et al. Single-cell atlas of the developing Down syndrome brain cortex. Nat Med 32, 1061–1072 (2026). https://doi.org/10.1038/s41591-026-04211-1
Palabras clave: Síndrome de Down, desarrollo fetal del cerebro, genómica unicelular, neuronas corticales, factores de transcripción