Clear Sky Science · es
Células CAR-T dirigidas a CD19 para enfermedades autoinmunes refractarias al tratamiento: el ensayo fase 1/2 CASTLE tipo cesta
Por qué importa un tratamiento de una sola vez
Muchas personas con enfermedades autoinmunes graves viven en una rueda interminable de medicación: brote tras brote y efectos secundarios acumulados. Este estudio explora una idea radicalmente diferente: usar una única infusión de células inmunitarias reprogramadas para «reiniciar» el sistema inmunitario y que deje de atacar al propio cuerpo. Para pacientes con lupus severo, endurecimiento de la piel y órganos, o inflamación muscular que han agotado las opciones, ese reinicio podría significar alivio duradero sin fármacos diarios.
Tres enfermedades duras, un problema común
El lupus eritematoso sistémico, la esclerosis sistémica y las miopatías inflamatorias idiopáticas pueden parecer distintas en su presentación—afectando articulaciones, piel, pulmones, riñones o músculos—pero comparten un defecto central: ciertas células inmunitarias llamadas células B fallan y contribuyen a la inflamación crónica. Los tratamientos estándar, desde esteroides hasta fármacos inmunosupresores potentes y perfusiones de anticuerpos, pueden calmar los síntomas pero rara vez eliminan la causa raíz. Muchos pacientes pasan por múltiples terapias que solo funcionan parcialmente o provocan efectos secundarios intolerables, quedando con daño orgánico progresivo y mala calidad de vida.
Reprogramar los defensores del cuerpo
El ensayo CASTLE probó una terapia celular personalizada llamada Zorpo-cel en 24 adultos con formas severas y resistentes al tratamiento de estas tres enfermedades. Los médicos primero recolectaron los linfocitos T de cada paciente, los «soldados» del sistema inmunitario, y en el laboratorio los dotaron de un nuevo sensor—un receptor quimérico de antígeno—que reconoce un marcador llamado CD19 presente en la mayoría de las células B. Tras un breve ciclo de quimioterapia para crear espacio en el sistema inmunitario, los pacientes recibieron una única infusión de estas células modificadas, conocidas como células CAR-T anti-CD19. La esperanza era que identificaran y eliminaran las células B descontroladas, permitiendo que creciera un repertorio celular más saludable.
Primero seguridad, luego señales de alivio
Dado que este tratamiento puede ser intenso en pacientes con cáncer, el objetivo principal de este ensayo en fase temprana fue la seguridad. Los investigadores vigilaron de cerca una reacción inflamatoria peligrosa llamada síndrome de liberación de citocinas y los efectos secundarios neurológicos. En CASTLE, casi tres cuartas partes de los pacientes tuvieron solo fiebre e inflamación leves y de corta duración; no se observaron tormentas de citocinas graves, toxicidad cerebral ni problemas hematológicos persistentes. Los problemas más comunes fueron descensos temporales de los glóbulos blancos e infecciones leves, que se manejaron con cuidados estándar. Un paciente desarrolló lesión renal asociada a la reactivación de un virus y a un brote de la enfermedad subyacente, lo que llevó a establecer normas más estrictas para controlar la actividad de la enfermedad antes de la infusión.
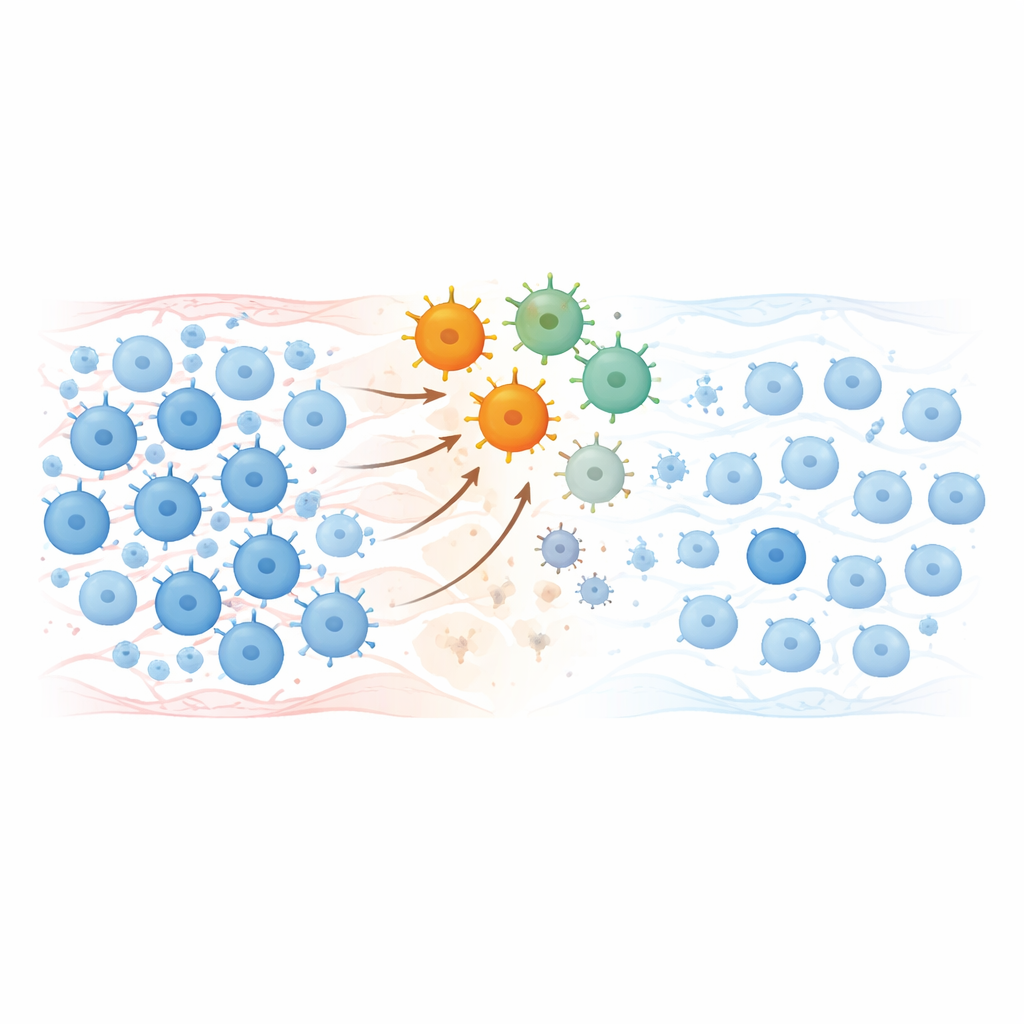
Reiniciar el sistema inmunitario
Aunque la seguridad fue la prioridad, las mejoras clínicas fueron llamativas. A los seis meses, 22 de 24 pacientes cumplieron criterios de éxito predefinidos adaptados a su enfermedad: la mayoría de los pacientes con lupus alcanzaron una definición estricta de remisión, todos los pacientes con esclerosis sistémica no empeoraron en la enfermedad pulmonar y mostraron mejor función respiratoria y una piel más blanda, y la mayoría de los pacientes con inflamación muscular ganaron fuerza y tuvieron niveles más bajos de enzimas musculares. Es importante subrayar que todos los participantes pudieron suspender los esteroides y otros inmunosupresores y mantenerse sin ellos durante el estudio de seis meses y más allá, sin relapsos observados en un seguimiento medio de alrededor de un año.
Qué ocurre en la sangre
Las pruebas de laboratorio mostraron que las células CAR-T infundidas se expandieron durante unos días, eliminaron las células B circulantes y luego desaparecieron gradualmente en un par de meses. Cuando las células B reaparecieron, su población era distinta: predominaban células vírgenes y «frescas», mientras que las células de memoria y los precursores productores de anticuerpos que a menudo albergan la memoria autoinmune se redujeron notablemente. Muchos autoanticuerpos dañinos cayeron a niveles muy bajos o indetectables, sin embargo los anticuerpos protectores de vacunas previas contra infecciones como sarampión o tétanos se mantuvieron en gran parte, lo que sugiere un reinicio dirigido más que un borrado total de la memoria inmunitaria.
Una visión de una nueva era terapéutica
Para las personas que viven con una enfermedad autoinmune grave, la idea de un tratamiento único que produzca remisión duradera sin fármacos parecía hasta ahora inalcanzable. Este ensayo sugiere que las células T modificadas pueden silenciar de forma segura a las células B rebeldes en tres enfermedades distintas y permitir que el sistema inmunitario se reconstruya de forma más tranquila y menos autodestructiva. CASTLE es un estudio temprano y relativamente pequeño, y serán necesarios ensayos pivotal más amplios para confirmar la duración del beneficio y qué pacientes se benefician más. Aun así, apunta hacia un futuro en el que reiniciar el sistema inmunitario—en lugar de suprimirlo sin fin—podría convertirse en un objetivo realista.
Cita: Müller, F., Hagen, M., Wirsching, A. et al. CD19 CAR-T cells for treatment-refractory autoimmune diseases: the phase 1/2 CASTLE basket trial. Nat Med 32, 1142–1151 (2026). https://doi.org/10.1038/s41591-025-04185-6
Palabras clave: Terapia con células CAR-T, enfermedad autoinmune, lupus eritematoso sistémico, esclerosis sistémica, células B