Clear Sky Science · es
Evasión antigénica multimodal frente a agentes de enlace de células T dirigidos a GPRC5D en mieloma múltiple
Cuando el cáncer supera la inmunoterapia de precisión
Potentes fármacos inmunitarios están transformando el tratamiento del mieloma múltiple, un cáncer de la sangre que sigue siendo incurable para la mayoría de los pacientes. Estas terapias funcionan redirigiendo las propias células T del organismo para que busquen y destruyan células tumorales marcadas por «banderas» específicas en su superficie. Una bandera prometedora es una molécula llamada GPRC5D. Sin embargo, como ocurre con muchas terapias dirigidas, los tumores pueden evolucionar y eludir el tratamiento. Este estudio desentraña, con detalle inusual, cómo las células de mieloma modifican u ocultan la bandera GPRC5D para escapar de fármacos que reclutan células T y que son altamente eficaces.
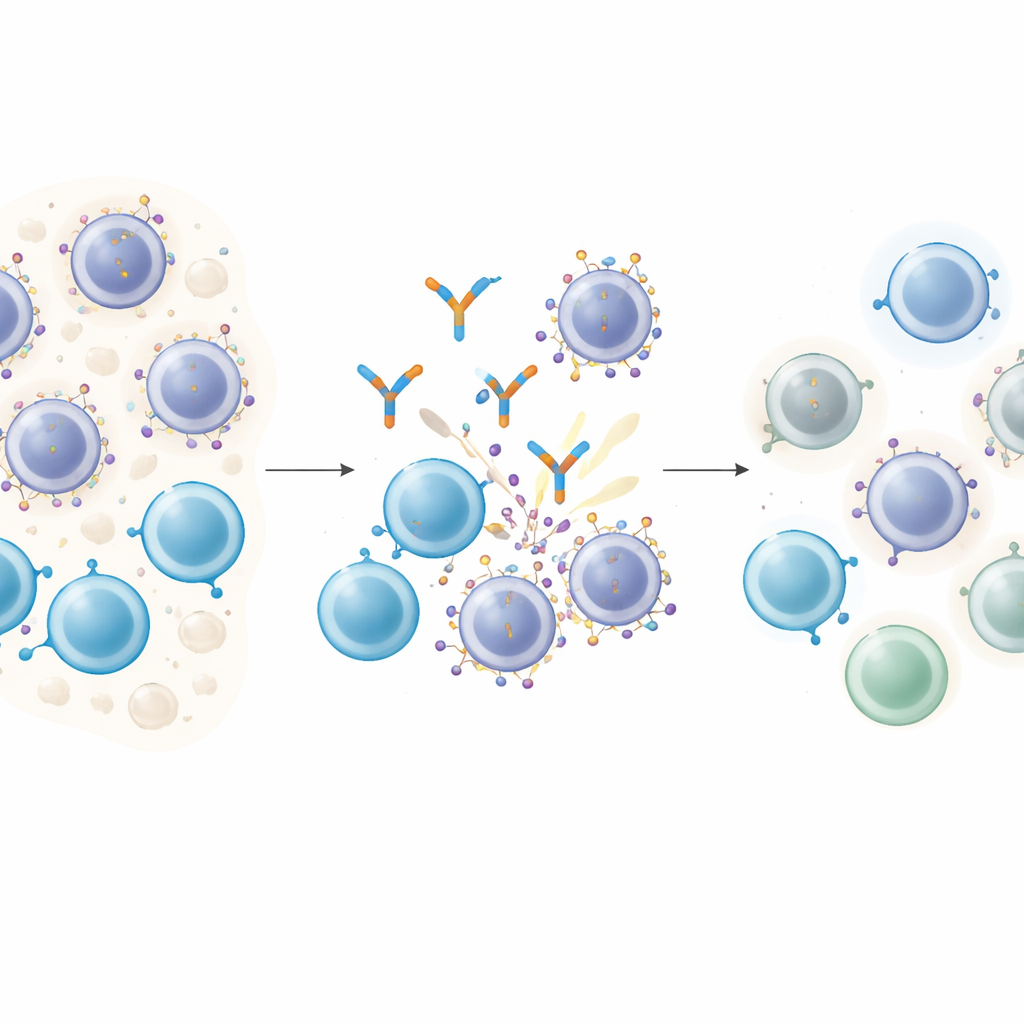
Cómo los fármacos inteligentes se anclan a las células cancerosas
Los anticuerpos que enlazan células T actúan como casamenteros moleculares: un extremo atrapa una célula T y el otro se fija a una molécula diana en la célula cancerosa, acercando ambos en contacto directo para que la célula T pueda matar a su presa. En el mieloma múltiple, GPRC5D es un objetivo atractivo porque es abundante en células plasmáticas malignas y escaso en la mayoría de los tejidos normales. Los pacientes tratados con un fármaco dirigido a GPRC5D llamado talquetamab suelen experimentar remisiones profundas. Sin embargo, casi todos recaen con el tiempo, lo que plantea una pregunta crítica: ¿están cambiando las células cancerosas el mismo objetivo del que dependen estos fármacos?
Rastreando la evolución tumoral en tiempo real
Los investigadores siguieron a 21 personas con mieloma difícil de tratar que recibieron talquetamab. Recogieron muestras de médula ósea antes del tratamiento en algunos pacientes y de nuevo cuando el cáncer reapareció, y luego emplearon múltiples capas de análisis de ADN, ARN y cromatina para examinar las células tumorales. Esta visión ultra‑detallada reveló que, en aproximadamente dos tercios de los pacientes con recaída, el cáncer había alterado GPRC5D de maneras que reducirían o bloquearían el efecto del fármaco. De forma llamativa, varias subclonas resistentes distintas —ramas genéticamente diferentes del tumor— coexistían a menudo en la misma persona, lo que muestra que la evolución hacia la evasión puede seguir múltiples caminos a la vez.
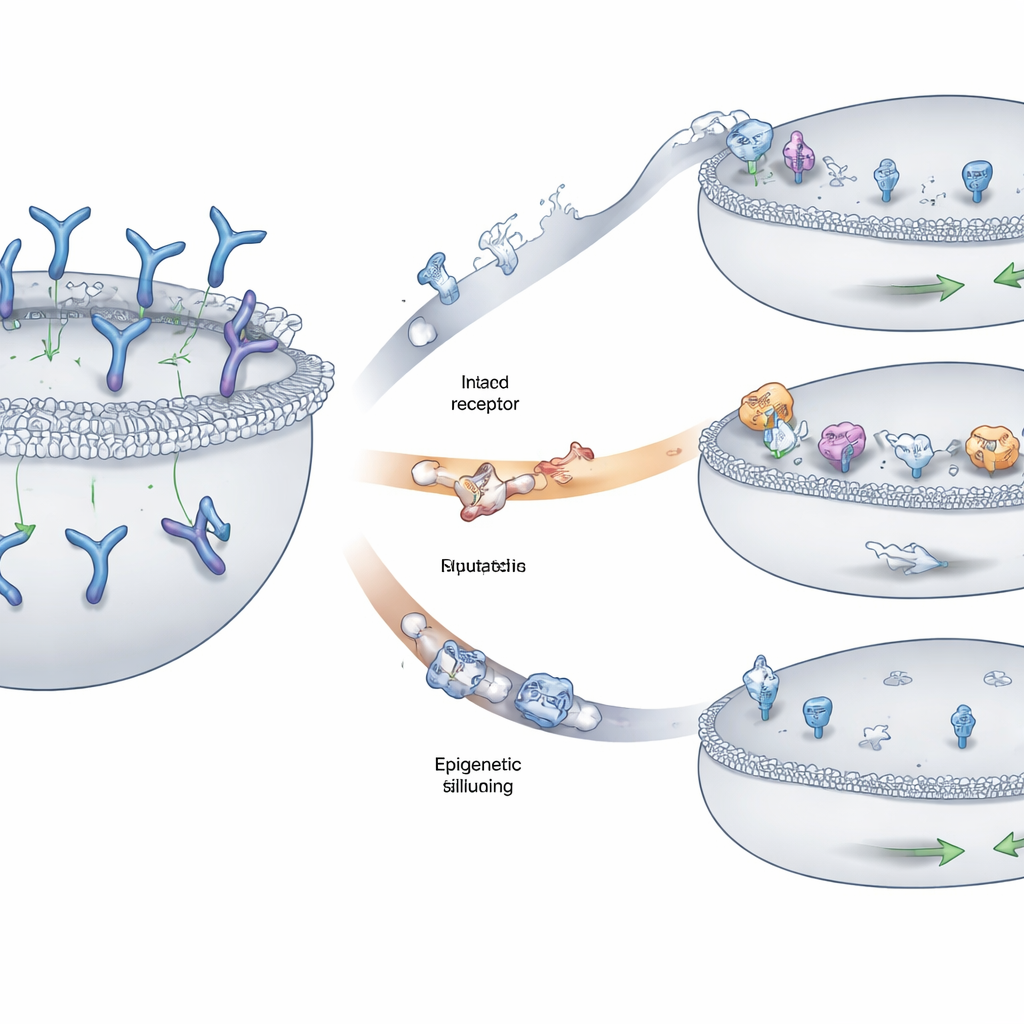
Tres formas principales en que los tumores ocultan el objetivo
El equipo identificó tres patrones recurrentes mediante los cuales las células de mieloma eludían el reconocimiento. En algunos pacientes, fragmentos del cromosoma que contienen el gen GPRC5D se eliminaron en ambas copias, borrando la bandera por completo de la superficie celular. En otros, cambios más pequeños —sustituciones de una sola letra del ADN o pequeñas inserciones y deleciones— deformaron regiones clave de la proteína GPRC5D. Muchas de estas alteraciones perturbaron partes de la proteína necesarias para su correcto tráfico desde el interior celular hasta la membrana externa, provocando que GPRC5D quedara atrapada en compartimentos internos en lugar de mostrarse donde el fármaco pudiera detectarla. Una tercera vía implicó el silenciamiento epigenético: el ADN que rodea a GPRC5D se compactó y marcó químicamente de forma que el gen apenas se transcribía, aunque la secuencia subyacente permaneciera en gran parte intacta. Las células tumorales que usaron esta estrategia produjeron muy poco o nada de GPRC5D.
Cuando la bandera está presente pero la cerradura ya no encaja
No todas las rutas de escape eliminaron GPRC5D de la superficie celular. En algunos casos la proteína parecía normal en las pruebas de laboratorio estándar pero ya no encajaba con el fármaco como una llave en una cerradura. El equipo recreó mutaciones específicas derivadas de pacientes en líneas celulares de laboratorio y evaluó cómo de bien distintos anticuerpos dirigidos a GPRC5D podían unirse y matar estas células. Una mutación alteró sutilmente el punto exacto donde talquetamab se agarra al receptor, reduciendo drásticamente la capacidad del fármaco para unirse y desencadenar la muerte celular, aunque el receptor aún fuera visible con tinciones de rutina. De forma intrigante, otro fármaco dirigido a GPRC5D que se aferra al receptor en dos sitios siguió siendo eficaz contra varias de estas mutaciones, lo que subraya cómo el diseño del fármaco —por ejemplo, el uso de unión multivalente o a múltiples epítopos— puede influir en si las clonas resistentes sobreviven.
Más allá del objetivo: otros límites al ataque inmune
Si bien la mayoría de las recaídas mostraron alguna forma de pérdida o alteración de GPRC5D, una minoría de pacientes recurrió sin cambios evidentes en el propio objetivo. En estos casos, el problema parecía residir en las células T: estaban menos en forma y eran menos capaces de matar células cancerosas en ensayos de laboratorio, lo que sugiere que la exposición continua y prolongada a la terapia de enlace puede agotar el sistema inmune. El estudio también descubrió que un subtipo genético particular de mieloma (que implica un intercambio cromosómico llamado t(11;14)) mantiene de forma natural el gen GPRC5D en un estado de cromatina más “cerrado”, con una expresión basal más baja. Esto plantea la posibilidad de que algunos pacientes puedan estar predispuestos a respuestas pobres porque sus tumores parten ya con niveles atenuados de la bandera objetivo.
Qué significa esto para los pacientes y los tratamientos futuros
Para pacientes y clínicos, este trabajo explica por qué incluso las terapias dirigidas a GPRC5D de gran potencia aún no son curativas: las células de mieloma pueden borrar, reordenar, desviar o apagar la misma bandera de la que dependen estos fármacos, y con frecuencia lo hacen de varias maneras a la vez. Los hallazgos sugieren que monitorizar el ADN tumoral, en lugar de limitarse a medir los niveles de proteína, será importante para detectar mutaciones de escape emergentes que las pruebas estándar pueden pasar por alto. También apuntan a estrategias de nueva generación —como fármacos que se unan a GPRC5D con mayor avididad en varios sitios, combinaciones que ataquen más de un objetivo a la vez o agentes que reabran genes silenciados— para adelantarse a la evolución tumoral. En esencia, este estudio cartografía las rutas de escape que emplea el mieloma para que las terapias futuras puedan diseñarse para bloquearlas, manteniendo los tratamientos basados en células T eficaces durante más tiempo.
Cita: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
Palabras clave: mieloma múltiple, agentes de enlace de células T, GPRC5D, evasión antigénica, inmunoterapia contra el cáncer