Clear Sky Science · es
Linavonkibart y pembrolizumab en tumores sólidos avanzados resistentes a la inmunoterapia con bloqueo de puntos de control: un ensayo de fase 1
Por qué los cánceres resistentes importan a todos
Los fármacos de inmunoterapia que "quitan los frenos" al sistema inmunitario han cambiado el tratamiento de muchos cánceres, pero la mayoría de los pacientes o bien nunca se benefician o finalmente ven que sus tumores vuelven a crecer. Este estudio evalúa un nuevo anticuerpo terapéutico, linavonkibart, diseñado para desactivar un escudo potente que los tumores usan para ocultarse del ataque inmunitario, y lo combina con una inmunoterapia ya existente, pembrolizumab. Los resultados ofrecen un primer indicio de que, incluso en pacientes cuyos cánceres ya habían dejado de responder a los inhibidores de puntos de control, puede ser posible restaurar el control inmunitario manteniedo los efectos secundarios bajo control.
Un escudo oculto alrededor de los tumores
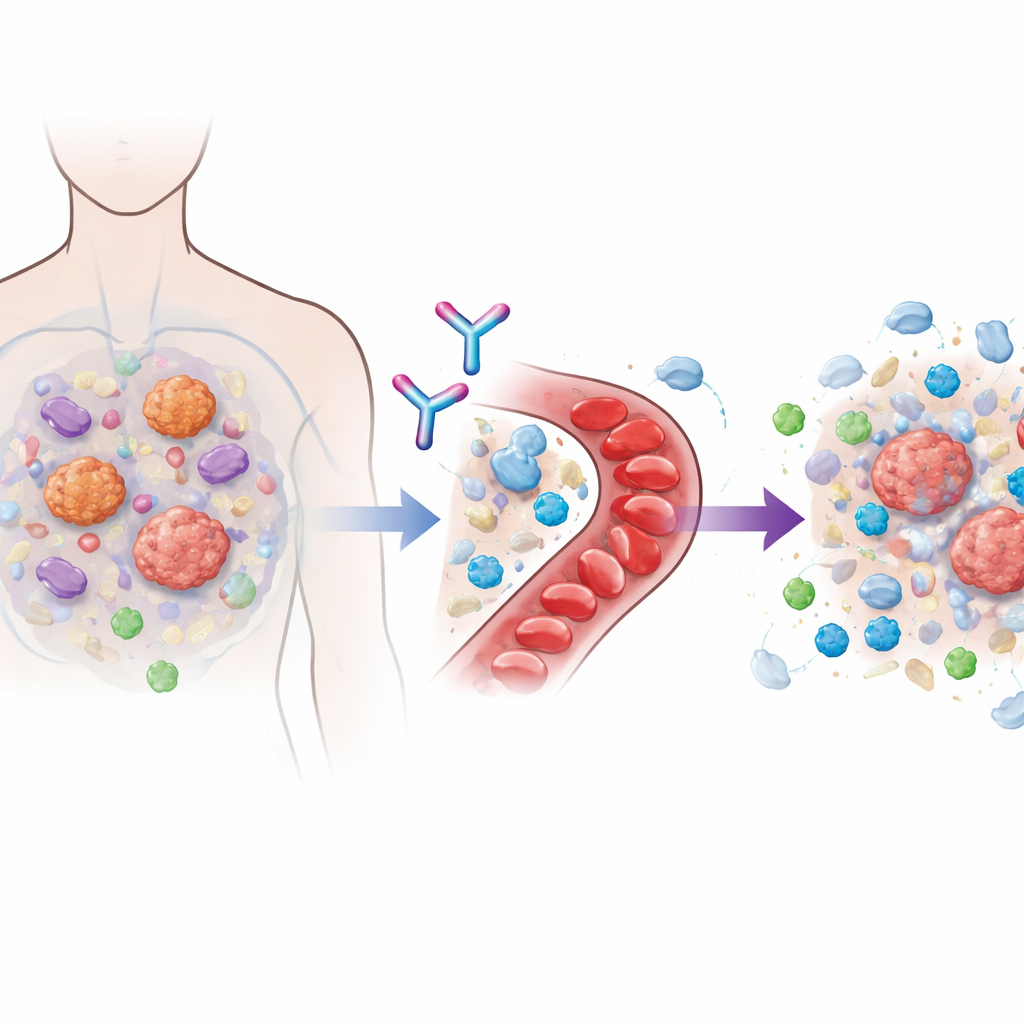
Muchos fármacos modernos de inmunoterapia actúan bloqueando las llamadas moléculas de punto de control, como PD‑1, que normalmente restringen a las células T. Cuando se liberan estos frenos, las células inmunitarias pueden atacar el cáncer con más fuerza. Pero los tumores a menudo se adaptan construyendo un vecindario hostil a su alrededor que mantiene fuera a las células T citotóxicas o las debilita cuando llegan. Un arquitecto clave de esta burbuja protectora es una proteína de señalización llamada TGFβ1, que producen tanto las células cancerosas como las células de soporte cercanas. Intentos anteriores de bloquear toda la familia TGFβ mostraron prometedoras señales pero se toparon con problemas graves en el corazón y en la coagulación, porque otros miembros de la familia son importantes para tejidos sanos. Linavonkibart fue diseñado para sortear este problema neutralizando selectivamente solo la forma latente e inactiva de TGFβ1 antes de que se active, dejando intactas las moléculas estrechamente relacionadas que el organismo necesita.
Diseñando una prueba humana inicial cuidadosa
El ensayo DRAGON fue un estudio multicéntrico de fase 1 realizado en 22 hospitales de Estados Unidos y Corea del Sur. Reclutó a 112 adultos con tumores sólidos avanzados, todos ellos con opciones de tratamiento limitadas. En la primera parte del estudio, linavonkibart se administró solo a dosis crecientes de forma escalonada a pequeños grupos de pacientes, o combinado con su fármaco previo basado en PD‑1. Este enfoque escalonado se usó para mapear la seguridad, cómo se distribuye y persiste el fármaco en el torrente sanguíneo, y para elegir una dosis para su prueba ampliada. En la segunda parte, 78 pacientes cuyos cánceres ya habían resistido al menos un ciclo de inmunoterapia con PD‑1 recibieron una dosis fija de linavonkibart junto con pembrolizumab. Estos pacientes presentaban cánceres difíciles de tratar, incluidos carcinoma de células claras de riñón, melanoma, cáncer de cabeza y cuello, cáncer urotelial (vejiga) y cáncer de pulmón, y la mayoría había recibido varios tratamientos previos.
Primero la seguridad: qué les ocurrió a los pacientes
El objetivo principal de este ensayo en fase inicial fue la seguridad, y linavonkibart mostró resultados alentadores en ese aspecto. En todos los niveles de dosis no se alcanzó una dosis máxima tolerada, y no se observaron efectos secundarios limitantes de dosis ni muertes atribuidas al fármaco. Cuando linavonkibart se combinó con pembrolizumab en la dosis de fase 2, aproximadamente tres cuartas partes de los pacientes experimentaron algún efecto adverso relacionado con el tratamiento, similar a lo que suele observarse con inmunoterapia sola. Erupciones cutáneas y prurito fueron los problemas adicionales más frecuentes, y un pequeño número de pacientes desarrolló inflamación más grave de piel o pulmón. De forma importante, no se observó el peligroso exceso de reacción inmunitaria conocido como síndrome de liberación de citocinas, que puede ocurrir con algunos anticuerpos terapéuticos, y el patrón general de seguridad se pareció en gran medida al de pembrolizumab por sí solo.
Indicios de que el sistema inmunitario puede reactivarse
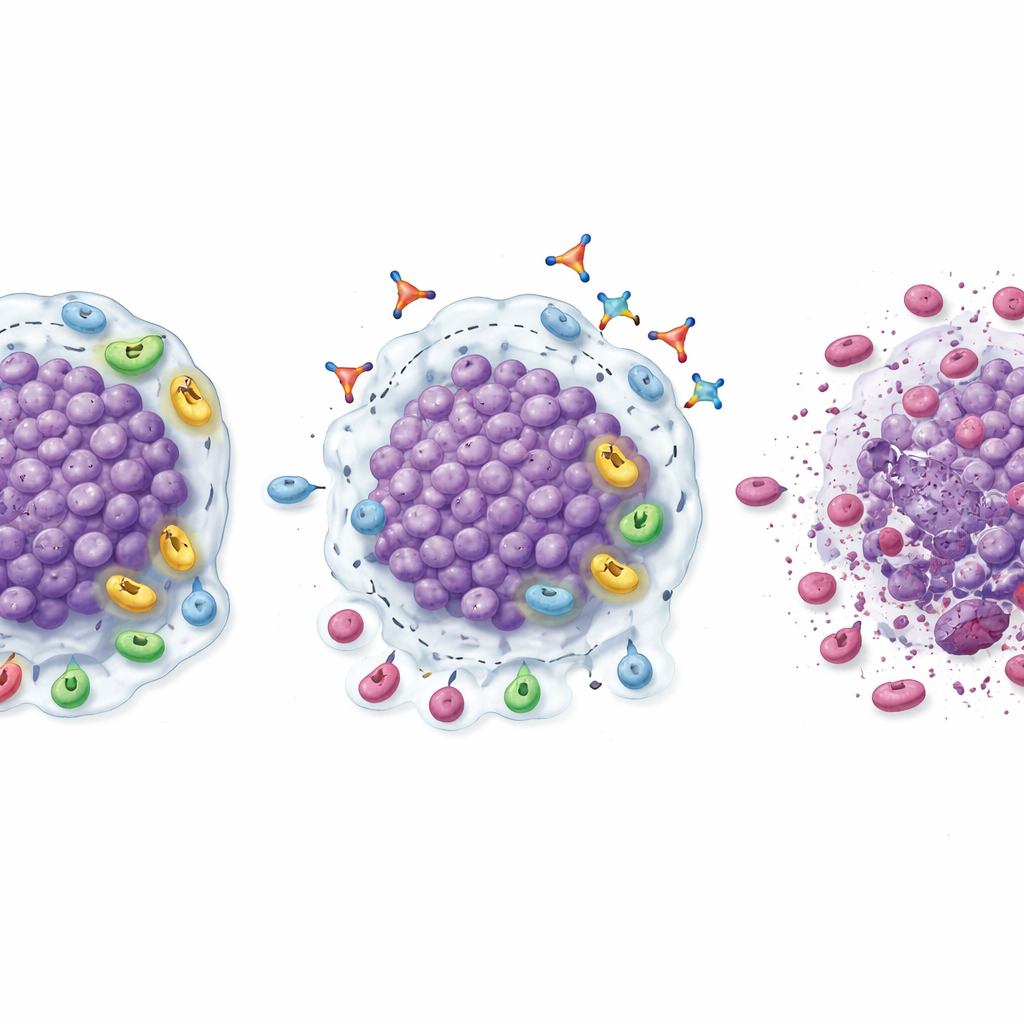
Aunque no fue un ensayo amplio y definitivo de eficacia, varios signos sugirieron que bloquear TGFβ1 podría ayudar a reavivar respuestas al bloqueo de PD‑1. En la fase de expansión, la combinación linavonkibart–pembrolizumab redujo tumores medibles en una fracción notable de pacientes que previamente habían dejado de beneficiarse de los fármacos anti‑PD‑1. Las tasas de respuesta confirmadas fueron del 20% en carcinoma de células claras de riñón, 18,2% en melanoma y algo más del 9% en cánceres de cabeza y cuello y urotelial, con un paciente con cáncer renal que alcanzó la desaparición completa de la enfermedad visible. Muchas de estas respuestas duraron varios meses, y los pacientes que respondieron permanecieron en la combinación por un tiempo mucho mayor que con su terapia previa basada en PD‑1. Las biopsias tomadas antes y después del tratamiento ofrecieron una explicación biológica: los tumores mostraron mayor infiltración de células T CD8 «asesinas», niveles más altos de células T activadas, menos células T reguladoras y células mieloides supresoras, y un cambio global hacia un microambiente más inflamado y preparado para el ataque.
Identificando quién podría beneficiarse más
Los investigadores también exploraron qué pacientes podrían tener más probabilidad de responder. En el carcinoma de células claras de riñón, los tumores que ya contenían muchas células T CD8 al inicio —pero que además eran ricos en células T reguladoras y expresaban altos niveles de TGFβ1— tenían más probabilidades de reducirse con la terapia combinada. En estos pacientes, las tasas de respuesta y la supervivencia libre de progresión fueron sustancialmente mayores que en el grupo renal más amplio. Este patrón sugiere un "punto óptimo": tumores que tienen muchos soldados inmunitarios presentes pero están contenidos por una supresión impulsada por TGFβ1 pueden ser candidatos ideales para linavonkibart más bloqueo de PD‑1. Si se valida en estudios mayores, pruebas de tejido sencillas para estos marcadores podrían ayudar a los médicos a seleccionar a los pacientes con mayor probabilidad de beneficiarse.
Qué significa este trabajo de cara al futuro
Para las personas con cánceres avanzados que ya han resistido la inmunoterapia, la posibilidad de reactivar su propio sistema inmunitario sin añadir toxicidad grave resulta atractiva. Este ensayo de primera administración en humanos aporta evidencia temprana de que deshabilitar selectivamente el escudo TGFβ1 con linavonkibart puede hacerse de forma segura y quizá restaurar un control tumoral significativo cuando se combina con un inhibidor de PD‑1, particularmente en ciertos cánceres renales. Aunque el estudio fue pequeño y no aleatorizado, su historial de seguridad, las lecturas biológicas y las respuestas duraderas constituyen un argumento sólido para ensayos de fase 2 más amplios. Si estudios futuros confirman estos hallazgos, este enfoque podría ampliar el círculo de pacientes que pueden beneficiarse de la inmunoterapia, convirtiendo algunos cánceres hoy obstinados en otros que vuelven a ser vulnerables a las defensas del propio organismo.
Cita: Yap, T.A., Sweis, R.F., Vaishampayan, U. et al. Linavonkibart and pembrolizumab in immune checkpoint blockade-resistant advanced solid tumors: a phase 1 trial. Nat Med 32, 992–1001 (2026). https://doi.org/10.1038/s41591-025-04157-w
Palabras clave: inmunoterapia contra el cáncer, inhibición de TGFβ1, resistencia a inhibidores de puntos de control inmunitario, carcinoma de células claras del riñón, microambiente tumoral