Clear Sky Science · es
Dexametasona adyuvante estratificada por genotipo para meningitis tuberculosa en adultos VIH-negativos: un ensayo aleatorizado de fase 3
Por qué importa este estudio sobre una infección cerebral
La meningitis tuberculosa es la forma más letal de la tuberculosis, que ataca el cerebro y sus membranas protectoras. Los médicos de todo el mundo añaden de forma habitual un potente fármaco antiinflamatorio, la dexametasona, al tratamiento antituberculoso con la esperanza de salvar más vidas. Sin embargo, su beneficio ha sido modesto y desigual, lo que plantea una pregunta urgente: ¿podemos usar los genes de una persona para decidir quién realmente necesita este medicamento y quién podría prescindir de él con seguridad? Este amplio ensayo en Vietnam se propuso poner a prueba esa idea de forma directa.
Una infección peligrosa del cerebro
La meningitis tuberculosa comienza cuando las bacterias de la tuberculosis se diseminan desde los pulmones hacia el cerebro. A medida que el sistema inmune reacciona, se acumulan inflamación e hinchazón alrededor del encéfalo y la médula espinal, provocando dolor de cabeza, fiebre, confusión y, sin tratamiento, con frecuencia la muerte. La atención estándar combina meses de antibióticos para matar las bacterias con esteroides para calmar la inflamación dañina. Estudios previos mostraron que la dexametasona reducía ligeramente las muertes en general, pero no en todos los subgrupos de pacientes, lo que dejaba incertidumbre sobre cuándo realmente resulta útil.
Una pista genética sobre la respuesta a esteroides
Trabajos anteriores apuntaron a un gen llamado LTA4H, que contribuye a controlar la intensidad de la respuesta inmune durante la tuberculosis. Las personas heredan distintas versiones, o genotipos, de este gen, etiquetadas como CC, CT y TT. Estudios pequeños previos sugirieron que los pacientes con el tipo TT tenían una reacción inflamatoria muy intensa pero obtenían un beneficio claro de la dexametasona, mientras que aquellos con genotipos CC o CT podrían no beneficiarse e, incluso, en algunos casos, verse perjudicados. Si esto fuera cierto, los médicos podrían adaptar el uso de esteroides basándose en una prueba genética rápida en la cabecera del paciente.
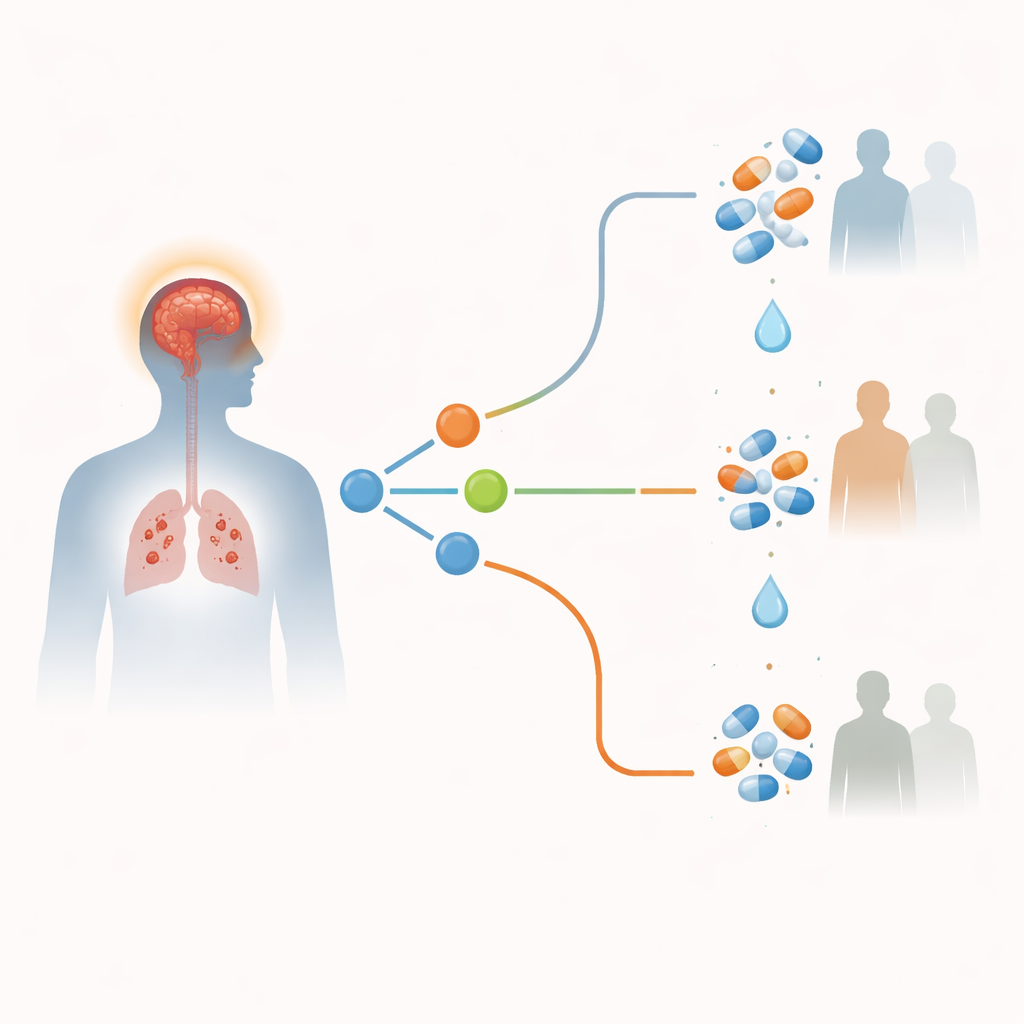
Un ensayo clínico guiado por genotipo
Para someter esta idea a una prueba rigurosa, los investigadores realizaron un amplio ensayo de fase 3 en dos hospitales de Ho Chi Minh. Reclutaron a 720 adultos con sospecha de meningitis tuberculosa que no tenían VIH. Todos recibieron los antibióticos estándar contra la tuberculosis. Tras una prueba sanguínea rápida para determinar su genotipo de LTA4H, 613 pacientes con los genotipos comunes CC o CT fueron asignados aleatoriamente para recibir dexametasona o un placebo a juego durante 6–8 semanas. Debido a que datos anteriores sugerían un fuerte beneficio, los 89 pacientes con el raro genotipo TT recibieron dexametasona a etiqueta abierta y no fueron aleatorizados. El resultado principal fue si los pacientes murieron o desarrollaron un nuevo problema cerebral grave, como una caída importante del nivel de conciencia o nueva parálisis, dentro de los 12 meses.
Qué encontró el ensayo
Entre los pacientes CC y CT, los resultados fueron notablemente similares tanto si recibieron dexametasona como si no. Aproximadamente uno de cada tres pacientes en cada grupo murió o sufrió un nuevo evento cerebral grave en el plazo de un año. Los análisis estadísticos no pudieron demostrar que omitir la dexametasona fuera “no peor” que usarla, pero tampoco mostraron que la dexametasona mejorara claramente la supervivencia o la discapacidad en estos genotipos. Los efectos adversos graves —como infecciones severas o hemorragias— fueron aproximadamente igual de frecuentes con dexametasona y placebo, lo que sugiere que el fármaco fue en general seguro en este contexto. Los pacientes TT, que todos recibieron dexametasona, tuvieron resultados comparables a los de los otros grupos en términos generales, aunque hubo indicios de que podrían evolucionar mejor que otros cuando su enfermedad era muy grave.
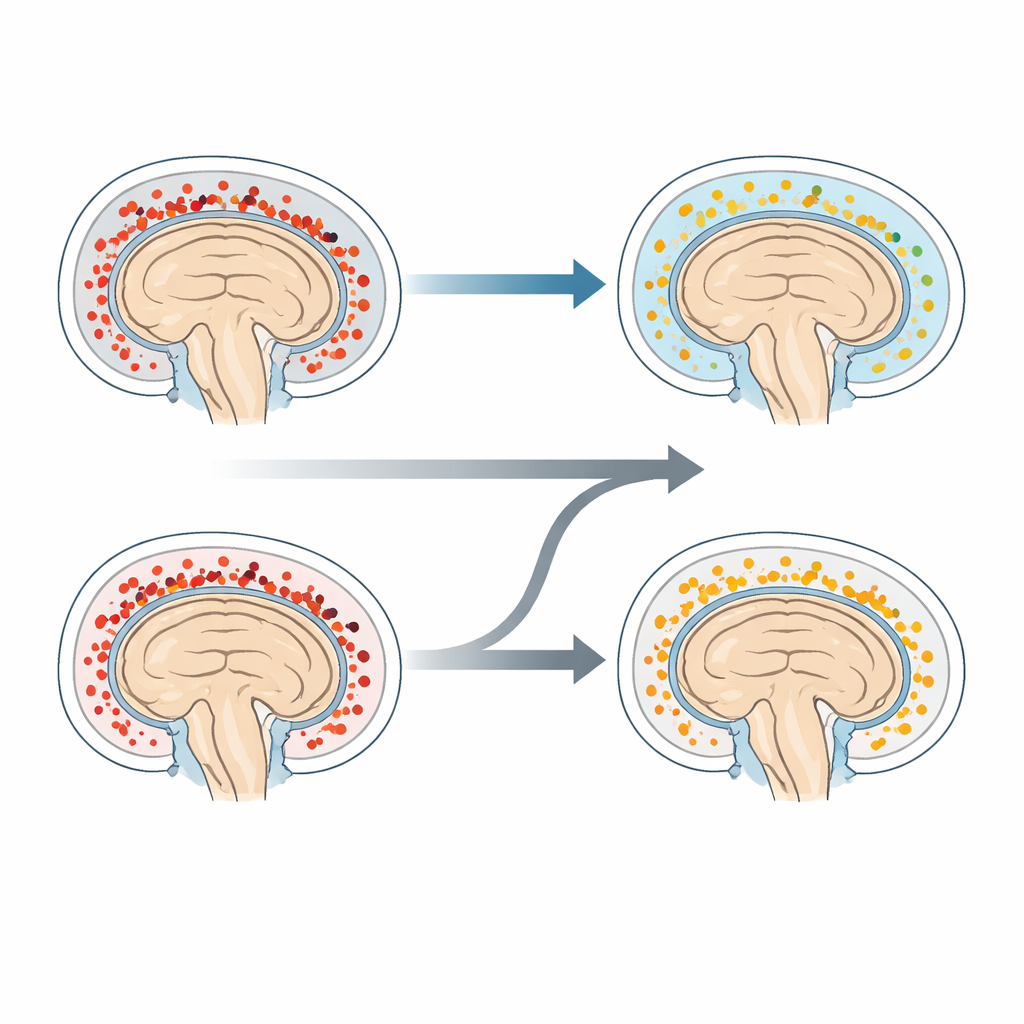
Observando la respuesta inmune en el cerebro
El equipo también examinó muestras de líquido cefalorraquídeo y sangre para ver cómo la dexametasona y el genotipo de LTA4H modulaban la inflamación. La dexametasona redujo claramente varias proteínas inflamatorias y vías inmunes en el líquido cefalorraquídeo de los pacientes CC, y en menor medida en los CT, durante el primer mes de tratamiento. En la sangre, no obstante, los cambios inducidos por el esteroide fueron más evidentes principalmente en los pacientes CT. A pesar de estos cambios medibles, no se encontró un patrón simple que vinculase la magnitud de la respuesta inflamatoria con quién vivió o murió, lo que subraya la complejidad de la enfermedad.
Qué significa esto para los pacientes hoy
Cuando los investigadores combinaron los datos de este ensayo con un estudio vietnamita anterior del mismo régimen de esteroide, encontraron que la dexametasona redujo modestamente las muertes totales en adultos VIH-negativos con meningitis tuberculosa. En conjunto, los resultados apoyan la continuidad del uso de dexametasona en estos pacientes, independientemente de su genotipo LTA4H. Al mismo tiempo, la esperada regla genética simple —administrar esteroides solo a pacientes TT y evitarlos en los demás— no se confirmó. El trabajo muestra que nuestra respuesta inmune a la tuberculosis cerebral está gobernada por muchos factores, no solo un gen, y que se necesitan tratamientos antiinflamatorios nuevos y más selectivos. Por ahora, el diagnóstico precoz, los antibióticos rápidos y la dexametasona estándar siguen siendo la estrategia mejor probada para mejorar la supervivencia en esta enfermedad devastadora.
Cita: Donovan, J., Duc Bang, N., Dong, H.K.T. et al. Genotype-stratified adjunctive dexamethasone for tuberculous meningitis in HIV-negative adults: a randomized controlled phase 3 trial. Nat Med 32, 849–858 (2026). https://doi.org/10.1038/s41591-025-04138-z
Palabras clave: meningitis tuberculosa, dexametasona, genética del hospedador, neuroinflamación, ensayo clínico