Clear Sky Science · es
Mapa interpretable de la inflamación en las células inmunitarias circulantes
Por qué la inflamación en la sangre te importa
La inflamación está en el centro de muchas enfermedades, desde la artritis y el asma hasta la COVID-19 y el cáncer. Aun así, los médicos siguen teniendo dificultades para interpretar las señales inflamatorias del organismo de forma que expliquen claramente qué falla y qué tratamiento será más eficaz. Este estudio construye un enorme “mapa” de las células inmunitarias que circulan en la sangre y muestra cómo estas células podrían actuar como biomarcadores vivos y fácilmente muestreables para clasificar una amplia gama de enfermedades inflamatorias.
Construyendo un gran mapa de células inmunitarias
Para cartografiar este paisaje, los investigadores analizaron más de 6,5 millones de células inmunitarias tomadas de la sangre de 1.047 personas. Estos voluntarios comprendían 19 condiciones, incluidas enfermedades autoinmunes como el lupus y la artritis reumatoide, enfermedades pulmonares crónicas como el asma y la EPOC, infecciones como la COVID-19 y el VIH, y varios cánceres, junto con donantes sanos. Mediante secuenciación de ARN unicelular midieron qué genes estaban activados en cada célula individual y luego usaron métodos estadísticos avanzados para corregir diferencias técnicas entre estudios y agrupar las células en 64 estados inmunitarios distintos. Este “Atlas de la Inflamación” captura tanto protagonistas conocidos —como células T, células B y monocitos— como subtipos más especializados que cambian con la enfermedad.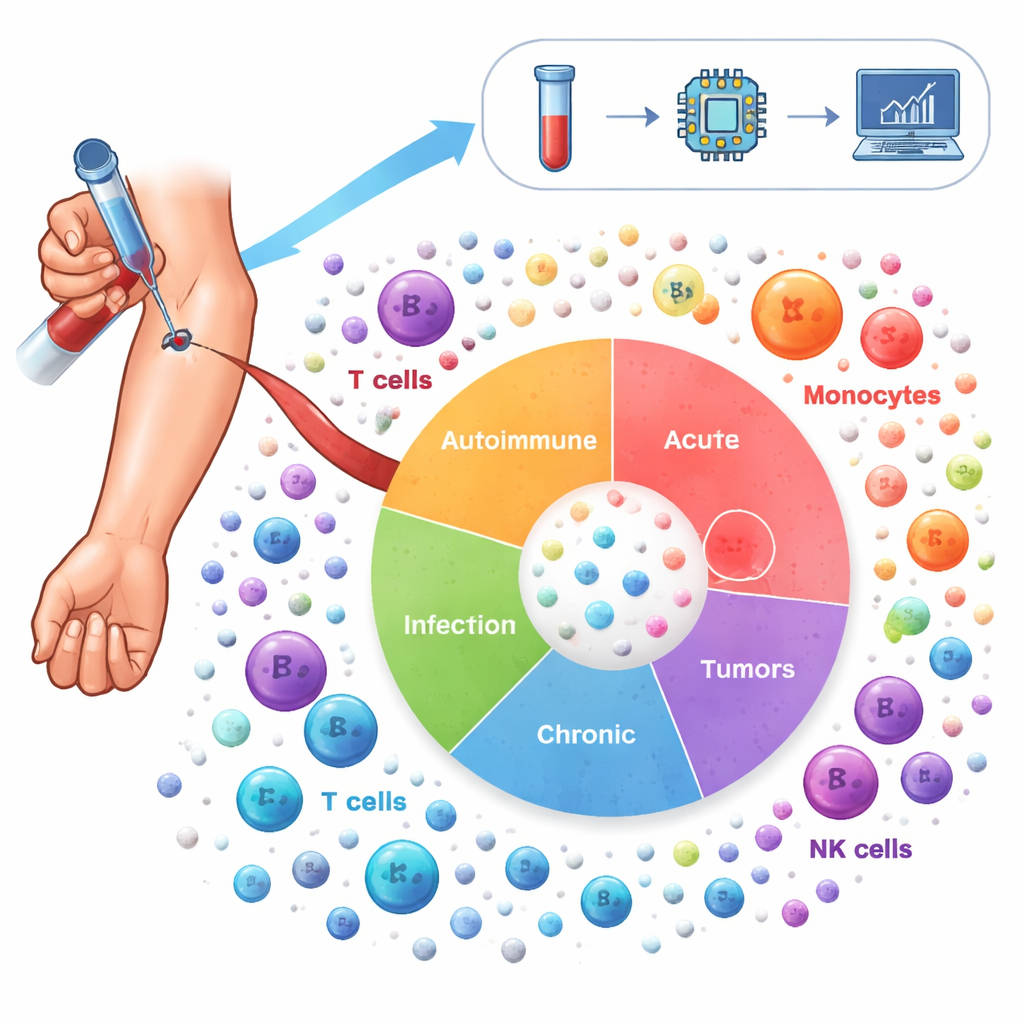
Interpretando las firmas inflamatorias del cuerpo
El equipo se centró a continuación en genes que controlan cómo se activan las células inmunitarias, cómo se desplazan por el organismo, cómo presentan antígenos y cómo responden a moléculas señalizadoras como los interferones y el factor de necrosis tumoral. Agruparon estos genes en 21 “firmas” biológicas y las refinaron para cada tipo celular principal. Al comparar pacientes con donantes sanos, pudieron ver qué firmas estaban aumentadas o disminuidas en distintas enfermedades. Por ejemplo, muchas enfermedades inflamatorias mediadas por el sistema inmune mostraron mayor actividad de moléculas de adhesión y maquinaria de presentación de antígenos, mientras que las respuestas a interferones estaban deprimidas en la mayoría de los tipos celulares pero aumentadas en ciertos linfocitos T CD8. Infecciones virales como la gripe y la COVID-19 potenciaron los programas inducidos por interferón, mientras que infecciones crónicas como el VIH y la hepatitis B los debilitaban.
Profundizando en genes clave y interruptores de control
Puesto que las firmas amplias aún ocultan detalles importantes, los investigadores examinaron genes individuales y sus reguladores. En células T CD8 no naïvas encontraron que dos genes, FGFBP2 y GZMB, estaban especialmente activos en subtipos de memoria efectora concretos, particularmente en la colitis ulcerosa. Estos genes se han vinculado con daños en las superficies epiteliales, y su señal intensa en sangre sugiere que estas células agresivas ya están preparadas antes de entrar en los tejidos. Un análisis separado de redes de regulación génica destacó dos factores de transcripción, STAT1 y SP1, como controladores centrales de los programas inducidos por interferón. Sus patrones de actividad difirieron entre enfermedades y tipos celulares —por ejemplo, comportamiento opuesto en monocitos frente a células T CD8 en el lupus, y cambios entre fases de brote y no brote— lo que insinúa cómo las mismas vías pueden ser protectoras en un contexto y perjudiciales en otro.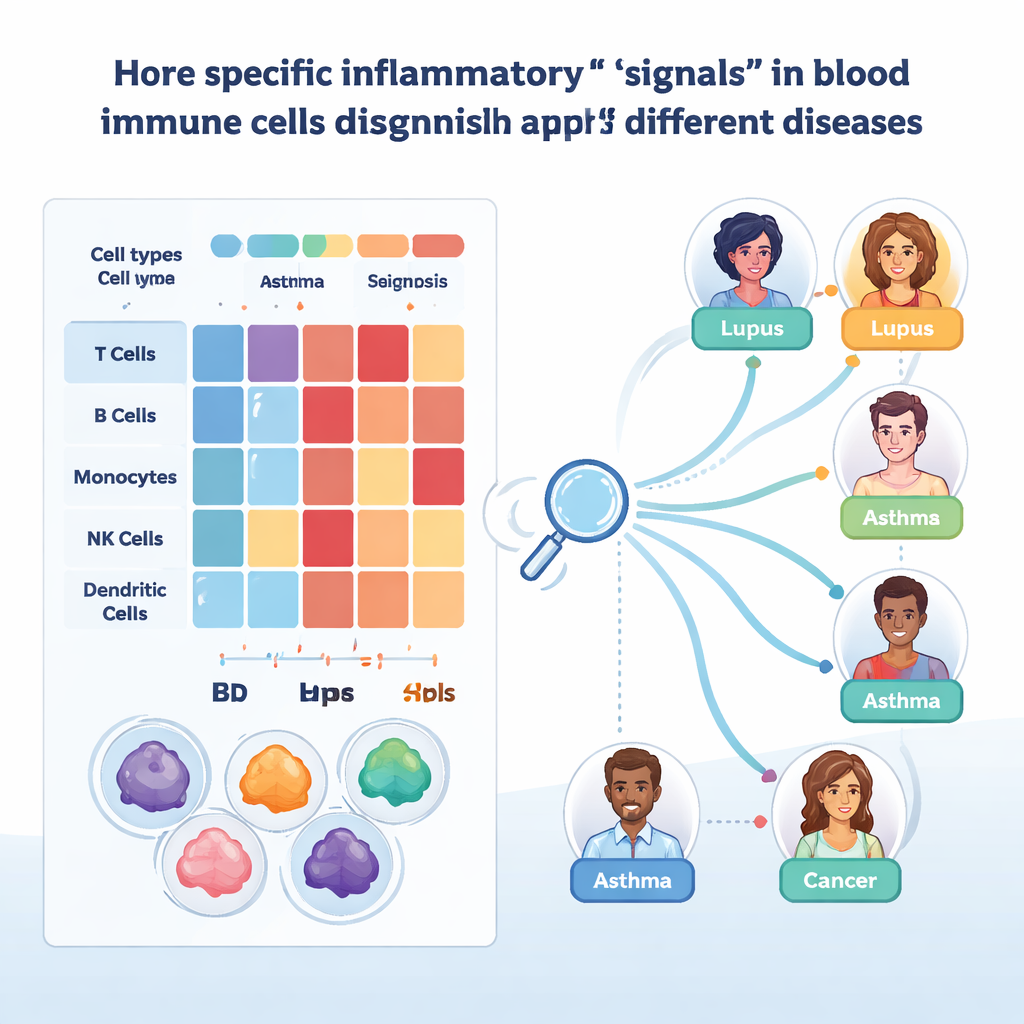
Entrenando máquinas para detectar enfermedades a partir de células sanguíneas
Para convertir este atlas en una herramienta práctica, el equipo aplicó aprendizaje automático interpretable. Entrenaron modelos de árboles de decisión con impulso por gradiente por separado para cada tipo celular principal, pidiendo a los algoritmos que etiquetaran cada célula con la enfermedad correcta según su expresión génica. Estos modelos alcanzaron alta precisión cuando se probaron con muestras reservadas, especialmente tras corregir las diferencias técnicas. Usando SHAP, un método que explica qué genes impulsan cada decisión, los investigadores pudieron identificar biomarcadores candidatos. Un ejemplo es CYBA en monocitos, cuyos niveles ayudaron a distinguir enfermedades cutáneas como la psoriasis de la inflamación intestinal en la enfermedad de Crohn y la colitis ulcerosa. Otro es IFITM1 en ciertos linfocitos T y células linfoides innatas, que separa el asma de la EPOC y sugiere patrones distintos de defensa antiviral crónica.
Hacia una brújula diagnóstica basada en la sangre
Finalmente, los autores se preguntaron si era posible clasificar a pacientes enteros —no solo células individuales— a partir de sus perfiles inmunitarios circulantes. Proyectaron los datos de cada célula en un espacio de “incrustación” comprimido, promediaron esas incrustaciones por tipo celular para cada paciente y entrenaron clasificadores para predecir la enfermedad. Cuando los pacientes nuevos se parecían a los del conjunto de entrenamiento, el rendimiento fue excelente. Pero cuando las muestras procedían de estudios completamente independientes que usaban métodos de laboratorio diferentes, la precisión cayó abruptamente, revelando la sensibilidad de estas herramientas a la variabilidad técnica. Un conjunto de datos más controlado y “centralizado”, generado en un único centro con una sola química de secuenciación, recuperó gran parte del rendimiento, lo que apunta a la necesidad de protocolos estandarizados o conjuntos de entrenamiento muy grandes y diversos.
Qué significa esto para el diagnóstico y el tratamiento futuros
Para un lector no especializado, el mensaje clave es que tus células inmunitarias circulantes llevan una huella rica de cómo está inflamada tu organismo. Leyendo estas huellas célula por célula, este trabajo demuestra que es posible distinguir entre muchas enfermedades, descubrir genes que pueden impulsar síntomas específicos y comenzar a construir pruebas sanguíneas universales que clasifiquen enfermedades inflamatorias. El estudio aún no es una prueba clínica lista para usar —las diferencias técnicas entre estudios siguen limitando la fiabilidad— pero sienta las bases para futuras herramientas de “biopsia líquida” que podrían ayudar a los médicos a identificar el diagnóstico y el tratamiento adecuados antes, mediante una extracción de sangre sencilla.
Cita: Jiménez-Gracia, L., Maspero, D., Aguilar-Fernández, S. et al. Interpretable inflammation landscape of circulating immune cells. Nat Med 32, 633–644 (2026). https://doi.org/10.1038/s41591-025-04126-3
Palabras clave: inflamación, células inmunitarias, secuenciación de ARN unicelular, biomarcadores, aprendizaje automático