Clear Sky Science · es
CD38 confiere a las células Treg específicas de antígeno locales resistencia al estrés para el control de la inflamación compartimentada del SNC
Por qué importan las células inmunitarias que protegen el cerebro
Muchas enfermedades autoinmunes del cerebro, como la esclerosis múltiple, se comportan como incendios latentes: una llamarada inicial de inflamación se apaga, pero el daño puede reactivarse años después. Este estudio plantea una pregunta aparentemente sencilla con grandes implicaciones: tras un ataque en el sistema nervioso central (SNC), ¿qué mantiene la paz y qué hace que vuelva la enfermedad? Los autores se centran en una pequeña población de células inmunitarias llamadas células T reguladoras que se aposentan en el cerebro y la médula espinal tras la inflamación, y revelan cómo una única molécula de superficie las equipa para sobrevivir en un entorno hostil y prevenir recaídas.
Los pacificadores inmunitarios que permanecen
Usando un modelo murino que imita aspectos de la esclerosis múltiple, los investigadores rastrearon distintos tipos de células T a medida que la enfermedad alcanzaba su pico y luego entraba en fase de recuperación. Mientras que las células T auxiliares convencionales que impulsan la inflamación disminuían conforme mejoraban los síntomas, las células T reguladoras —células especializadas que normalmente amortiguan las respuestas inmunitarias— permanecían en el SNC. Su proporción dentro del conjunto local de células T aumentó en realidad, y se agruparon en nichos distintivos alrededor de los espacios de líquido cerebral y las membranas protectoras que recubren el cerebro. Marcando el origen de las células T entrantes, el equipo mostró que, tras la recuperación, muy pocas células T reguladoras nuevas llegaban desde los ganglios linfáticos. En cambio, la población del SNC se mantenía en gran medida de forma local, lo que sugiere una fuerza residente de “mantenimiento de la paz” a largo plazo. 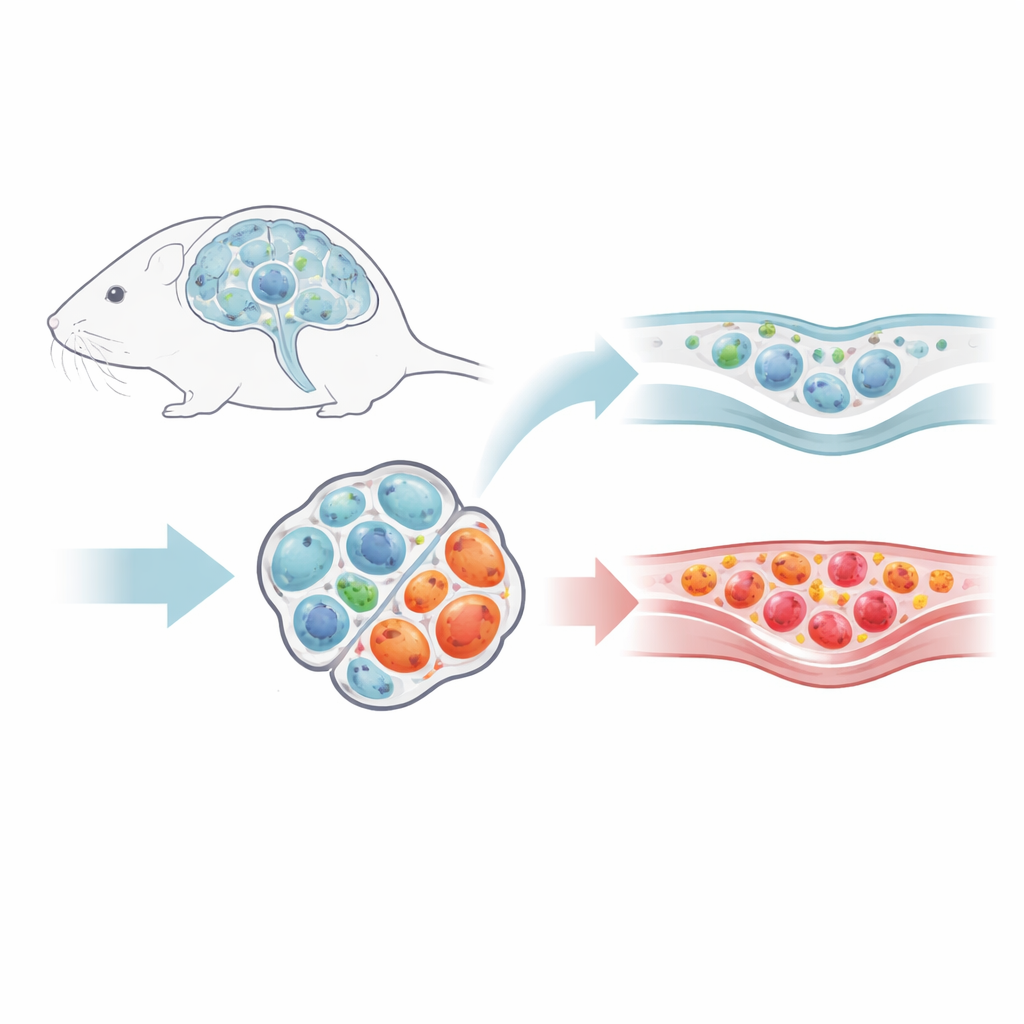
Guardianes tolerantes al estrés en un nicho hostil
El SNC postinflamatorio dista mucho de ser un entorno confortable para estos guardianes. Tras la oleada principal de la enfermedad, los niveles de la señal de crecimiento interleucina-2 (IL-2) —de la que las células T reguladoras dependen en gran medida— caen porque la mayoría de las células T convencionales se han retirado. Al mismo tiempo, el tejido es rico en la molécula metabólica NAD+, que puede desencadenar la muerte celular o atenuar receptores clave de la superficie cuando es modificada por una enzima específica. Mediante el etiquetado genético y el seguimiento de células T reguladoras individuales, los autores distinguieron células “estables” que mantuvieron su identidad de otras “inestables” que perdieron su programa característico Foxp3. Las células estables mostraron una firma mucho más fuerte de señalización por IL-2 y niveles más altos de receptores de IL-2, lo que sugiere que la capacidad de detectar cantidades escasas de IL-2 es central para sobrevivir en este entorno estresado.
Control local de las recaídas desde dentro del cerebro
Para comprobar si estas células T reguladoras residentes son realmente importantes para el control a largo plazo de la enfermedad, los investigadores las eliminaron selectivamente del SNC usando una toxina administrada directamente en el líquido cerebral, manteniendo intactas la mayoría de las células T reguladoras sistémicas en el resto del cuerpo. En cuestión de días, los ratones que se estaban recuperando desarrollaron recaídas graves con parálisis renovada. En contraste, agotar las células T reguladoras solo en el cuerpo, preservando las del SNC, no desencadenó brotes. La recaída implicó la rápida reactivación y expansión de células T efectoras que ya estaban alojadas en el SNC, incluso cuando se bloqueó su reclutamiento desde la sangre. Esto demuestra que las células T reguladoras locales, más que las circulantes, son esenciales para contener las células agresivas residuales que permanecen tras el paso del ataque agudo.
Cómo una enzima protege a las células reguladoras
Indagando más, los autores buscaron moléculas que distingan a las células T reguladoras tolerantes al estrés en el SNC. Surgió un actor clave: CD38, una enzima en la superficie celular que degrada el NAD+ extracelular. En el SNC inflamado, las células T reguladoras aumentaron fuertemente CD38, mientras que las células T convencionales no mostraron un cambio tan marcado. Cuando el equipo transfirió células T reguladoras reactivas al mielina carentes de CD38 en ratones, esas células alcanzaron el SNC pero no lograron controlar la enfermedad, a diferencia de sus homólogas normales. En animales quiméricos mixtos, donde solo las células T reguladoras residentes eran deficientes en CD38, eliminar la fracción competente en CD38 fue suficiente para provocar recaídas, mostrando que CD38 actúa de forma intrínseca a la célula para permitir un control efectivo.
Protegiendo la señal vital
Experimentos mecanísticos revelaron cómo CD38 confiere esta resistencia. Los altos niveles de NAD+ en el SNC pueden alimentar la modificación química de proteínas de superficie por la enzima ARTC2.2. Un blanco sensible es la subunidad de alta afinidad del receptor de IL-2, que las células T reguladoras expresan a niveles muy elevados, especialmente cuando reconocen antígenos cerebrales. En células T reguladoras deficientes en CD38 expuestas a NAD+, la mayoría de los receptores de IL-2 resultaron modificados, lo que condujo a una activación más débil del mensajero STAT5 y a una menor respuesta a la IL-2. En contraste, las células que expresan CD38 redujeron localmente el NAD+ a su alrededor, limitando esta modificación dañina y preservando una señalización fuerte por IL-2. En ratones vivos, inyectar NAD+ en el cerebro eliminó selectivamente a la mayoría de las células T reguladoras mediante esta vía, mientras preservaba a las células T convencionales, subrayando lo precario que es el nicho sin esta enzima protectora. 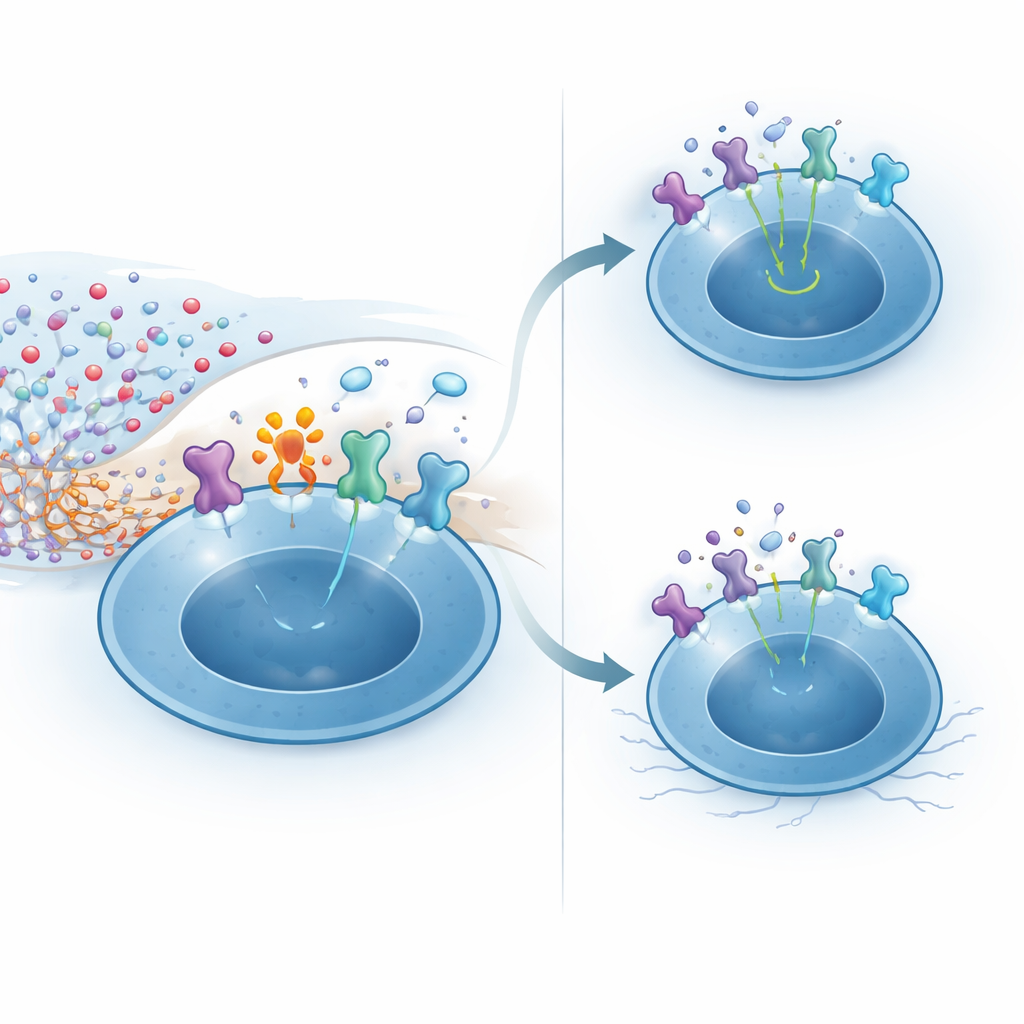
Qué significa esto para la autoinmunidad cerebral crónica
Este trabajo dibuja un panorama de la autoinmunidad crónica del SNC como una batalla compartimentada: pequeños racimos de células T agresivas residuales residen en el cerebro y la médula espinal, contenidas por células T reguladoras locales igualmente especializadas. Estos guardianes son “tolerantes al estrés” porque CD38 les permite sobrevivir a niveles elevados de NAD+ y seguir detectando cantidades mínimas de IL-2, preservando su identidad y su función supresora. Para el lector no especializado, la conclusión clave es que el control a largo plazo de enfermedades como la esclerosis múltiple puede depender menos del sistema inmunitario circulante y más de nutrir y proteger a estos pacificadores residentes dentro del cerebro mismo, potencialmente apuntando a vías que mejoren la función de CD38 o la sensibilidad a IL-2 en las células T reguladoras.
Cita: Chen, HH., Tyystjärvi, S., Ruiz Navarro, D. et al. CD38 endows local antigen-specific Treg cells with stress resilience for control of compartmentalized CNS inflammation. Nat Immunol 27, 516–529 (2026). https://doi.org/10.1038/s41590-025-02416-z
Palabras clave: células T reguladoras, esclerosis múltiple, inflamación del sistema nervioso central, enzima CD38, tolerancia inmunitaria