Clear Sky Science · es
El patrón espacial de la señalización TGFβ en fibroblastos subyace a la resistencia al tratamiento en la artritis reumatoide
Por qué importa el dolor articular persistente
Mucha gente con artritis reumatoide toma medicamentos modernos que calman el sistema inmunitario, pero sus articulaciones siguen doliendo y rígidas. Este estudio pregunta por qué algunos pacientes no mejoran incluso cuando la inflamación en la articulación parece remitir. Al examinar con detalle dónde y cómo ciertas células de soporte en la articulación activan programas de cicatrización, los investigadores identifican una forma oculta de daño que podría explicar el dolor continuo y apuntar a nuevas estrategias terapéuticas.
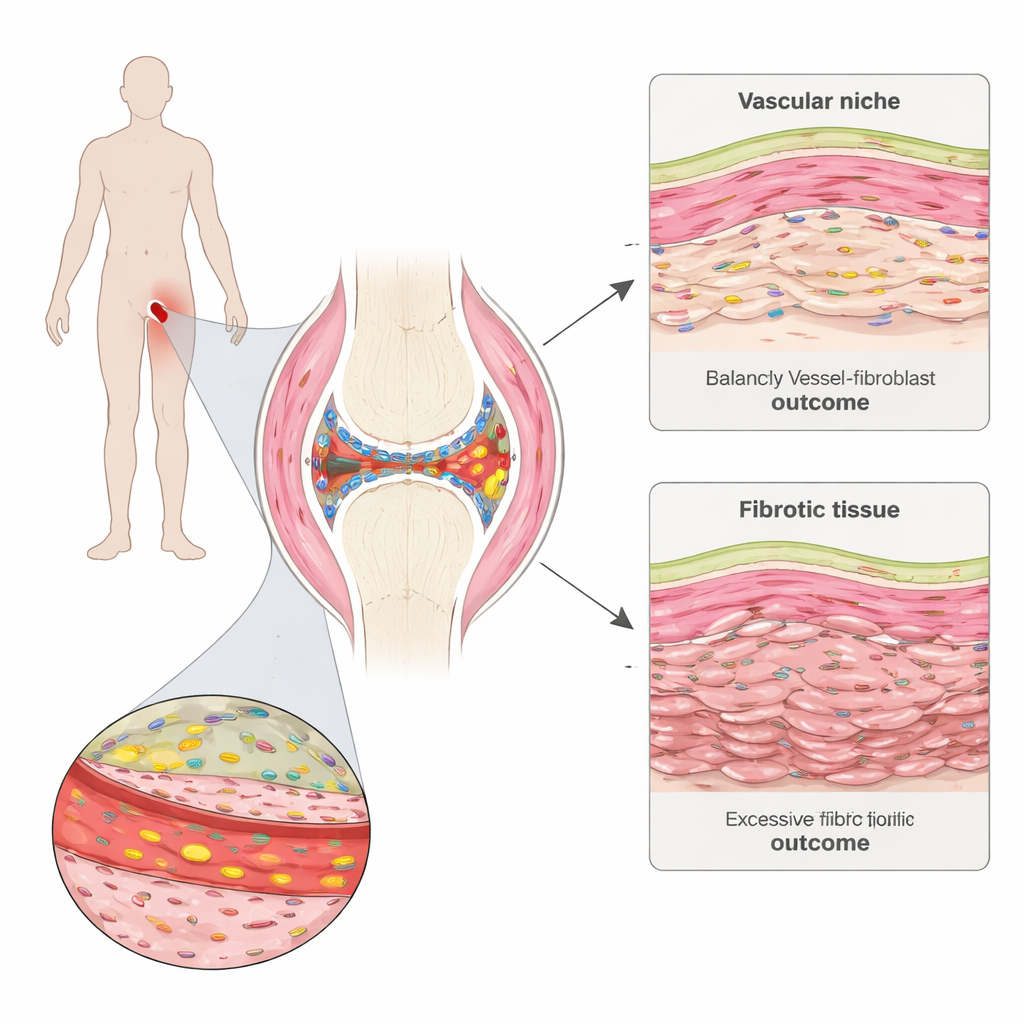
Una mirada más cercana dentro de la articulación dolorida
La artritis reumatoide ataca la sinovia, un tejido delgado que recubre y lubrica las articulaciones. El equipo tomó pequeñas biopsias sinoviales de personas con enfermedad temprana antes de iniciar el tratamiento y de nuevo seis meses después. Usando mapeo espacial avanzado de la expresión génica, pudieron ver qué genes estaban activos en miles de células individuales preservando la posición de esas células en el tejido. Identificaron “vecindarios” distintos en la sinovia, incluidos cúmulos de células inmunes, zonas ricas en grasa, el delgado revestimiento interno y regiones densas en vasos sanguíneos y células estructurales llamadas fibroblastos.
Células formadoras de cicatrices y resistencia al tratamiento
Al comparar a los pacientes que después alcanzaron remisión con los que no, los investigadores hallaron un patrón llamativo: antes del tratamiento, los pacientes que no remitieron ya mostraban señales más intensas de cicatrización tisular, o fibrosis. Un programa fibroblástico particular, marcado por alta producción de una proteína de la matriz extracelular llamada COMP, estaba ampliado en estos pacientes. Estos fibroblastos ricos en COMP compartían características con las células formadoras de cicatrices observadas en la fibrosis pulmonar y cutánea y se relacionaban de forma más firme con una mala respuesta al tratamiento. Con el tiempo, las regiones dominadas por estas células tendían a volverse densamente rellenadas con tejido conectivo pero relativamente pobres en células, lo que sugiere que depositan una matriz rígida que puede persistir incluso después de que la inflamación disminuya.
Los vasos sanguíneos como conductores ocultos
Los fibroblastos fibrogénicos no estaban dispersos al azar. Se agrupaban alrededor de los vasos sanguíneos, formando zonas peri‑vasculares estratificadas. La capa más interna, pegada a la pared del vaso, expresaba genes distintos de los de la capa exterior. El equipo demostró que las células que recubren los vasos envían señales Notch a los fibroblastos cercanos, que a su vez modulan cómo estos responden a una familia de señales pro‑cicatrización conocidas como TGF‑beta. Cerca del vaso, la señalización Notch empuja a los fibroblastos a producir TGF‑beta pero al mismo tiempo reduce el número de receptores de TGF‑beta en su superficie, limitando su sensibilidad. A mayor distancia, donde la influencia de Notch disminuye, los fibroblastos presentan más receptores y se vuelven muy responsivos, transformándose en células ricas en COMP que impulsan la fibrosis.
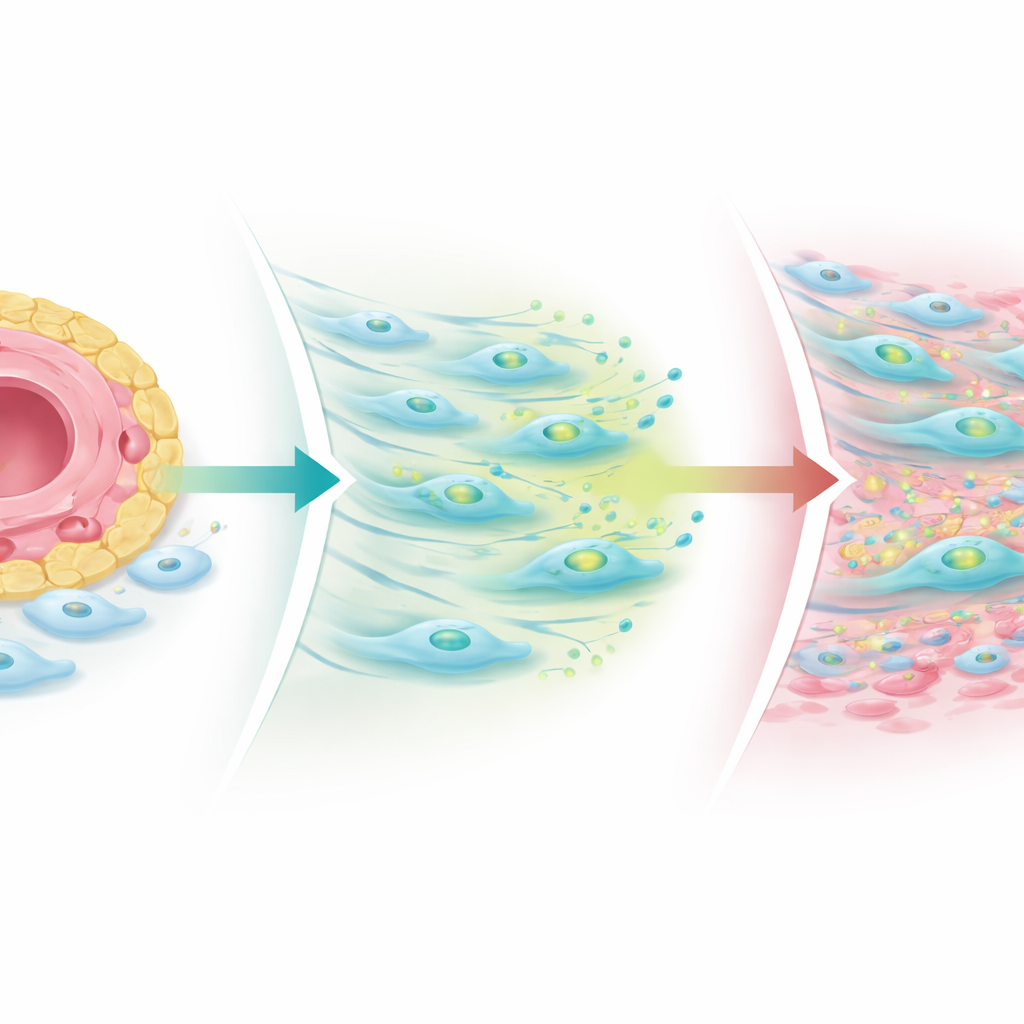
Qué ocurre cuando se rompe el equilibrio
Los investigadores construyeron modelos articulares simplificados en placas de laboratorio y organoides tridimensionales hechos con tejido de pacientes para explorar este mecanismo. Cuando reforzaron las señales Notch provenientes de las células endoteliales, los fibroblastos aumentaron la producción de TGF‑beta pero redujeron los niveles de receptores, limitando la cicatrización. Cuando bloquearon Notch o alteraron su patrón estable, los fibroblastos recuperaron receptores de TGF‑beta—especialmente un co‑receptor llamado receptor III de TGF‑beta—y las células fibrogénicas COMP‑positivas se expandieron alejándose de los vasos. En biopsias de pacientes tomadas tras el tratamiento, los cúmulos de células inmunes se redujeron en casi todos, pero los nichos fibrogénicos, en particular las regiones ricas en COMP, a menudo crecieron, sobre todo en aquellos cuyo dolor articular persistió. Esto sugiere que los fármacos antiinflamatorios estándar pueden apagar el “fuego” inmune mientras dejan intacto o incluso revelan un proceso de cicatrización que mantiene las articulaciones rígidas y dolorosas.
Nuevas formas de calmar las articulaciones rebeldes
Finalmente, el equipo probó si interrumpir este circuito fibrogénico podría tener utilidad terapéutica. En organoides derivados de pacientes, fármacos que inhiben Notch o bloquean la señalización de TGF‑beta redujeron la producción de COMP, de otras proteínas asociadas a la cicatriz y de colágenos clave, y reconfiguraron la actividad génica en las zonas perivasculares. Para un observador no especializado, el mensaje es que no todo el daño de la artritis reumatoide procede de la inflamación visible: parte está “codificado” en las células de soporte de la articulación y en sus vasos. Al dirigir la conversación Notch–TGF‑beta que controla cómo los fibroblastos depositan tejido cicatricial, tratamientos futuros podrían prevenir o revertir una forma fibrótica y persistente de la enfermedad que resiste a los fármacos actuales centrados en el sistema inmune.
Cita: Bhamidipati, K., McIntyre, A.B.R., Kazerounian, S. et al. Spatial patterning of fibroblast TGFβ signaling underlies treatment resistance in rheumatoid arthritis. Nat Immunol 27, 556–571 (2026). https://doi.org/10.1038/s41590-025-02386-2
Palabras clave: artritis reumatoide, fibrosis, fibroblastos, señalización TGF‑beta, vía Notch