Clear Sky Science · es
Ingeniería de xilosiltransferasas para manipular proteoglicanos en células de mamífero
Por qué importan los «abrigos» celulares
Cada célula de nuestro cuerpo lleva un «abrigo» molecular que la ayuda a comunicarse con sus vecinas y a percibir el entorno. Una parte principal de ese abrigo está formada por proteoglicanos: proteínas adornadas con largas cadenas de azúcares que funcionan como pequeñas antenas para factores de crecimiento, señales inmunitarias y señales estructurales. Cuando esta decoración azucarada falla, el desarrollo puede verse comprometido y tejidos como el óseo y el muscular pueden resultar gravemente afectados. Sin embargo, a los científicos les ha resultado difícil mapear exactamente qué proteínas llevan estas cadenas y cómo los componentes individuales del abrigo influyen en el comportamiento celular. Este estudio presenta una estrategia química precisa para etiquetar y reconstruir estas cadenas de azúcares en células de mamífero vivas, abriendo una vía para leer y reescribir la información codificada en sus superficies. 
Redirigir el primer paso de la unión de azúcares
La construcción de los proteoglicanos comienza cuando una familia especial de enzimas, las xilosiltransferasas XT1 y XT2, instala el primer azúcar sobre una proteína, marcando el punto donde crecerá una larga cadena. Debido a que ambas enzimas pueden realizar ese mismo primer paso, ha sido difícil saber en el interior celular qué proteínas esconde cada una. Los autores emplearon un diseño de «protuberancia y hueco» —común en la biología química moderna— para resolver esto. Reconfiguraron ligeramente el sitio activo de XT1, creando espacio adicional (el «hueco»), e introdujeron un bloque de construcción azucarado coincidente y algo más voluminoso, 6AzGlc (la «protuberancia»). La XT1 diseñada puede ahora usar este azúcar modificado, mientras que la enzima natural no, lo que permite a los investigadores etiquetar únicamente las proteínas modificadas por la enzima rediseñada.
Introducir un azúcar diseñado en las células
Para que este enfoque funcionara en células vivas, el equipo tuvo que entregar el azúcar con protuberancia en una forma que el metabolismo celular reconociera. En lugar de depender de las vías normales de captación de azúcares —que no manejan bien los análogos de xilosa— construyeron una versión enmascarada de 6AzGlc que lleva un grupo fosfato oculto. Una vez en el citosol, las enzimas celulares desenmascaran ese grupo y convierten la molécula en UDP‑6AzGlc, la forma activada requerida por las xilosiltransferasas diseñadas. Cromatografía cuidadosa confirmó que las células tratadas con el compuesto enmascarado correctamente configurado producían cantidades substanciales del azúcar activado diseñado, mientras que un control imagen especular produjo casi ninguna. 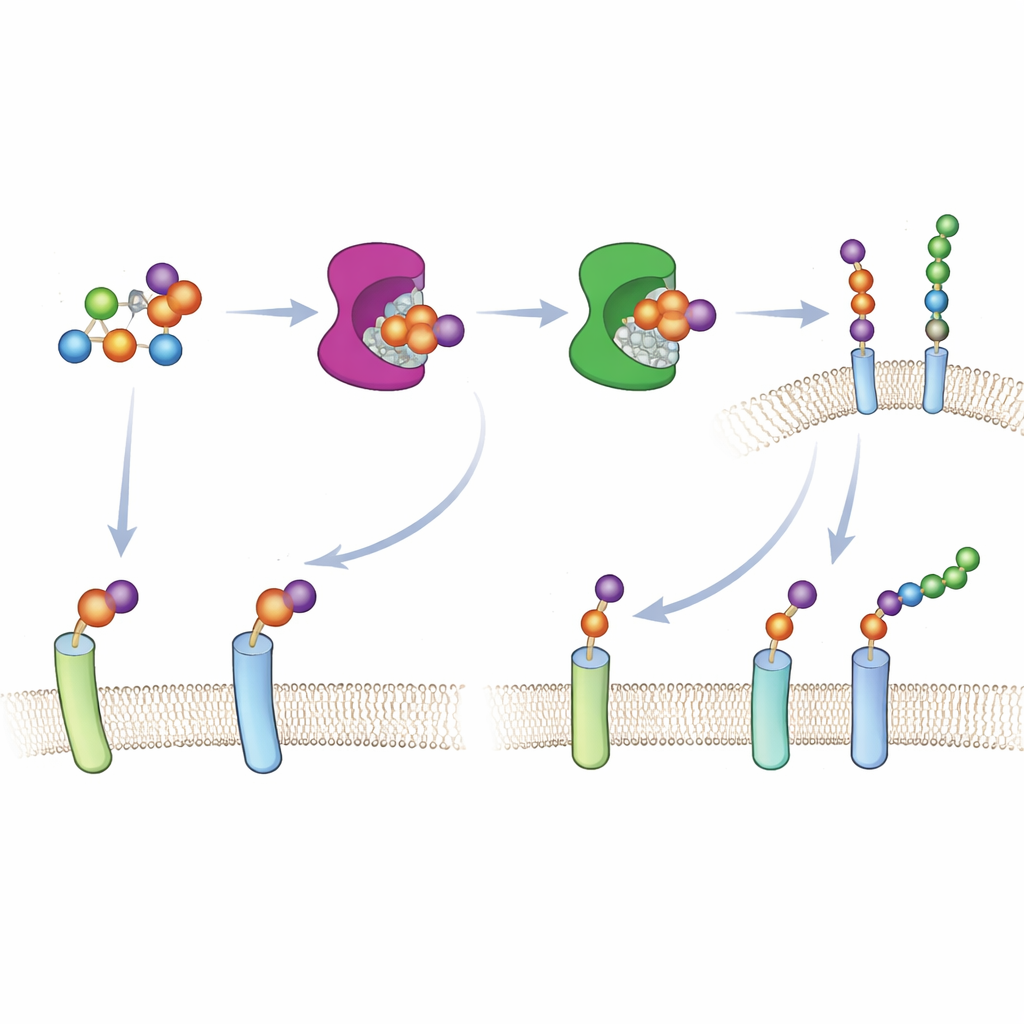
Etiquetar e identificar a los actores ocultos
Con la enzima modificada y el azúcar activado en su lugar, los investigadores demostraron que solo las células que expresaban la XT1 o XT2 diseñada incorporaban la etiqueta 6AzGlc en sus proteoglicanos de superficie. El grupo azida de 6AzGlc actúa como un pequeño asa química que puede «clicarse» a colorantes fluorescentes o a biotina, permitiendo la visualización y el enriquecimiento de las proteínas etiquetadas. La espectrometría de masas de las muestras enriquecidas reveló una colección amplia de proteoglicanos conocidos —incluyendo decorina, múltiples glicopicanos, sindecano‑4, CD44 y versicano—, confirmando que el sistema marca proteínas genuinamente portadoras de azúcares. Es importante que las enzimas diseñadas preservaron las mismas preferencias de secuencia que sus contrapartes naturales, lo que significa que la etiqueta química se instala en sitios de unión auténticos y no en posiciones nuevas o artificiales.
Construir proteoglicanos diseñados
Un beneficio inesperado de la etiqueta 6AzGlc es que, a diferencia del azúcar inicial natural, no puede ser extendida por las enzimas posteriores para formar una cadena completa. Esto efectivamente tope la cadena y simplifica la estructura molecular que debe analizarse por espectrometría de masas. Los autores convirtieron esta característica en una herramienta: después de que XT1 instala 6AzGlc en un sitio de unión natural, usan química «click» para acoplar fragmentos sintéticos de heparina, creando «proteoglicanos diseñados» con cadenas azucaradas definidas con precisión. En células de cáncer de mama que carecían de su propio sindecano‑1, la incorporación de esas versiones diseñadas restauró la extensión normal sobre una superficie recubierta de proteína, demostrando que el proteoglicano químicamente reconstruido puede sustituir funcionalmente al natural.
Qué significa esto para la biología y la medicina
Este trabajo proporciona un conjunto potente de herramientas para etiquetar y manipular selectivamente las cadenas de azúcares que controlan cómo las células se comunican. Al separar los roles de XT1 y XT2 y etiquetar solo sus objetivos directos, los investigadores pueden ahora mapear qué proteoglicanos operan en tejidos y estados patológicos específicos. La capacidad de detener el crecimiento natural de la cadena y reemplazarlo por azúcares construidos a medida también permite a los científicos desentrañar cuánto de la función de un proteoglicano la aporta su columna vertebral proteica frente a su «abrigo» azucarado. A largo plazo, dicha ingeniería de precisión puede ayudar a descifrar la señalización compleja en la superficie celular e inspirar terapias que reparen o reprogramen abrigos celulares defectuosos en trastornos del desarrollo, cáncer y otras enfermedades.
Cita: Li, Z., Chawla, H., Di Vagno, L. et al. Xylosyltransferase engineering to manipulate proteoglycans in mammalian cells. Nat Chem Biol 22, 612–621 (2026). https://doi.org/10.1038/s41589-025-02113-w
Palabras clave: proteoglicanos, glicosaminoglicanos, xilosiltransferasa, biología química, señalización en la superficie celular