Clear Sky Science · es
Un único sitio alostérico integra activación, modulación e inhibición en TRPM5
Cómo un pequeño guardián condiciona el gusto y el metabolismo
Los alimentos que disfrutamos y la forma en que nuestros cuerpos procesan el azúcar dependen de proteínas microscópicas “guardianas” en nuestras células. Uno de esos guardianes, un canal llamado TRPM5, nos ayuda a percibir sabores dulces, amargos y umami y ayuda al páncreas a liberar insulina. Este estudio revela cómo un pequeño bolsillo en TRPM5 puede actuar como un mando maestro: activar el canal, ajustar su sensibilidad e incluso apagarlo, hallazgos que podrían orientar futuros tratamientos para la diabetes, la obesidad y trastornos intestinales.
Un canal en la encrucijada del gusto y la glucemia
TRPM5 se sitúa en las membranas de las células gustativas de la lengua, en las células productoras de hormonas del intestino y en las células secretoras de insulina del páncreas. Cuando aumentan los niveles de calcio dentro de estas células, TRPM5 se abre y deja pasar iones cargados positivamente, cambiando brevemente el voltaje celular. En las papilas gustativas, esta señal eléctrica indica al cerebro la presencia de algo dulce, amargo o umami en la lengua. En el páncreas, contribuye a afinar las ráfagas de insulina tras una comida. Personas y animales con función TRPM5 alterada muestran problemas en la liberación de insulina y en el control de la glucemia, lo que sugiere que fármacos dirigidos a TRPM5 podrían algún día ayudar a tratar enfermedades metabólicas. Sin embargo, hasta hace poco, los investigadores carecían de herramientas precisas para encender o apagar este canal.
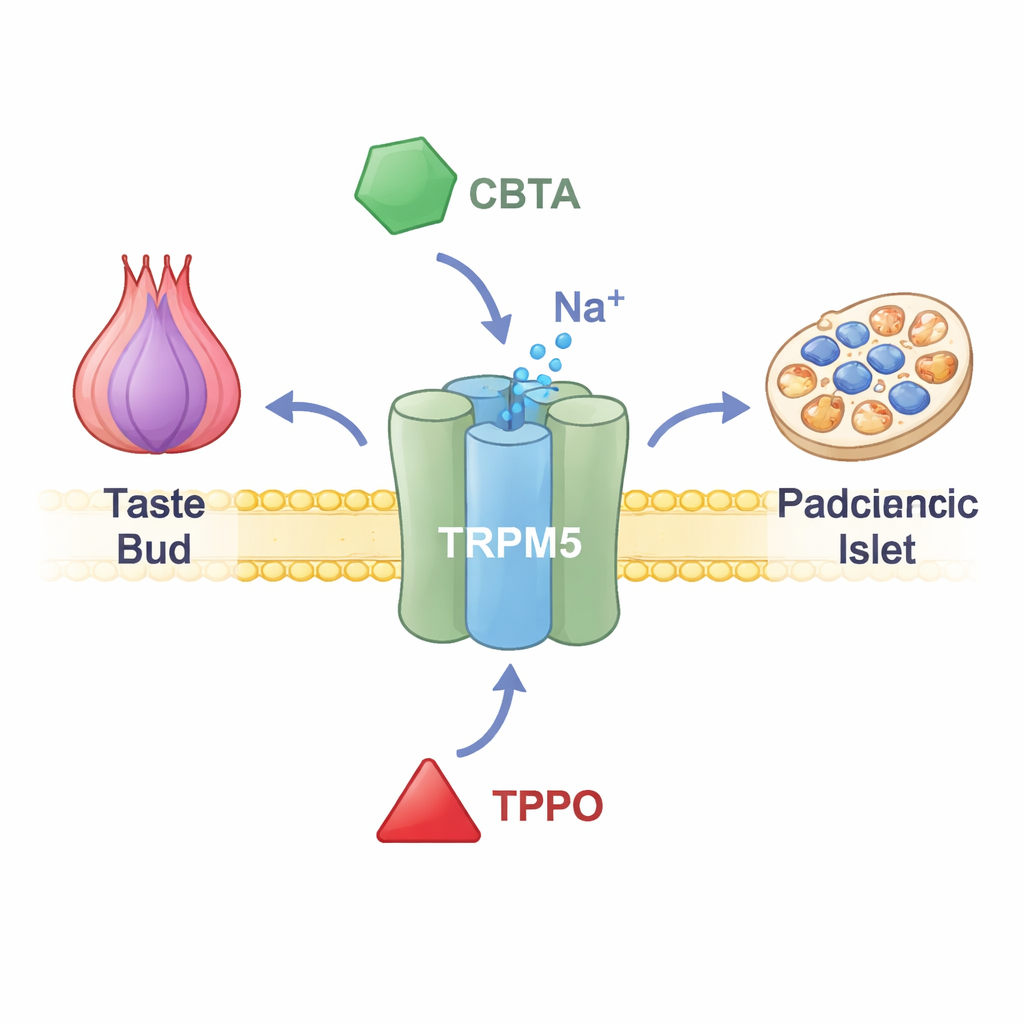
Un nuevo interruptor químico que sobrecarga el canal
Los investigadores se centraron en un compuesto sintético llamado CBTA, conocido anteriormente por estimular TRPM5 pero poco comprendido. Mediante registros eléctricos en células diseñadas para producir TRPM5, demostraron que CBTA puede abrir el canal incluso cuando el calcio está casi ausente, lo que prueba que actúa como un activador verdadero en lugar de solo potenciar los efectos del calcio. Cuando hay cantidades diminutas de calcio —niveles que normalmente mantienen TRPM5 en reposo— CBTA y el calcio actúan de forma conjunta, generando corrientes mucho mayores que cualquiera de los dos por separado. Esto significa que CBTA hace que TRPM5 sea extraordinariamente sensible, de modo que niveles de calcio cercanos al reposo se vuelven suficientes para disparar la apertura completa del canal.
Un bolsillo de control oculto revelado por criomicroscopía
Para ver cómo funciona esto a escala atómica, el equipo utilizó criomicroscopía electrónica para capturar instantáneas tridimensionales de TRPM5 en distintas condiciones. Descubrieron que CBTA se aloja en una cavidad hasta ahora desapercibida en la parte superior de una región sensible al voltaje del canal, justo por encima de donde normalmente se une el calcio. Esta cavidad, formada por un conjunto de aminoácidos, actúa como un sitio de acoplamiento preciso. Cuando los científicos mutaron los elementos clave que recubren este bolsillo, CBTA dejó de poder activar TRPM5, aunque el calcio seguía funcionando, lo que confirma que esta diminuta hendidura es esencial para la acción del compuesto. Sorprendentemente, la unión de CBTA reorganiza sutilmente partes cercanas de la proteína de modo que facilita enormemente que el calcio ocupe su sitio habitual, lo que explica la sinergia extraordinaria observada en las mediciones eléctricas.
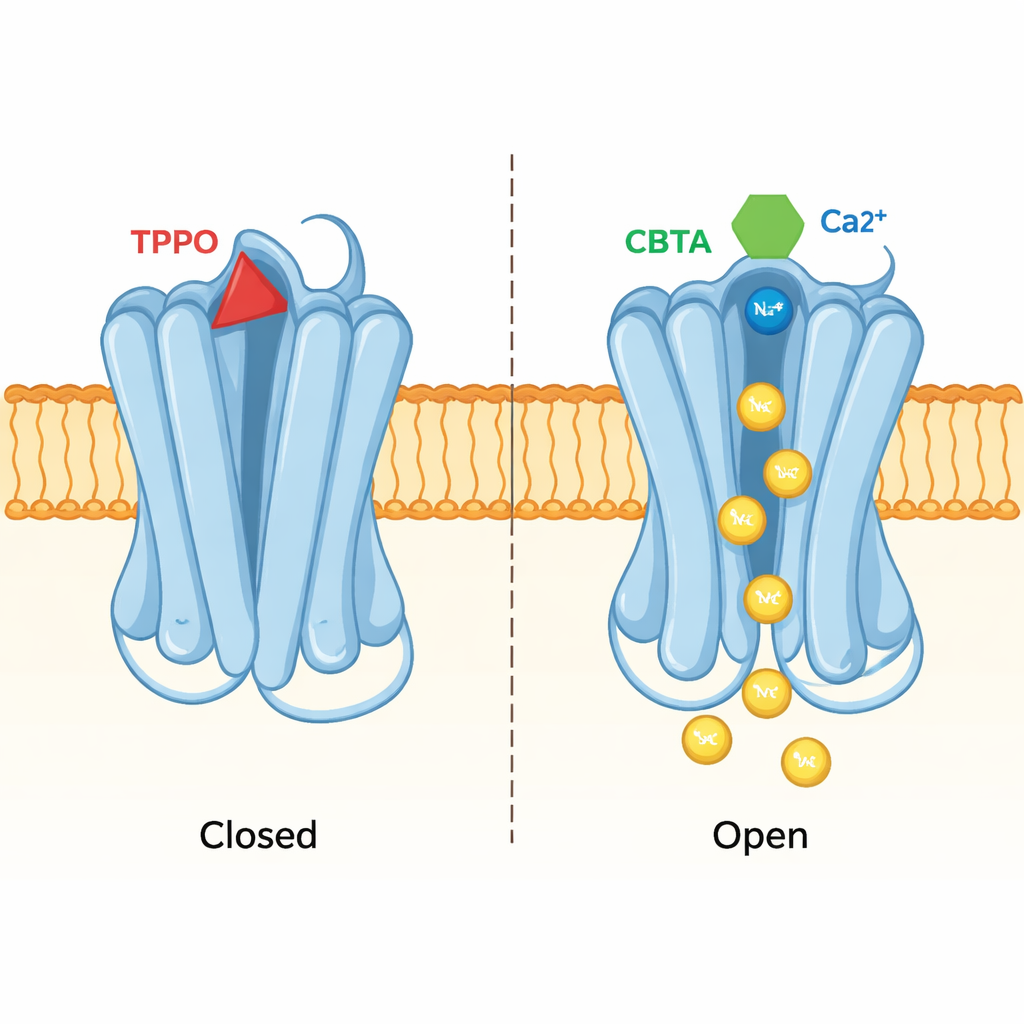
Un bolsillo, dos resultados opuestos
El mismo enfoque estructural reveló cómo un inhibidor llamado TPPO utiliza exactamente el mismo bolsillo para producir el efecto contrario. Cuando TPPO se une, ambos sitios de calcio en TRPM5 permanecen ocupados, pero el poro central del canal se mantiene apretado y no pasa corriente iónica. La comparación de las estructuras con TPPO y con CBTA mostró que sus diferentes formas empujan segmentos vecinos de la proteína en direcciones opuestas. CBTA promueve movimientos que se transmiten hasta el poro y lo abren; TPPO, en cambio, interrumpe la comunicación entre el bolsillo y el poro, manteniendo la compuerta cerrada. En esencia, este único bolsillo puede actuar como acelerador o freno, según la molécula que lo ocupe.
Redirigiendo el cableado interno del canal
El estudio también muestra que este bolsillo de control puede asumir funciones que normalmente realiza una región separada de unión al calcio en el interior de la célula. En canales mutantes donde el sitio interno habitual para el calcio está desactivado, el calcio por sí solo no podía abrir TRPM5. Sin embargo, CBTA seguía activando estos mutantes y remodeló un elemento estructural clave que conecta las partes internas y externas del canal. En otros mutantes que rompen la conexión entre la unión del calcio y la apertura del poro, añadir CBTA restauró el comportamiento normal. Estos resultados revelan que el sitio recién identificado puede redirigir o reparar la comunicación entre distintos dominios del canal, actuando como un centro flexible para la señalización a larga distancia dentro de la proteína.
Por qué importa para futuros fármacos
Para no especialistas, el mensaje central es que los investigadores han encontrado un único bolsillo sensible a fármacos en TRPM5 que puede integrar activación, ajuste fino y apagado. Un pequeño activador como CBTA puede tanto imitar al calcio como amplificar en gran medida la sensibilidad del canal, mientras que otro compuesto, TPPO, puede mantener el mismo canal bloqueado, todo al acoplarse en el mismo lugar. Este panorama unificado de cómo se controla TRPM5 abre la puerta al diseño de moléculas a medida que potencien o atenúen su actividad en tejidos específicos, con aplicaciones potenciales que van desde mejorar terapias basadas en el gusto y fármacos para la motilidad intestinal hasta desarrollar nuevas estrategias para gestionar la glucemia y las enfermedades metabólicas.
Cita: Ruan, Z., Lee, J., Li, Y. et al. A single allosteric site merges activation, modulation and inhibition in TRPM5. Nat Chem Biol 22, 402–410 (2026). https://doi.org/10.1038/s41589-025-02097-7
Palabras clave: canal TRPM5, percepción del gusto, secreción de insulina, apertura de canales iónicos, modulación alostérica