Clear Sky Science · es
Análisis de asociación del genoma completo de la hipotiroidismo autoinmune revelan contribuciones autoinmunes y específicas de la tiroides y una relación inversa con el riesgo de cáncer
Por qué esto importa para la salud cotidiana
Mucha gente se siente cansada, con frío o con niebla mental sin darse cuenta de que la glándula tiroidea puede ser la culpable. El hipotiroidismo autoinmune, en el que las defensas del propio cuerpo atacan lentamente la tiroides, afecta a más de una de cada veinte personas. Este estudio utiliza datos genéticos de cientos de miles de voluntarios para plantear dos preguntas principales: qué cambios hereditarios en nuestro ADN hacen que esta afección sea más probable y cómo se relacionan esos mismos cambios con el riesgo de desarrollar cáncer. Las respuestas revelan una compensación sorprendente entre un sistema inmunitario que a veces daña la tiroides pero que también puede ofrecer protección adicional frente a los tumores.
Mirando a lo largo de todo el genoma
Los investigadores combinaron registros de salud e información genética de dos grandes proyectos poblacionales, FinnGen en Finlandia y el UK Biobank en el Reino Unido. Se centraron en personas que necesitaban reemplazo de hormona tiroidea a largo plazo y excluyeron cuidadosamente a quienes tenían problemas tiroideos debidos a cirugía, cáncer u otras causas no autoinmunes. Esto produjo más de 81.000 casos de hipotiroidismo autoinmune y más de 700.000 controles, convirtiéndolo en el estudio más grande sobre esta afección hasta la fecha. Al escanear millones de marcadores de ADN en todo el genoma, descubrieron 418 señales genéticas independientes fuera del principal clúster de genes inmunes, repartidas en al menos 280 regiones del genoma. Muchas de estas señales implicaban cambios raros o de baja frecuencia en el ADN que alteran la estructura de las proteínas, ofreciendo pistas directas sobre la biología subyacente.
Separando los efectos inmunes generales de los específicos de la tiroides
El hipotiroidismo autoinmune se sitúa en la intersección entre la autoinmunidad general y la biología específica de la glándula tiroides. Para separar estos componentes, el equipo comparó sus resultados con estudios genéticos de otras enfermedades autoinmunes y con los niveles sanguíneos de la hormona estimulante de la tiroides, el marcador clínico clave para detectar una tiroides poco activa. Usando un método de clasificación bayesiano, agruparon las señales genéticas en las compartidas con enfermedades autoinmunes amplias y en las más específicas para la regulación de la hormona tiroidea. Estimaron que aproximadamente el 38% de las señales actúan a través de vías inmunitarias generales que influyen en muchas enfermedades autoinmunes, mientras que alrededor del 20% actúan principalmente mediante la función tiroidea. Las variantes centradas en la tiroides tendían a influir en los niveles hormonales y en genes activos en el tejido tiroideo, mientras que las variantes de la inmunidad general eran más activas en los linfocitos T, las células blancas que coordinan las respuestas inmunitarias.
Acercándose a un interruptor inmunitario clave
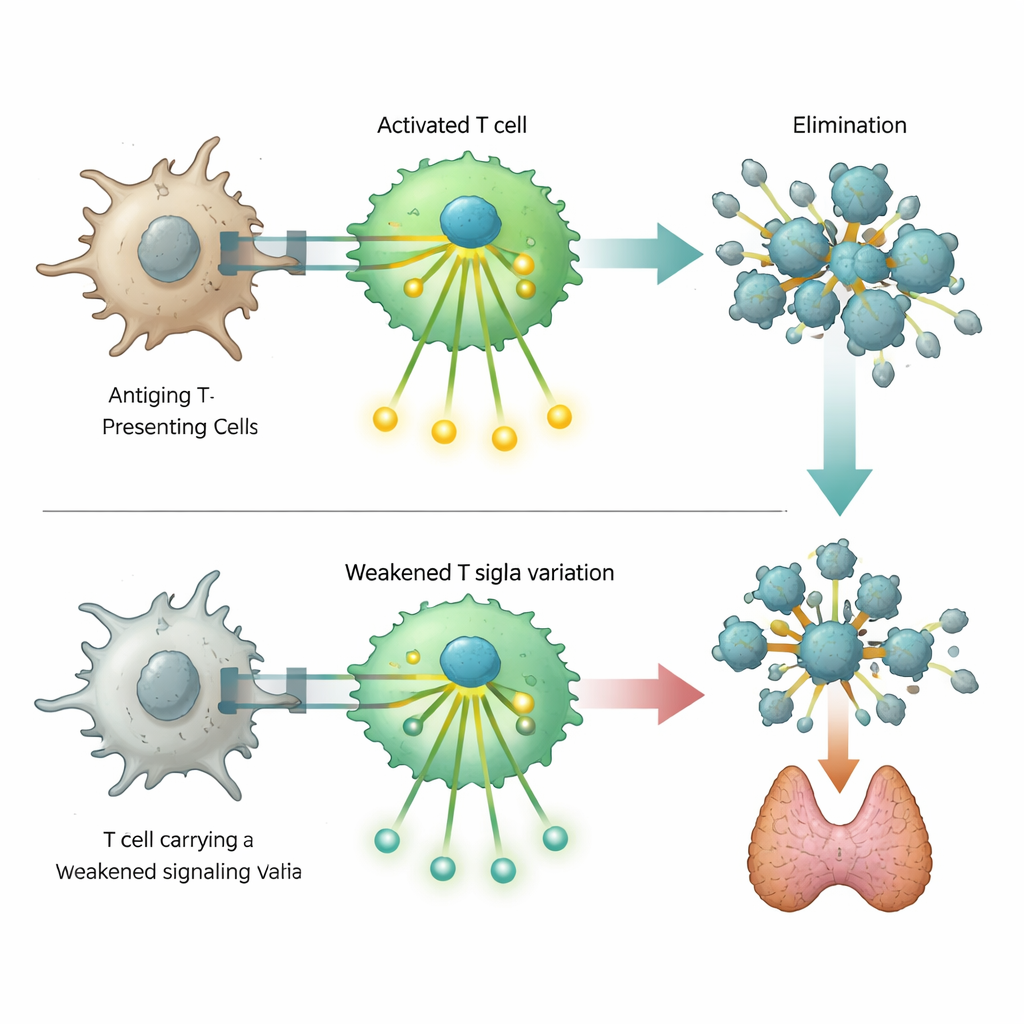
Uno de los hallazgos más llamativos involucró un cambio raro en el ADN del gen ZAP70, que codifica una proteína de señalización clave dentro de los linfocitos T. Se sabe que defectos severos en esta proteína causan deficiencia inmunitaria profunda, pero la variante identificada aquí produce solo una pérdida parcial de función. Experimentos de laboratorio en linfocitos T modificados mostraron que este ZAP70 alterado debilita, pero no bloquea completamente, la cascada de señales que normalmente sigue al reconocimiento de un objetivo. Las células portadoras de la variante tenían menos capacidad para activar marcadores de activación y pasos de señalización posteriores. Esta respuesta atenuada parece alterar el delicado equilibrio que normalmente elimina a los linfocitos T autorreactivos, predisponiendo así a los portadores a enfermedades autoinmunes y, al mismo tiempo, aumentando modestamente su riesgo de ciertas deficiencias inmunitarias.
Un vínculo inesperado con la protección frente al cáncer
Puesto que las mismas vías inmunitarias que impulsan la autoinmunidad también pueden atacar a los tumores, los autores se preguntaron a continuación cómo se relacionan las variantes genéticas del hipotiroidismo autoinmune con el riesgo de cáncer. Calcularon una puntuación poligénica que resume la tendencia heredada de cada persona hacia el hipotiroidismo y probaron su asociación con muchas enfermedades en los datos finlandeses. Como era de esperar, una puntuación más alta se correlacionó con un mayor riesgo de diversas enfermedades autoinmunes. Más sorprendente fue un patrón consistente de menor riesgo para varios cánceres, especialmente carcinoma basocelular y otros cánceres de piel, pero también cáncer de mama y de próstata y un agrupamiento global de “todos los cánceres”. Cuando el equipo examinó directamente los barridos genómicos del cáncer, alrededor del 10% de los sitios vinculados al hipotiroidismo también influían en el cáncer de piel, con la misma variante genética que generalmente aumentaba la autoinmunidad tiroidea mientras disminuía el riesgo de cáncer cutáneo. Estas variantes compartidas se concentraron en genes relacionados con la inmunidad, incluidos objetivos farmacológicos bien conocidos utilizados en la inmunoterapia con inhibidores de puntos de control.
Qué significa esto para pacientes y medicina
Visto de forma accesible, este trabajo muestra que algunas personas nacen con sistemas inmunitarios ajustados un poco “más activos”, lo que las hace más propensas a un daño lento y a menudo silencioso de la glándula tiroidea, pero al mismo tiempo mejor preparadas para detectar y eliminar tumores emergentes. El estudio desenreda qué cambios genéticos actúan mediante una sobreactivación inmunitaria general y cuáles afectan específicamente la producción de hormona tiroidea, explicando por qué condiciones como la enfermedad de Hashimoto y la de Graves pueden compartir algunos genes de riesgo y, sin embargo, empujar la función tiroidea en direcciones opuestas. También ayuda a explicar por qué los pacientes que desarrollan problemas tiroideos mientras reciben fármacos que potencian la inmunidad contra el cáncer a menudo responden mejor a esos tratamientos. En conjunto, los hallazgos sugieren que la variación común y natural en genes de puntos de control inmunitario y de señalización moldea tanto la enfermedad tiroidea autoinmune como el riesgo vitalicio de cáncer, ofreciendo nuevas pistas para la prevención y un uso más personalizado de las inmunoterapias.
Cita: Reeve, M.P., Kanai, M., Graham, D.B. et al. Genome-wide association analyses of autoimmune hypothyroidism reveal autoimmune and thyroid-specific contributions and an inverse relationship with cancer risk. Nat Genet 58, 550–559 (2026). https://doi.org/10.1038/s41588-026-02521-1
Palabras clave: hipotiroidismo autoinmune, enfermedad tiroidea, riesgo genético, sistema inmunitario, protección contra el cáncer