Clear Sky Science · es
Análisis de asociación del genoma completo resaltan el papel del entorno molecular intestinal en la variación de la microbiota humana
Por qué tu ADN y las bacterias intestinales forman parte de la misma historia
Billones de microbios viven en nuestros intestinos y afectan todo, desde la digestión y el metabolismo hasta el sistema inmune. Pero, ¿por qué algunas personas albergan de forma natural mezclas diferentes de bacterias intestinales que otras, incluso cuando viven en el mismo lugar y comen alimentos similares? Este estudio, basado en datos genéticos detallados y de microbiota de casi 30.000 adultos en Suecia y Noruega, muestra que nuestro propio ADN contribuye en silencio a escribir la comunidad microbiana que vive dentro de nosotros.
Una mirada masiva al interior de los intestinos nórdicos
Para descubrir cómo los genes humanos moldean el microbioma, los investigadores combinaron datos de cuatro grandes estudios poblacionales suecos, que abarcaron 16.017 adultos, y comprobaron sus hallazgos en 12.652 noruegos. Todos los participantes proporcionaron sangre para el análisis del ADN humano y muestras de heces para secuenciación profunda del ADN microbiano. En lugar de centrarse solo en grupos amplios de bacterias, el equipo utilizó métodos de alta resolución capaces de distinguir cientos de especies individuales. Después escanearon el genoma humano, variante por variante, para ver qué zonas del ADN se asociaban con la riqueza microbiana global (cuántas especies diferentes están presentes) y con la presencia o abundancia de especies bacterianas específicas.
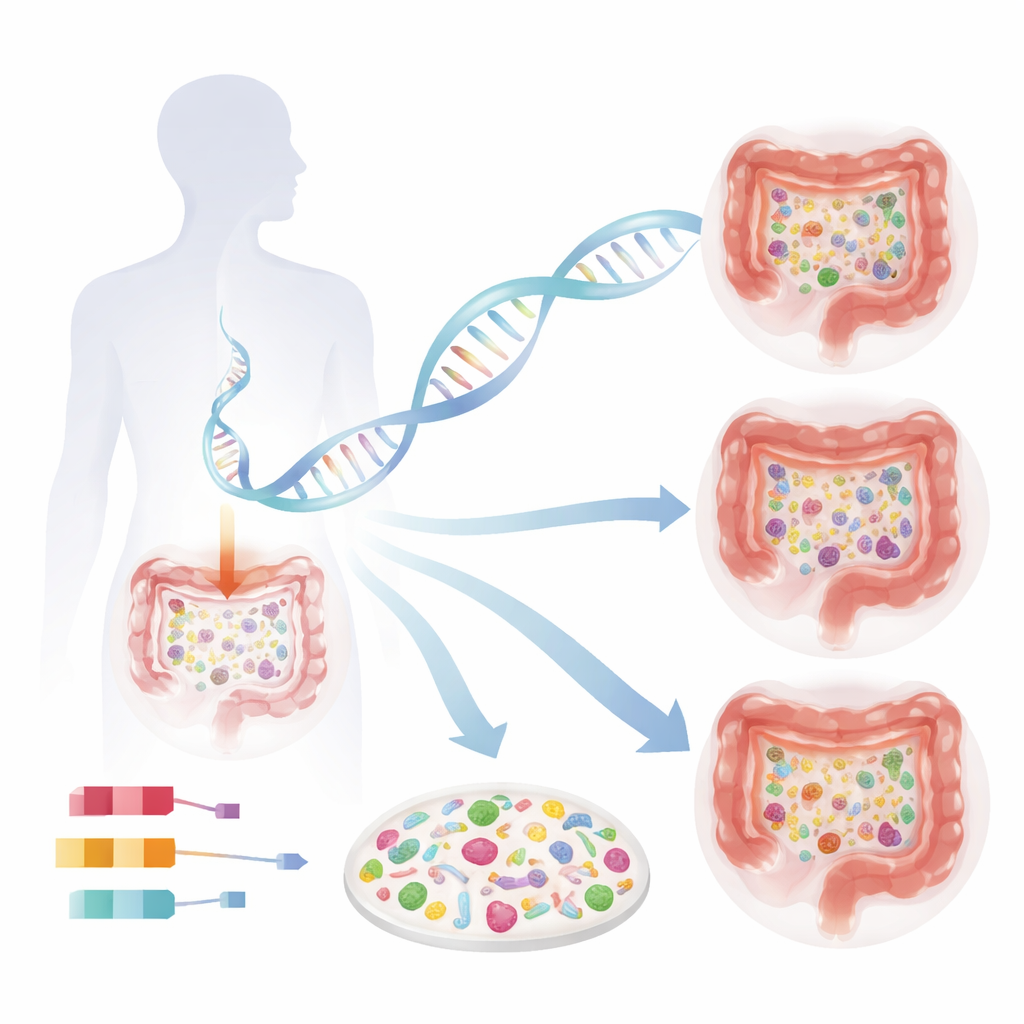
Interruptores genéticos que ajustan la riqueza microbiana
Uno de los descubrimientos más llamativos fue una región del genoma humano que contiene dos genes, OR51E1 y OR51E2, conocidos anteriormente como receptores de olores. Estos receptores también se localizan en células especiales productoras de hormonas en el revestimiento intestinal y detectan ácidos grasos producidos por microbios. Las personas que portaban una versión particular de esta región del ADN tendían a tener menos especies bacterianas en sus intestinos, y este patrón se confirmó de manera independiente en el grupo noruego. El hallazgo sugiere que la forma en que las células intestinales perciben los ácidos grasos derivados de microbios retroalimenta la diversidad del propio microbioma, posiblemente al alterar hormonas intestinales que controlan la motilidad, el apetito o las respuestas inmunitarias locales.
Azúcares superficiales, moco y el vecindario microbiano
El estudio también identificó varias regiones genéticas que gobiernan el entorno azucarado y viscoso en la superficie intestinal—territorio privilegiado para las bacterias. Variantes en el conocido gen de la lactasa (LCT), que determina si los adultos pueden digerir la lactosa de la leche, se asociaron con cambios en múltiples especies, incluyendo Bifidobacterium que prosperan con la lactosa. Genes que definen grupos sanguíneos y el estado de “secretor” relacionado—ABO, FUT2 y FUT3–FUT6—modifican los azúcares que contienen fucosa que se muestran en el moco intestinal y en las secreciones. Diferentes combinaciones genéticas aquí se vincularon a conjuntos distintos de bacterias que pueden adherirse a o alimentarse de estos azúcares. Otra región clave se localizó dentro de un gen de mucina, MUC12, parte del andamiaje de la propia capa de moco. Cambios en esta región se asociaron con la abundancia de una especie llamada Coprobacillus cateniformis e incluso compartieron una señal genética con la frecuencia de las deposiciones, lo que sugiere efectos entrelazados sobre la función intestinal y la composición microbiana.
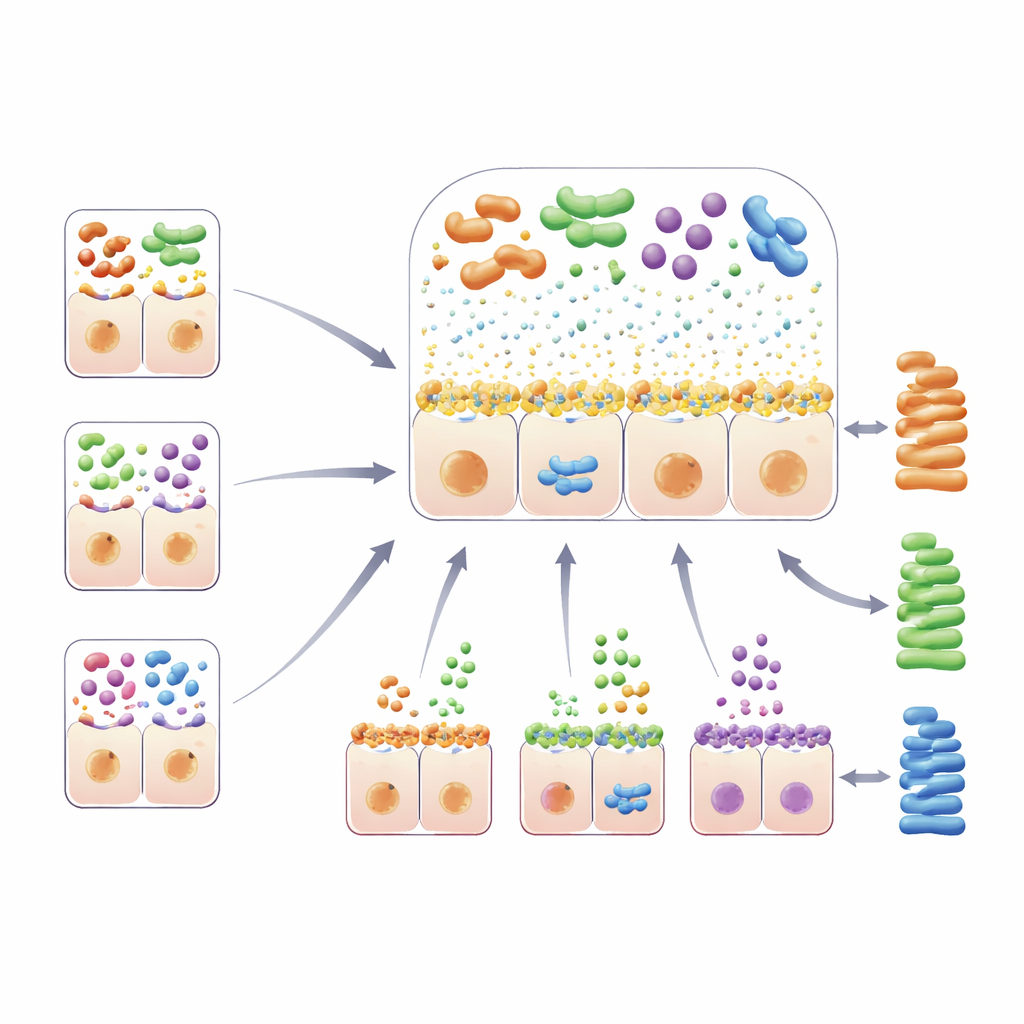
De los microbios al metabolismo y la forma corporal
Más allá de mapear “quién vive allí”, el equipo preguntó si las regiones del ADN vinculadas a determinadas bacterias también se solapaban con rasgos humanos como el colesterol en sangre, los ácidos biliares y la distribución de la grasa corporal. En varios casos participaron las mismas piezas del genoma. Variantes cerca de los genes CORO7–HMOX2 y FOXP1 afectaron a un grupo de bacterias que incluye Turicibacter y Clostridium saudiense, y también se alinearon con diferencias en la relación cintura–cadera, los ácidos biliares y el colesterol de lipoproteínas de baja densidad (LDL). Usando herramientas genéticas diseñadas para sugerir causa y efecto, los autores hallaron indicios de que un microbio, una especie de Intestinibacter, podría elevar el colesterol LDL, y que Turicibacter podría influir en dónde se almacena la grasa corporal. Otra región, SLC5A11, se asoció con una bacteria productora de butirato, Agathobaculum butyriciproducens, que ha mostrado efectos protectores en modelos animales de enfermedad cerebral. En este caso, la variante del ADN humano pareció reducir los niveles sanguíneos de una pequeña molécula llamada mio-inositol mientras favorecía el crecimiento de este microbio potencialmente beneficioso.
Qué significa esto para la salud y futuros tratamientos
En conjunto, estos resultados muestran que los genes humanos implicados en la detección intestinal, la composición del moco y los azúcares superficiales ayudan a determinar qué especies microbianas pueden establecerse con éxito en nuestros intestinos. Los efectos son modestos para cualquier gen individual, y la imagen hasta ahora es más clara para bacterias relativamente comunes en personas de ascendencia europea. Aun así, el trabajo amplía la lista de regiones del ADN humano vinculadas de forma fiable a microbios intestinales específicos de apenas un par a al menos ocho, y conecta varias de ellas con rasgos metabólicos como el colesterol y el patrón de distribución de la grasa corporal. Para el público general, el mensaje clave es que el microbioma intestinal no está moldeado solo por la dieta y el entorno: nuestro propio plano genético construye el hábitat que encuentran los microbios, inclinando a la comunidad hacia unos residentes y alejando a otros. A medida que lleguen estudios más amplios y diversos, entender esta relación bidireccional entre genes y microbios podría ayudar a personalizar consejos dietéticos, predecir riesgos de enfermedad y, quizás, guiar terapias que combinen fármacos, dieta y manipulación dirigida del microbioma.
Cita: Dekkers, K.F., Pertiwi, K., Baldanzi, G. et al. Genome-wide association analyses highlight the role of the intestinal molecular environment in human gut microbiota variation. Nat Genet 58, 540–549 (2026). https://doi.org/10.1038/s41588-026-02512-2
Palabras clave: microbioma intestinal, genética humana, moco intestinal, ácidos biliares, metabolismo