Clear Sky Science · es
GlycoRNA complejado con heparán sulfato regula la señalización de VEGF-A
Cómo las células afinan las señales para la formación de vasos sanguíneos
Los vasos sanguíneos no surgen allí donde aparecen señales de crecimiento de forma indiscriminada: deben controlarse con precisión para nutrir los tejidos sin alimentar tumores ni provocar ceguera. Este artículo revela un "freno" inesperado sobre una señal principal de crecimiento vascular llamada VEGF-A. Los autores muestran que pequeños fragmentos de ARN, que decoran el exterior de las células en colaboración con azúcares y proteínas, pueden atenuar el mensaje de VEGF-A, replanteando la forma en que pensamos sobre el lenguaje que usan las células en sus superficies.
Un papel sorprendente del ARN en la superficie celular
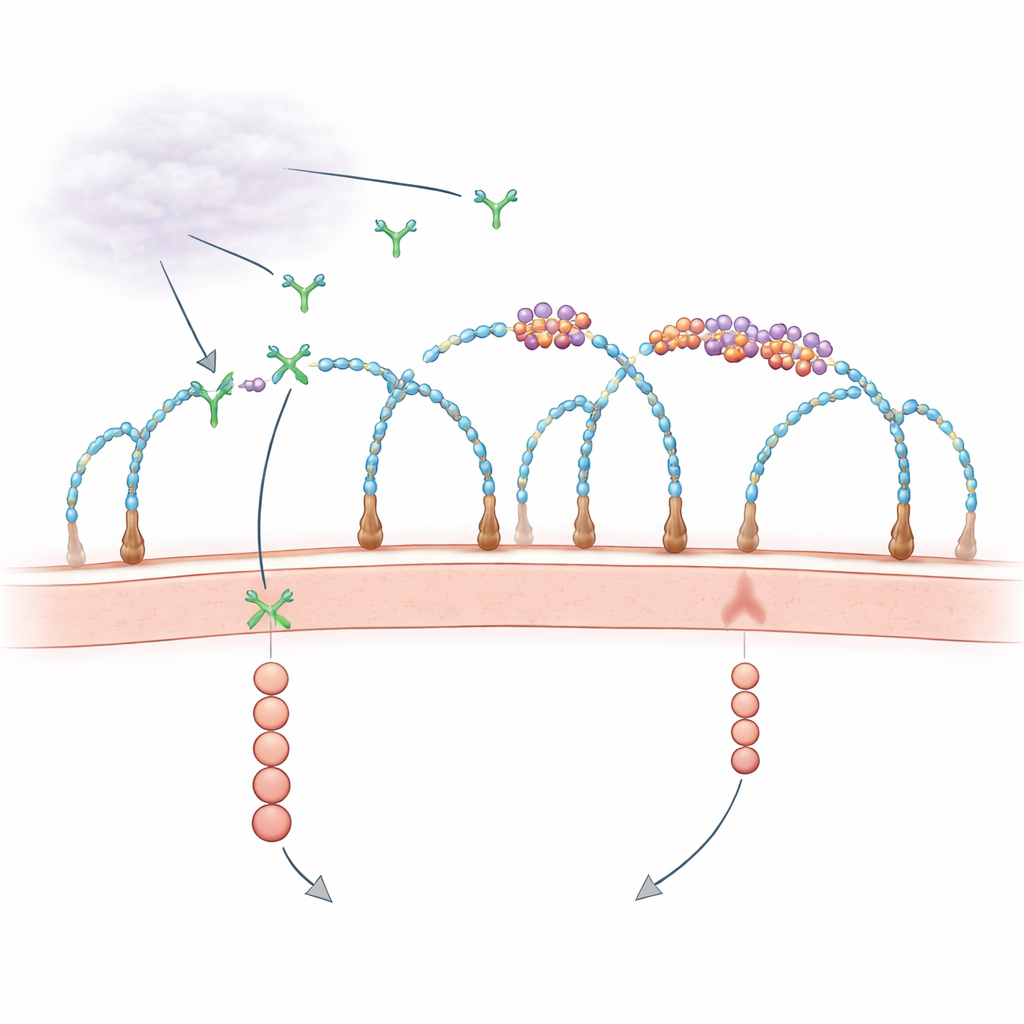
Durante décadas, los biólogos han sabido que el recubrimiento exterior de la célula, rico en proteínas decoradas con azúcares llamadas proteoglicanos de heparán sulfato, ayuda a capturar factores de crecimiento y presentarlos a sus receptores. Al mismo tiempo, observaciones dispersas insinuaban que fragmentos de ARN fuera de las células podrían influir en el crecimiento vascular, pero los actores y mecanismos no estaban claros. Trabajos recientes revelaron que algunos ARN pequeños están químicamente unidos a azúcares complejos para formar “glycoRNAs”, y que ciertas proteínas ligadoras de ARN también aparecen en la superficie celular, agrupándose junto con estos ARN. El nuevo estudio plantea una pregunta directa: ¿estos pequeños islotes de ARN–proteína en la membrana controlan realmente cómo se reciben señales de crecimiento como VEGF-A?
Construir islotes agrupados de ARN–proteína con cadenas de azúcar
Mediante cribados CRISPR de genoma completo y microscopía de alta resolución, los investigadores descubrieron que cadenas de azúcar específicas—heparán sulfato con determinadas sulfatas—son andamios esenciales para ensamblar estos cúmulos de ARN–proteína, que denominan ribonucleoproteínas en la superficie celular (csRNPs). Cuando se eliminaron enzimas clave que construyen o sulfatan el heparán sulfato, los cúmulos de glycoRNA y sus proteínas asociadas desaparecieron de la superficie celular, aunque los ARN y proteínas seguían presentes dentro de las células. Enzimas que recortan las cadenas de heparán sulfato de la superficie o bloqueos químicos de la sulfatación produjeron el mismo efecto. Estos resultados muestran que las cadenas de heparán sulfato intactas y correctamente sulfatadas organizan las csRNPs en islotes a nanoescala en la membrana.
Los cúmulos de ARN actúan como frenos sobre una potente señal de crecimiento vascular
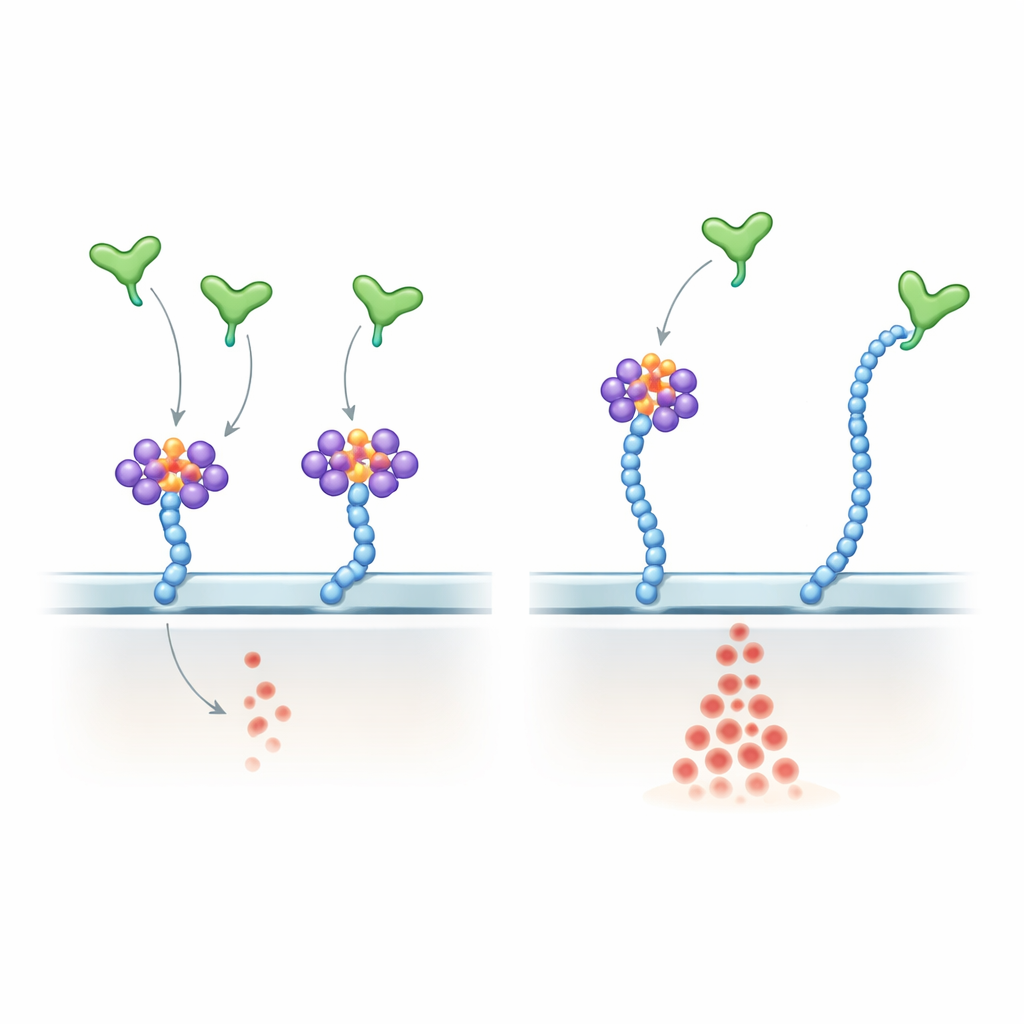
El equipo se centró luego en células endoteliales humanas, que recubren los vasos sanguíneos y responden a VEGF-A. Encontraron que estas células también muestran cúmulos de csRNP anclados por heparán sulfato. Tratar células vivas con RNasas, enzimas que degradan ARN, eliminó el componente ARN sin perturbar las cadenas de azúcar subyacentes. En esas condiciones, la forma más común de VEGF-A que se une al heparán (VEGF-A165) desencadenó una activación mucho más intensa de la vía de señalización ERK aguas abajo, mientras que una forma más corta sin la cola de unión al heparán (VEGF-A121) no se vio afectada. Más moléculas de VEGF-A165 se unieron a la superficie celular tras la eliminación del ARN, aunque los niveles de receptor permanecieron iguales. En dispositivos microfluídicos 3D, las células endoteliales expuestas a RNasa crecieron más en geles de colágeno y formaron estructuras tubulares de modo más robusto, lo que indica que destruir el ARN de la superficie desata un comportamiento pro-angiogénico.
Desentrañar cómo VEGF-A detecta ARN frente a azúcar
Para explorar el mecanismo, los autores mostraron que VEGF-A165 se une directamente a ciertos ARN pequeños, incluidos muchos glycoRNAs conocidos, a través de su región C-terminal cargada positivamente—la misma región que se une al heparán sulfato. Diseñaron una versión sutil de VEGF-A165 en la que residuos clave de arginina en esta cola se cambiaron por lisinas. Este mutante mantuvo su carga positiva global y aún reconoció cadenas de heparán sulfato, pero se unió pobremente al glycoRNA y se volvió en gran medida insensible al tratamiento con RNasa. En células endoteliales, el mutante produjo una activación de ERK más intensa y más resistente a RNasa que la VEGF-A165 normal, imitando de cerca el efecto de eliminar ARN de la superficie celular. En ratones vivos, inyectar el mutante en el ojo provocó un crecimiento vascular retiniano más exuberante que la proteína normal. En embriones de pez cebra, la sobreexpresión de la versión mutante de Vegfa alteró el patrón vascular normal y aumentó el número de células endoteliales.
Del mecanismo básico a implicaciones más amplias
Finalmente, los autores demostraron que fusionar la cola de unión al heparán de VEGF-A a una proteína señal no relacionada, Wnt3a, podía redirigir la actividad de Wnt: unir la cola normal redujo los cambios desarrollamentales impulsados por Wnt, mientras que unir la cola insensible al ARN los aumentó. En conjunto, estos experimentos apoyan un modelo en el que los cúmulos csRNP, anclados por heparán sulfato específicamente sulfatado, se unen a VEGF-A y factores relacionados para moderar su actividad. Cuando se elimina el componente ARN o cuando los factores de crecimiento pierden su capacidad de detectar ARN, el equilibrio se inclina hacia una señalización más intensa y un desarrollo vascular alterado en varias especies.
Por qué esto importa para la salud y futuras terapias
Para un no especialista, el mensaje clave es que las células usan no solo proteínas y azúcares, sino también pequeños ARN expuestos en su superficie para afinar señales de crecimiento potentes como VEGF-A. Estos cúmulos de ARN–proteína anclados a azúcares actúan como frenos ajustables sobre la formación de vasos sanguíneos, ayudando a asegurar que los nuevos vasos broten dónde y cuándo se necesitan. Alterar este equilibrio—degradando el ARN de la superficie o modificando las propiedades de unión al ARN de los factores de crecimiento—puede exagerar o desviar el crecimiento vascular. Comprender esta capa de control recién revelada podría abrir la puerta a terapias que ajusten con mayor precisión la angiogénesis en cáncer, enfermedades oculares, cicatrización de heridas y medicina regenerativa, apuntando a los ARN de superficie, sus andamios de azúcar o las regiones sensibles al ARN de los factores de crecimiento.
Cita: Chai, P., Kheiri, S., Kuo, A. et al. GlycoRNA complexed with heparan sulfate regulates VEGF-A signalling. Nature 651, 808–818 (2026). https://doi.org/10.1038/s41586-025-10052-8
Palabras clave: angiogénesis, factor de crecimiento endotelial vascular, heparán sulfato, ARN en superficie celular, glycoRNA