Clear Sky Science · es
Secuenciación a escala poblacional resuelve determinantes del ADN persistente de EBV
Por qué un virus común sigue importando
La mayoría de los adultos portan el virus de Epstein–Barr (EBV), a menudo sin llegar a saberlo. Para algunos, sin embargo, este pasajero silencioso se asocia con enfermedades que van desde la mononucleosis hasta ciertos cánceres y trastornos autoinmunes. Este estudio plantea una pregunta sencilla pero de gran alcance: ¿podemos usar las enormes reservas de datos de ADN ya recopiladas de la población para ver quién tiene más EBV en sangre y si sus genes ayudan a determinar quién mantiene el virus bajo control y quién no?
Leer una huella viral oculta en nuestro ADN
Los biobancos modernos, como el UK Biobank y el programa All of Us de EE. UU., han secuenciado el ADN completo de cientos de miles de voluntarios. Estos proyectos se centraron en los genes humanos, pero los datos brutos también contienen fragmentos sueltos de ADN viral. Los investigadores se dieron cuenta de que el genoma humano de referencia usado para el alineamiento incluye una "cromosoma" adicional para EBV. Al reexaminar las lecturas que se alinearon con ese segmento de EBV, pudieron estimar cuántas copias del genoma de EBV estaban presentes en la sangre de cada persona en el momento de la toma de muestras. Tras enmascarar cuidadosamente algunas regiones repetitivas engañosas, definieron a las personas con niveles claramente detectables como portadoras de "ADNemia por EBV": una cantidad medible de ADN de EBV circulando en la sangre.
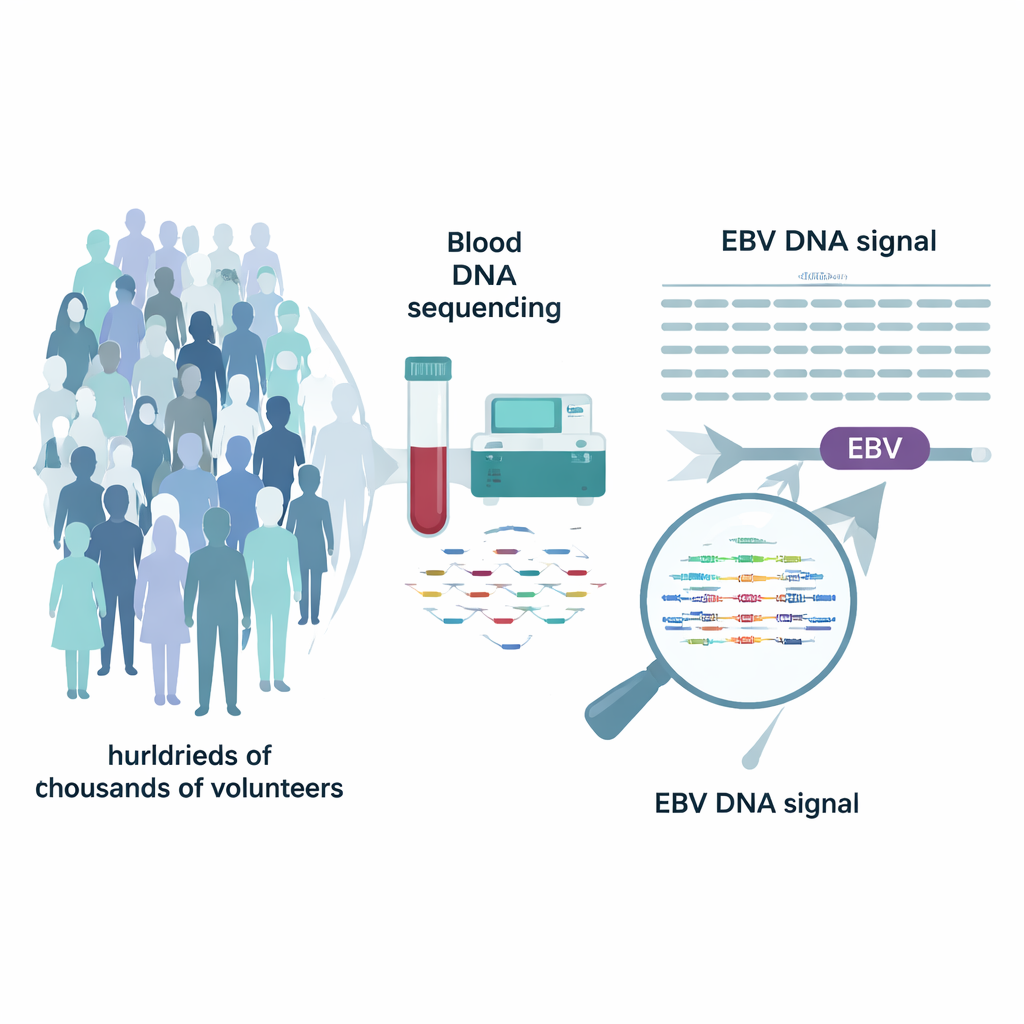
Una pequeña minoría porta una carga viral alta
Al examinar casi medio millón de personas en el UK Biobank y un cuarto de millón en All of Us, el equipo encontró que la mayoría de los adultos no tenían ADN detectable de EBV en sangre, aunque más del 90 % mostraba evidencia de infección pasada en pruebas de anticuerpos. Sin embargo, aproximadamente el 10 % de los participantes se situó en una cola de la distribución con ADN de EBV claramente elevado. Estos individuos tendían a ser mayores, con mayor proporción de hombres, y tenían una ligera mayor probabilidad de estar tomando medicamentos inmunosupresores. Patrones similares aparecieron en ambas cohortes, y en un conjunto separado de muestras de saliva el virus fue mucho más frecuente, lo que subraya que EBV reside en diferentes reservorios del cuerpo y que las mediciones en sangre capturan solo uno de ellos.
Vínculos entre la persistencia viral y la enfermedad
Con este nuevo biomarcador en mano, los autores investigaron cómo se relaciona la persistencia de ADN de EBV en sangre con la salud. Escanearon miles de códigos de diagnóstico y mediciones de laboratorio para ver cuáles eran más comunes en personas con ADNemia por EBV. Surgieron asociaciones sólidas con afecciones ya sospechadas de estar vinculadas a EBV, incluyendo el linfoma de Hodgkin, la artritis reumatoide, el lupus, la enfermedad pulmonar obstructiva crónica y ciertos cánceres de pulmón. También se detectaron señales para problemas cardiovasculares, insuficiencia renal, depresión y fatiga, y vínculos sugestivos con trastornos neurológicos raros como la neuromielitis óptica. Muchos de estos patrones se reprodujeron en la cohorte independiente de All of Us. El estudio no puede probar que EBV cause estos problemas, pero muestra que niveles altos de ADN de EBV en sangre son un marcador de riesgos de salud más amplios y de alteración inmune.
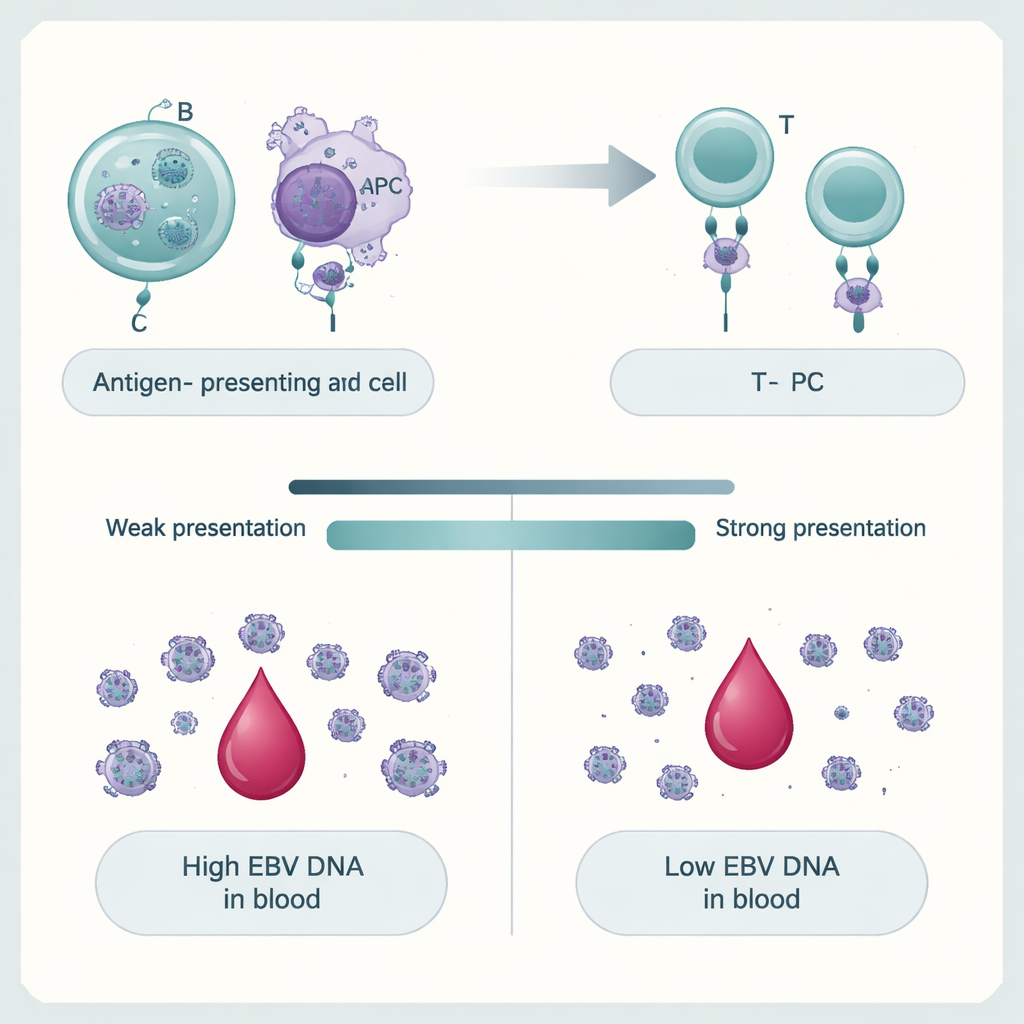
Cómo nuestros genes influyen en el control del virus
El equipo se preguntó entonces por qué solo algunas personas presentan niveles altos de ADN de EBV. Al escanear millones de variantes genéticas en todo el genoma, demostraron que la ADNemia por EBV es un rasgo poligénico: muchas pequeñas diferencias en el ADN actúan conjuntamente para empujar los niveles virales hacia arriba o hacia abajo. Las señales más fuertes se agruparon en y alrededor de genes del complejo mayor de histocompatibilidad (MHC), que ayudan a las células inmunitarias a mostrar fragmentos virales a las células T. Variantes que alteran estas proteínas, en particular las moléculas del MHC de clase II, se asociaron de forma estrecha con la persistencia del ADN de EBV. Los genes activos en las células B —la principal residencia a largo plazo de EBV— y en otras células presentadoras de antígeno estuvieron especialmente enriquecidos. Usando modelos computacionales de cómo diferentes variantes humanas del MHC se unen a fragmentos del proteoma de EBV, los autores encontraron que las versiones previstas para presentar fragmentos de EBV con mayor eficacia tendían a proteger frente a niveles altos de ADN de EBV, mientras que los presentadores más débiles se asociaban con persistencia.
Qué significa esto para entender la infección
Para el público general, el mensaje central es que nuestro equilibrio a largo plazo con EBV no es aleatorio. Al explotar datos de ADN a escala poblacional ya existentes, el estudio muestra que la composición genética de una persona —especialmente en genes inmunitarios que muestran piezas virales a las células T— ayuda a determinar cuánto EBV permanece en su sangre. Los niveles elevados señalan a un subconjunto de personas con mayor riesgo de una variedad de enfermedades inmunes, respiratorias y posiblemente neurológicas. El trabajo ofrece un plan para convertir datos antiguos de secuenciación en nuevos conocimientos sobre muchos virus que conviven con nosotros, y sugiere que estrategias específicas para potenciar o imitar una presentación antigénica eficaz podrían, algún día, ayudar a mantener infecciones de por vida como EBV mejor bajo control.
Cita: Nyeo, S.S., Cumming, E.M., Burren, O.S. et al. Population-scale sequencing resolves determinants of persistent EBV DNA. Nature 650, 664–672 (2026). https://doi.org/10.1038/s41586-025-10020-2
Palabras clave: Virus de Epstein–Barr, persistencia viral, genética humana, enfermedad autoinmune, secuenciación de biobancos