Clear Sky Science · es
Vacunas de ARNm individualizadas provocan una inmunidad duradera de células T en la TNBC adyuvante
Nueva esperanza tras el tratamiento del cáncer de mama
Para muchas mujeres con una forma agresiva de cáncer de mama denominada cáncer de mama triple negativo, el miedo no termina cuando concluyen la quimioterapia y la cirugía. Este cáncer tiene un alto riesgo de reaparecer y de diseminarse, a menudo en apenas unos años. El estudio descrito aquí prueba una vacuna altamente personalizada, construida a partir de las propias mutaciones del tumor de cada paciente, para comprobar si puede entrenar al sistema inmunitario para vigilar durante años y reducir la probabilidad de recaída una vez finalizado el tratamiento estándar.
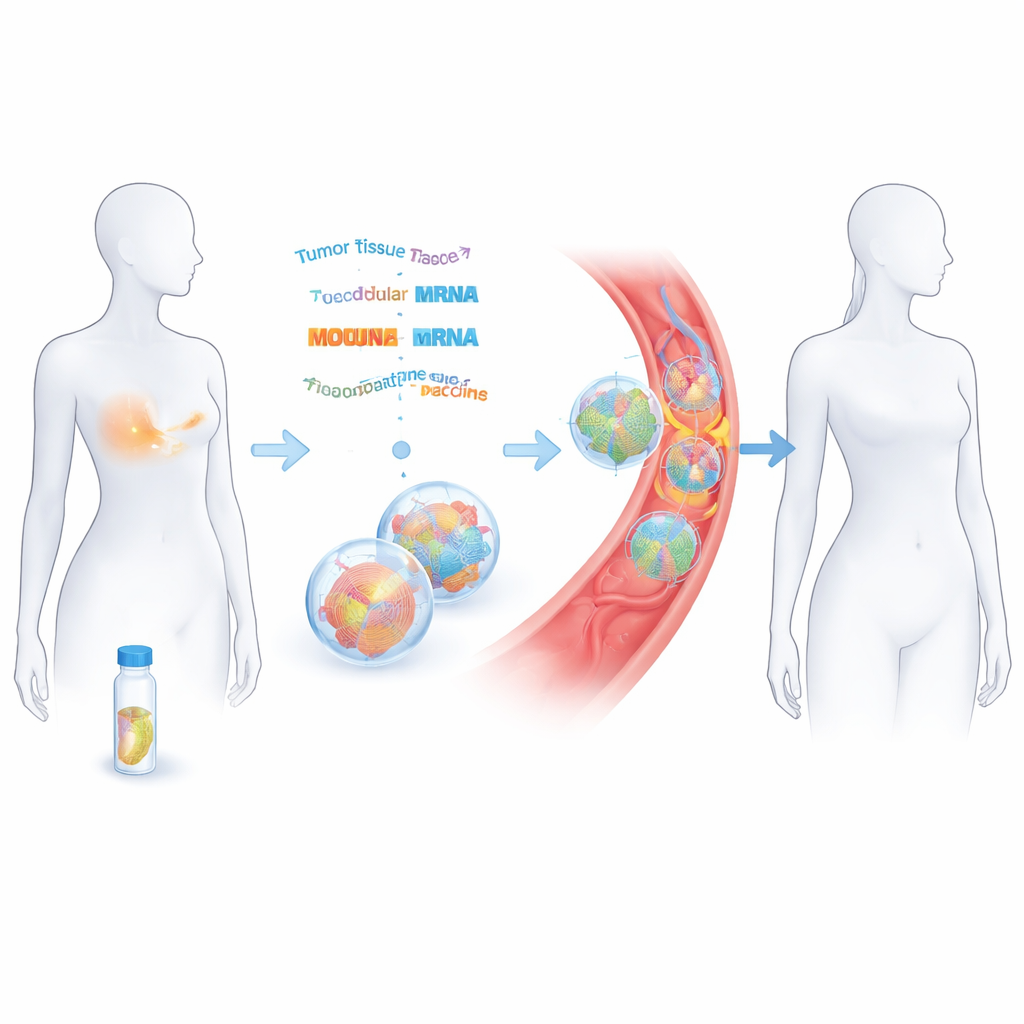
Convertir un tumor extirpado en una vacuna a medida
Los investigadores trabajaron con 14 mujeres que tenían cáncer de mama triple negativo en estadio temprano y que ya habían recibido cirugía y quimioterapia con intención curativa. A partir del tejido tumoral extraído, secuenciaron el ADN y ARN para catalogar las mutaciones únicas del cáncer. Con herramientas informáticas, predijeron cuáles de estos cambios podrían ser identificados como extraños por las células inmunitarias. Hasta 20 de estos “neoantígenos” se ensamblaron y codificaron en dos cadenas de ARN mensajero (ARNm), similar en principio a las vacunas contra la COVID‑19 pero adaptadas a cada paciente. Estas cadenas de ARNm se encapsularon en pequeñas burbujas lipídicas y se administraron por vía intravenosa en ocho dosis durante aproximadamente dos meses.
Cómo despierta la vacuna a los defensores inmunitarios
Una vez en el cuerpo, el ARNm instruye a centinelas inmunitarios llamados células dendríticas para que fabriquen brevemente las proteínas neoantigénicas y muestren fragmentos de ellas en su superficie. Esto actúa como un cartel de los más buscados para las células T, la fuerza principal del sistema inmunitario contra el cáncer. El equipo extrajo sangre antes de la vacunación y en varios momentos posteriores para testar si aparecían células T específicas frente a los neoantígenos y cuán potentes eran. Mediante ensayos de laboratorio sensibles, encontraron que todas las pacientes desarrollaron respuestas de células T nuevas o aumentadas contra al menos una de las mutaciones seleccionadas, y la mayoría respondió a varias. En muchos casos, grandes fracciones de las células T circulantes —niveles que normalmente sólo se ven con poderosas terapias celulares— estaban ahora orientadas a reconocer dianas específicas del tumor.
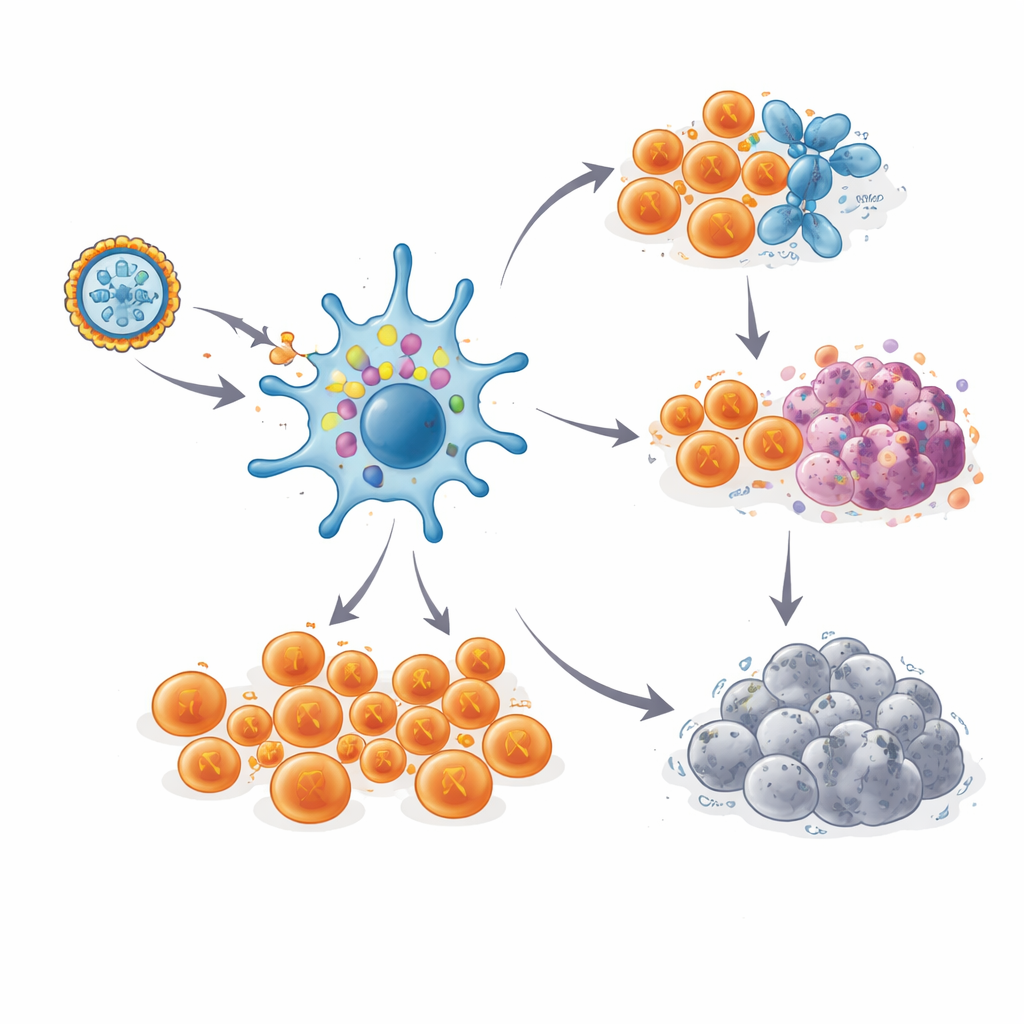
Memoria inmunitaria duradera
De forma importante, estas respuestas de células T no se desvanecieron rápidamente. En la mayoría de las pacientes, las respuestas fuertes alcanzaron su pico durante el periodo de vacunación, cayeron ligeramente y luego se mantuvieron en niveles altos entre uno y tres años y medio, incluso sin dosis de refuerzo. Al seguir las “huellas” únicas de los receptores de clones individuales de células T, los científicos pudieron rastrear células reactivas a neoantígenos concretos hasta seis años en una paciente que permaneció libre de cáncer. Los análisis detallados a nivel de célula única mostraron dos destinos principales para estas células. Muchas se convirtieron en células T citotóxicas altamente armadas, listas para destruir cualquier célula que portara el neoantígeno adecuado. Otras evolucionaron hacia una población de memoria más rara, con un perfil similar al de células madre y marcadores de autorrenovación, lo que sugiere un reservorio capaz de regenerar nuevas oleadas de combatientes si reaparecieran células cancerosas.
Qué ocurrió con las pacientes
Tras una mediana de algo más de cinco años de seguimiento desde la primera dosis de la vacuna, once de las catorce mujeres no habían sufrido una recaída; una de ellas falleció por causas no relacionadas mientras aún estaba en remisión. Tres mujeres sí recayeron, y sus casos arrojan pistas sobre por qué una vacuna personalizada a veces puede fallar. Una paciente solo logró una respuesta de células T débil y posteriormente se benefició de otra inmunoterapia, un anticuerpo anti‑PD‑1, antes de sucumbir finalmente a una enfermedad diseminada. Una segunda paciente tenía riesgo hereditario y tumores en ambas mamas; solo se utilizó un tumor para diseñar la vacuna, y más tarde se demostró que la recaída procedía del tumor genéticamente distinto y no vacunado. La tercera paciente presentó células T inducidas por la vacuna que infiltraron el tumor recurrente, pero las células cancerosas habían perdido en gran medida moléculas clave necesarias para mostrar neoantígenos en su superficie, ocultándose efectivamente del ataque inmunitario.
Por qué este trabajo importa para el futuro
Este estudio en fase temprana fue pequeño y no contó con un grupo de control, por lo que no puede demostrar que la vacuna por sí sola evitó las recaídas. No obstante, muestra que fabricar una vacuna compleja y personalizada de ARNm a partir del propio tumor del paciente es factible en entornos hospitalarios de rutina, en general bien tolerada y capaz de inducir ejércitos de células T potentes y duraderos contra múltiples dianas específicas del cáncer. Los hallazgos también destacan vías de escape que los tumores pueden utilizar, como la pérdida del aparato de presentación de antígenos o el surgimiento a partir de lesiones no dirigidas, lo que señala la necesidad de combinaciones con otras inmunoterapias y secuenciación tumoral más extensa. Para las pacientes con cáncer de mama triple negativo, este trabajo sugiere que una vacuna a medida, administrada tras el tratamiento estándar, podría algún día ayudar a impedir la reaparición de la enfermedad convirtiendo su propio sistema inmunitario en una línea de defensa duradera y muy específica.
Cita: Sahin, U., Schmidt, M., Derhovanessian, E. et al. Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC. Nature 651, 1088–1096 (2026). https://doi.org/10.1038/s41586-025-10004-2
Palabras clave: cáncer de mama triple negativo, vacunas contra el cáncer de ARNm, inmunoterapia con neoantígenos, inmunidad de células T, recurrencia tumoral