Clear Sky Science · es
El envejecimiento favorece la acumulación microglial de proteínas sinápticas de degradación lenta
Por qué importa la limpieza de proteínas en nuestro cerebro a medida que envejecemos
La mayoría de nosotros deseamos mantener la agudeza mental con la edad, pero el envejecimiento es el factor de riesgo más importante para el Alzheimer y otras demencias. Este estudio plantea una pregunta aparentemente sencilla: ¿qué sucede con la «tarea doméstica» diaria de las proteínas dentro de las células cerebrales a medida que envejecemos? Al desarrollar nuevas herramientas moleculares en ratones para seguir proteínas neuronales recién sintetizadas a lo largo del tiempo, los investigadores rastrean cómo se renuevan las proteínas, cómo se agrupan en agregados y cómo las células inmunitarias del cerebro, las microglías, ayudan a limpiar el desorden. Sus hallazgos revelan una desaceleración amplia en la limpieza proteica que se centra en las sinapsis —las uniones donde se comunican las neuronas— y que puede ayudar a explicar la pérdida de memoria relacionada con la edad.
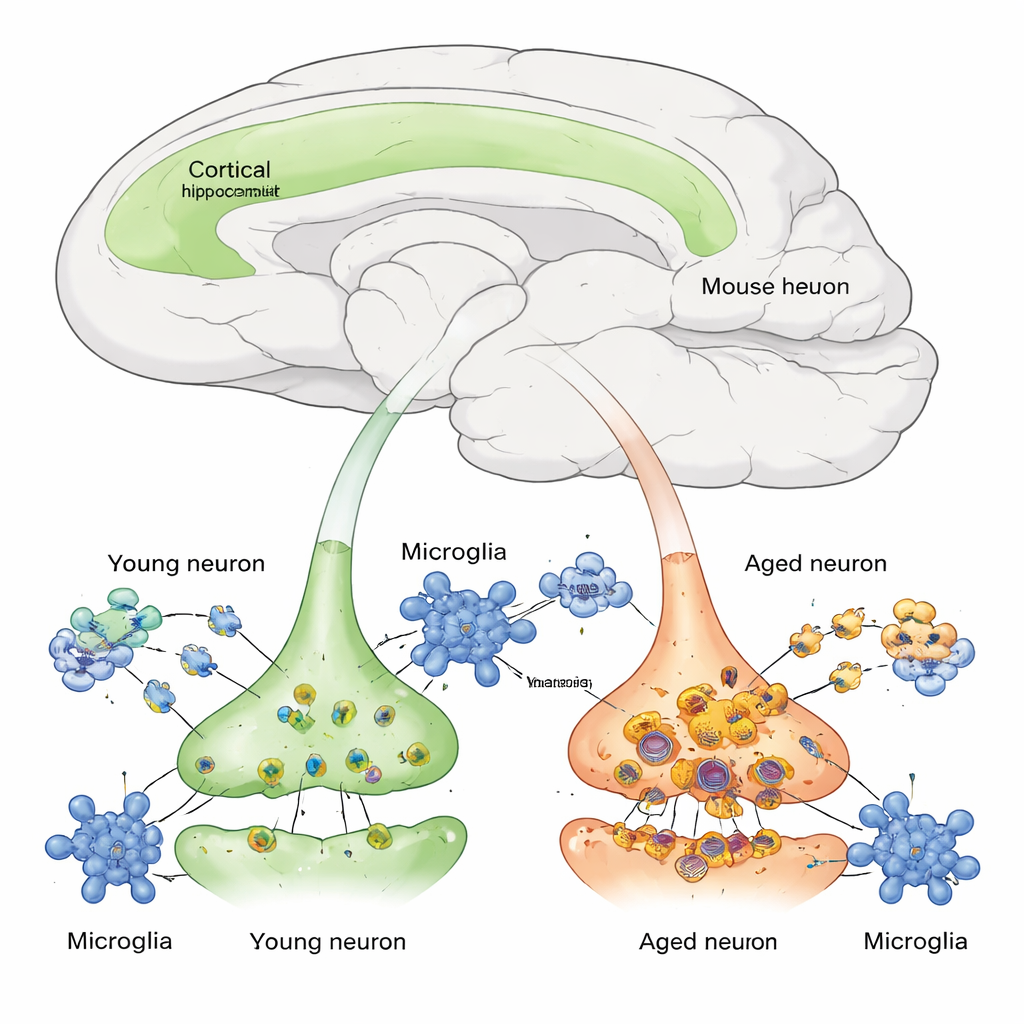
Rastreando proteínas nuevas en células cerebrales vivas
Las proteínas en nuestras células se sintetizan y se degradan constantemente, un equilibrio conocido como proteostasis. Hasta ahora ha sido difícil medir este proceso en tipos celulares concretos dentro de un cerebro mamífero vivo. Los autores diseñaron ratones con un sistema genético de «marcado» llamado BONCAT que hace que solo ciertas neuronas —las que usan el promotor Camk2a, principalmente neuronas excitadoras corticales y del hipocampo— inserten un aminoácido especial, clicable, en las proteínas recién hechas. Tras administrar este aminoácido a los ratones durante un periodo corto, el equipo pudo aislar e identificar únicamente las proteínas neuronales recién sintetizadas usando espectrometría de masas, y después observar cómo sus niveles descendían con el tiempo a medida que las proteínas se degradaban.
Cómo el envejecimiento ralentiza el recambio proteico
Usando una versión viral de la herramienta de marcado, los investigadores etiquetaron neuronas en ratones jóvenes (4 meses), de mediana edad (12 meses) y envejecidos (24 meses). Luego siguieron miles de proteínas en varias regiones cerebrales —corteza sensorial y visual, hipocampo e hipotálamo— durante un periodo de «persigue» de dos semanas tras cesar el marcado. Al modelar estas curvas de decaimiento, estimaron la vida media de cada proteína, es decir, cuánto tarda en eliminarse la mitad de ella. En promedio, las vidas medias de las proteínas neuronales se duplicaron aproximadamente entre los ratones jóvenes y los envejecidos, con la mayor parte de la desaceleración emergiendo tras la mediana edad. El efecto varió según la región, y ciertos conjuntos de proteínas se degradaron de forma estrechamente coordinada, lo que indica que rutas enteras —como las que controlan la señalización sináptica— comparten cinéticas dependientes de la edad.
Proteínas que se agrupan y sinapsis vulnerables
Una tasa de degradación más lenta aumenta el riesgo de que las proteínas se plieguen mal y se adhieran entre sí. El equipo aisló agregados insolubles en detergente de cerebros de ratones envejecidos y, usando su marcador neuronal, definió un «agregoma» de 1.726 proteínas neuronales que terminan en estos cúmulos. Casi la mitad de las proteínas que mostraron degradación reducida con la edad también aparecieron en los agregados, y muchas se relacionan por estudios genéticos previos con trastornos del neurodesarrollo o neurodegenerativos. Las proteínas sinápticas destacaron: componentes de la maquinaria pre- y postsináptica, uniones celulares y elementos mitocondriales en las sinapsis estaban muy enriquecidos tanto entre las proteínas de degradación lenta como entre las que se agregan. La microscopía confirmó que proteínas específicas como RTN3 y SRSF3 formaban puntas parecidas a agregados en el hipocampo de ratones envejecidos pero no en los jóvenes. Este fallo de la proteostasis centrado en la sinapsis concuerda con la evidencia de larga data que muestra que la pérdida sináptica se correlaciona estrechamente con el deterioro cognitivo.
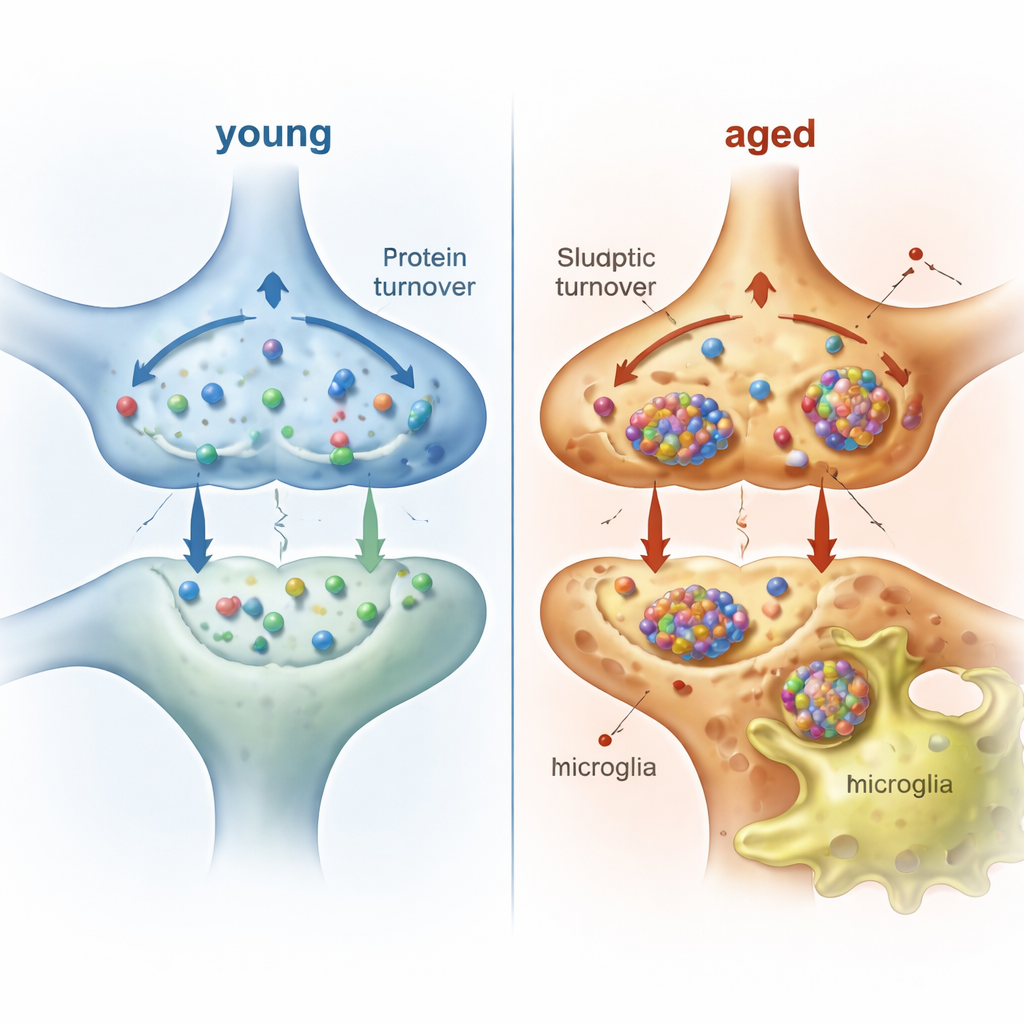
Microglía como el equipo de limpieza del cerebro
Las neuronas no afrontan esta carga en solitario. Las microglías, las células inmunitarias residentes del cerebro, monitorizan y podan sinapsis constantemente. Para ver qué material de origen neuronal ingieren realmente las microglías en animales vivos, los autores etiquetaron proteínas neuronales durante una semana en ratones jóvenes y envejecidos, luego purificaron cientos de miles de microglías y aislaron las proteínas marcadas que contenían. Detectaron cientos de proteínas neuronales dentro de las microglías, con una fuerte representación de componentes sinápticos, de membrana y mitocondriales. Muchas de estas proteínas llevan secuencias señal o son conocidas como carga de exosomas, lo que sugiere que la secreción es una vía de transferencia, mientras que otras concuerdan con la fagocitosis microglial de elementos sinápticos. En los ratones envejecidos, las microglías contenían más tipos y mayores cantidades de proteínas de origen neuronal que en los jóvenes, aunque el equilibrio entre componentes pre- y postsinápticos se mantuvo similar.
Cuando la limpieza falla, el cerebro paga el precio
Al superponer tres conjuntos de datos —proteínas cuya degradación se ralentiza con la edad, proteínas halladas en agregados neuronales y proteínas que se acumulan en microglías de cerebros envejecidos— el estudio identificó 166 proteínas que se sitúan en la intersección de estos procesos. Más de la mitad de todas las proteínas de origen neuronal enriquecidas en microglías envejecidas mostraron algún tipo de problema de proteostasis relacionado con la edad. Muchas están codificadas por genes previamente señalados como factores de riesgo para Alzheimer, Parkinson y otros trastornos cerebrales. En conjunto, estos resultados delinean una cascada: con la edad, el recambio de proteínas neuronales se ralentiza, especialmente en las sinapsis; las proteínas vulnerables tienen más probabilidad de plegarse mal y agregarse; y las microglías eliminan cada vez más estos componentes dañados, posiblemente mediante la fagocitosis de sinapsis estresadas. A corto plazo, esto puede proteger a las neuronas, pero a lo largo de décadas podría contribuir a la pérdida sináptica y al deterioro cognitivo. Entender y, eventualmente, restaurar una proteostasis neuronal saludable podría ser por tanto una estrategia clave para mantener la resiliencia cerebral en la vejez.
Cita: Guldner, I.H., Wagner, V.P., Moran-Losada, P. et al. Ageing promotes microglial accumulation of slow-degrading synaptic proteins. Nature 650, 930–941 (2026). https://doi.org/10.1038/s41586-025-09987-9
Palabras clave: envejecimiento cerebral, recambio proteico, sinapsis, microglía, neurodegeneración