Clear Sky Science · es
El blindaje metabólico dependiente de poliaminas regula el empalme alternativo
Cómo moléculas diminutas ayudan a las células a leer sus genes
Dentro de cada célula, el mismo guion de ADN puede leerse de muchas maneras, lo que permite que un número limitado de genes genere una enorme variedad de proteínas. Esta flexibilidad depende de un proceso llamado empalme alternativo, que edita los mensajes de ARN antes de que se conviertan en proteínas. Este artículo revela que pequeñas moléculas cargadas positivamente llamadas poliaminas orientan silenciosamente esta etapa de edición, actuando como una especie de escudo protector que ayuda a las células a decidir qué versiones de ARN producir. Dado que el empalme alternativo es crucial en el cáncer, la función cerebral y las células madre, desvelar esta capa oculta de control tiene implicaciones amplias para la salud y la enfermedad.
Pequeños ayudantes cargados en cada célula
Las poliaminas son moléculas diminutas y flexibles que portan múltiples cargas positivas. Las células las sintetizan a partir de nutrientes básicos y desde hace tiempo se las conoce como apoyos para el crecimiento y la supervivencia, especialmente en células que se dividen rápidamente como los tumores. Los autores se preguntaron si las poliaminas también actúan como señales, no solo como combustible. Al bloquear parcialmente la producción de poliaminas en células de cáncer de próstata y en ratones, midieron cómo cambiaban las proteínas y el ARN a lo largo del tiempo. Descubrieron que mucho antes de que los niveles totales de poliaminas cayeran de forma drástica, hubo una intensa oleada de cambios en la fosforilación de proteínas—marcadores químicos que activan o desactivan interruptores proteicos—especialmente en componentes de la maquinaria de edición del ARN celular, el espliceosoma.
Reconfigurando el editor de ARN de la célula
Centrándose específicamente en el ARN, el equipo utilizó secuenciación profunda para seguir el empalme alternativo cuando se inhibía la síntesis de poliaminas. Cientos de segmentos de ARN se omitieron o se incluyeron de forma diferente, en líneas celulares cancerosas, tipos celulares normales y tejidos de ratón. Estos cambios no fueron simplemente un efecto secundario de una división celular más lenta ni de otro proceso dependiente de poliaminas conocido como hipusinación. En cambio, cuando los investigadores reabastecieron las células con poliaminas externas, muchos de los cambios en el empalme volvieron rápidamente hacia la normalidad. Tanto fármacos como herramientas genéticas que redujeron las poliaminas produjeron patrones de empalme similares, y una reducción adicional de poliaminas con una combinación de fármacos reforzó aún más los cambios, confirmando que el efecto estaba estrechamente vinculado a la disponibilidad de poliaminas.
Un objetivo oculto: el módulo SF3 del empalme
Para localizar dónde actúan las poliaminas dentro de la maquinaria de empalme, los autores compararon la firma de empalme causada por la disminución de poliaminas con un mapa de referencia amplio generado al silenciar individualmente más de 300 factores de empalme conocidos. La coincidencia más cercana apuntó a una parte específica del espliceosoma llamada subcomplejo SF3, que ayuda a reconocer señales clave en el ARN. El análisis computacional de datos públicos de unión proteína–ARN apoyó este vínculo: los ARNs cuyo empalme se alteró por la pérdida de poliaminas eran especialmente propensos a ser unidos por proteínas SF3. Cuando el equipo deshabilitó parcialmente componentes de SF3 genéticamente o con un fármaco, los efectos sobre el empalme debidos a la depleción de poliaminas se borraron en gran medida, mostrando que la actividad intacta de SF3 es necesaria para esta nueva vía reguladora. 
Blindaje metabólico: cómo las poliaminas bloquean el etiquetado proteico
Al profundizar, los investigadores observaron que los sitios de fosforilación más afectados en las proteínas SF3 se agrupaban dentro de tramos cortos ricos en aminoácidos cargados negativamente. Modelado molecular y experimentos de resonancia magnética nuclear mostraron que las poliaminas se alojan en estos parches ácidos, formando múltiples contactos electrostáticos y cubriendo parcialmente residuos de serina cercanos donde normalmente se agregan grupos fosfato. Este “abrazo” físico reduce la accesibilidad de estos sitios a las quinasas proteicas—las enzimas que añaden fosfatos. En experimentos in vitro, añadir poliaminas bloqueó directamente a una quinasa llamada CK1 para fosforilar proteínas SF3. En células, inhibir CK1 y su pariente cercano CK2 mitigó los cambios de empalme provocados por la pérdida de poliaminas, y ratones diseñados genéticamente cuya proteína SF3A3 carecía de tres sitios clave de fosforilación se volvieron en gran parte insensibles a los desplazamientos de empalme dependientes de poliaminas. 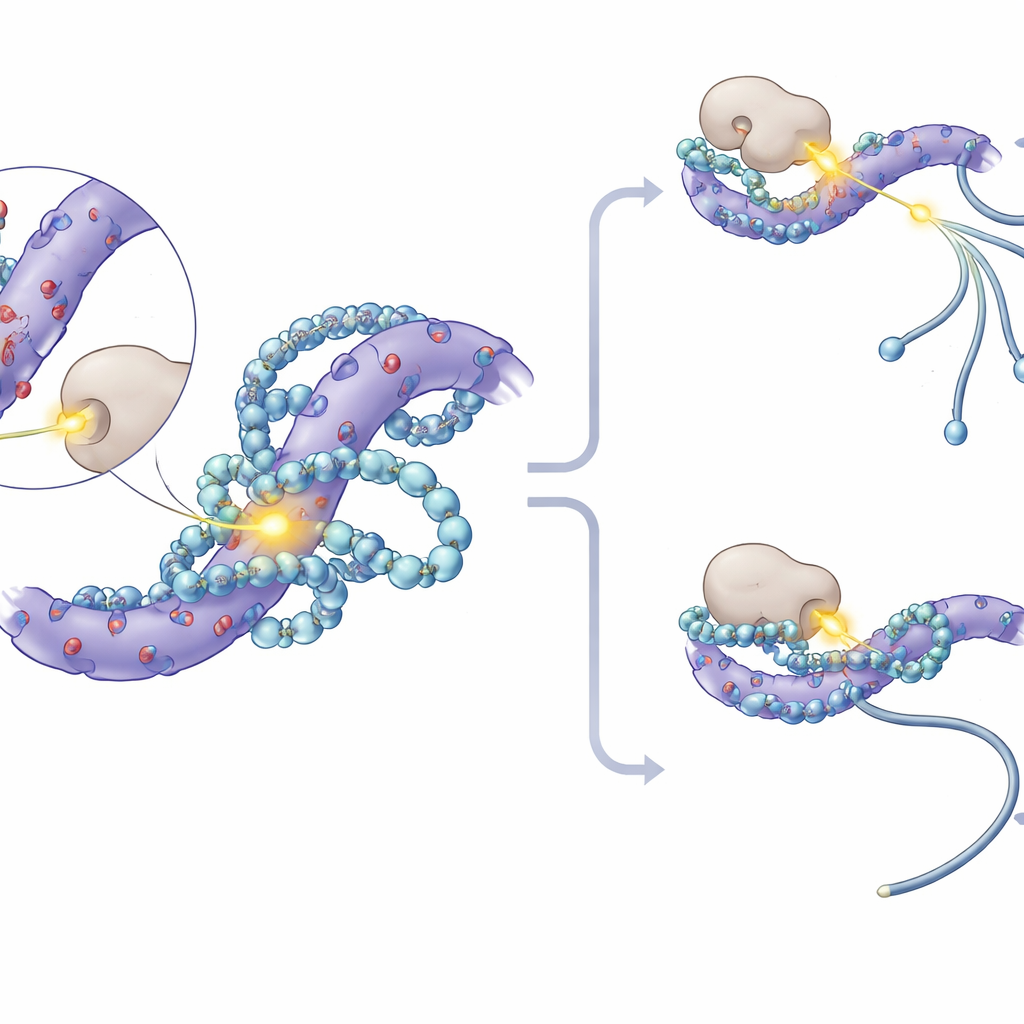
Una molécula diseñada que separa funciones
El estudio también presenta un fármaco similar a las poliaminas, BENSpm, que tiene una carga positiva más intensa pero al mismo tiempo suprime la producción celular de poliaminas. BENSpm se unió fuertemente a los parches ácidos de SF3 y bloqueó la acción de las quinasas, al igual que las poliaminas naturales, sin embargo no restauró el crecimiento celular cuando las poliaminas reales eran escasas. Esto permitió a los autores separar las funciones clásicas de las poliaminas (apoyo al crecimiento y al metabolismo) del papel recientemente definido de blindaje. En células madre embrionarias de ratón, la depleción de poliaminas empujó a las células a perder su marcador de “pluripotencia” Nanog y alteró su paisaje de empalme. BENSpm restauró tanto el perfil de empalme como la expresión de Nanog pese a la supresión continua de la síntesis normal de poliaminas, lo que indica que el blindaje metabólico es un requisito clave para mantener la identidad de las células madre.
Por qué importa este descubrimiento
En términos cotidianos, este trabajo muestra que las poliaminas actúan como pequeños guantes protectores alrededor de partes sensibles de proteínas clave del empalme. Cuando los guantes están puestos, las quinasas no pueden agarrar y etiquetar fácilmente esos sitios, y la edición del ARN de la célula sigue su curso. Cuando las poliaminas son bajas, los guantes se quitan, la fosforilación se dispara y los patrones de empalme cambian, con consecuencias tanto para las células cancerosas como para las células madre. Al definir este mecanismo de “blindaje metabólico” y al proporcionar una molécula herramienta que lo imita selectivamente, el estudio abre la puerta a nuevas formas de modular la lectura génica sin cambiar el ADN mismo, lo que podría inspirar futuras terapias que apunten al empalme en cáncer y medicina regenerativa.
Cita: Zabala-Letona, A., Pujana-Vaquerizo, M., Martinez-Laosa, B. et al. Polyamine-dependent metabolic shielding regulates alternative splicing. Nature 651, 819–828 (2026). https://doi.org/10.1038/s41586-025-09965-1
Palabras clave: poliaminas, empalme alternativo, procesamiento de ARN, señalización metabólica, regulación de células madre