Clear Sky Science · es
Las trayectorias de activación específicas del ligando dictan la señalización de los GPCR en células
Cómo un receptor puede comportarse como muchos interruptores
Muchos de los medicamentos actuales actúan sobre una gran familia de proteínas de la superficie celular llamadas receptores acoplados a proteína G, o GPCR. Estos receptores influyen en la frecuencia cardíaca, el estado de ánimo, la respiración y un sinfín de otras funciones del organismo. Durante décadas se les consideró como simples interruptores de encendido/apagado: un fármaco se une, el interruptor se activa y una señal fluye dentro de la célula. Este artículo muestra que la realidad es mucho más rica. Usando un nuevo tipo de "espía" fluorescente incorporado directamente en un receptor, los autores observan, en células vivas, cómo distintos fármacos envían el mismo receptor por rutas de activación diferentes —como elegir distintas vías a través de una ciudad— para producir patrones distintos de señalización. Entender estas rutas ocultas podría ayudar a diseñar fármacos que proporcionen el beneficio deseado evitando efectos secundarios.
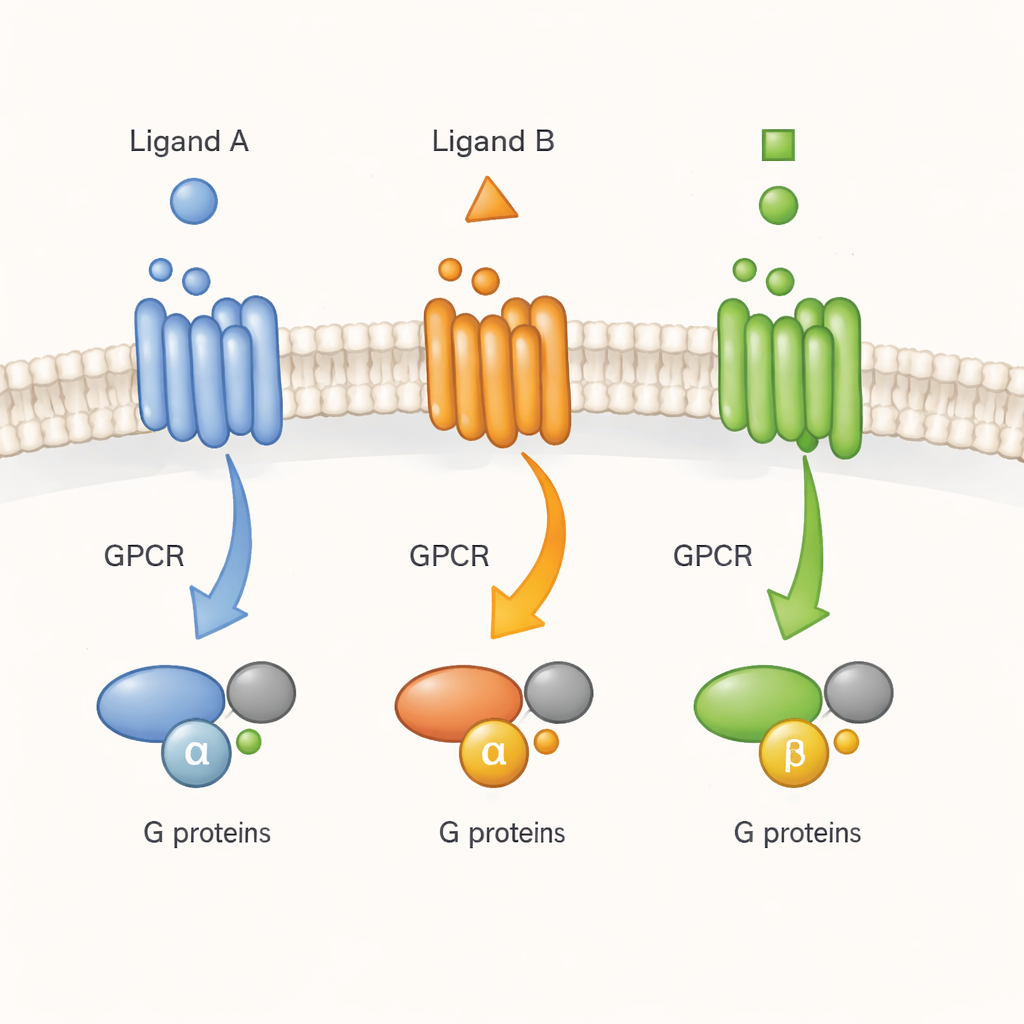
Vigilar el timbre de la célula en tiempo real
Los GPCR a menudo se describen como timbres moleculares: una molécula señal (un ligando) llama desde el exterior y el receptor transmite el mensaje a las proteínas G en el interior. Trabajos previos con receptores purificados en detergentes habían sugerido que los GPCR no se limitan a cambiar entre una sola conformación inactiva y otra activa. En su lugar, exploran muchas conformaciones que los fármacos pueden estabilizar en distinto grado. Pero no estaba claro si la misma complejidad existe en el entorno apretado y dinámico de una célula viva. Aquí, los autores se centran en un receptor representativo, el receptor muscarínico M2 de acetilcolina, un regulador importante de la actividad cardíaca y nerviosa, y preguntan si distintos ligandos lo empujan hacia formas activas diferenciadas que importan para la señalización celular real.
Construir pequeños reporteros luminosos en la superficie del receptor
Para seguir los movimientos del receptor sin alterar su función normal, el equipo usó la expansión del código genético, una tecnología que permite insertar un aminoácido diseñado en posiciones seleccionadas de la superficie externa del receptor. Este "anclaje" químico puede enlazarse mediante click con una pequeña sonda fluorescente en células vivas. Al sondear 72 posiciones y conservar sólo aquellas que seguían comportándose como receptores normales, construyeron un panel de siete variantes del receptor M2, cada una con un único tinte en un sitio distinto del bucle externo. Cuando se aplicó la mensajera natural acetilcolina, el brillo del tinte en esos sitios aumentó o disminuyó de maneras características, revelando cómo cada parte de la superficie externa del receptor se desplazaba al iniciarse la señalización. Crucialmente, estos receptores marcados aún podían activar proteínas G y sufrir una internalización normal, lo que muestra que los reporteros eran fieles y no perturbadores.
Los fármacos dejan "huellas conformacionales" distintas
Los investigadores compararon entonces varios fármacos que activan el receptor M2 pero con diferentes potencias: la propia acetilcolina del organismo, un agonista sintético extremadamente potente llamado iperoxo y dos agonistas parciales más débiles, arecolina y pilocarpina. Cada fármaco produjo un patrón único de cambios de fluorescencia a través de los siete sitios reporteros —una huella conformacional. En la mayoría de las posiciones, la magnitud del movimiento seguía la intensidad con la que el fármaco activaba el receptor. Sin embargo, en dos sitios la relación se invertía: los fármacos más débiles producían los cambios mayores y el fármaco más fuerte casi ninguno. Ese comportamiento no puede explicarse por un único estado activo. En cambio, indica que el mismo receptor, en células vivas, puede adoptar varias formas activas distintas, algunas favorecidas por fármacos fuertes y otras por fármacos débiles.
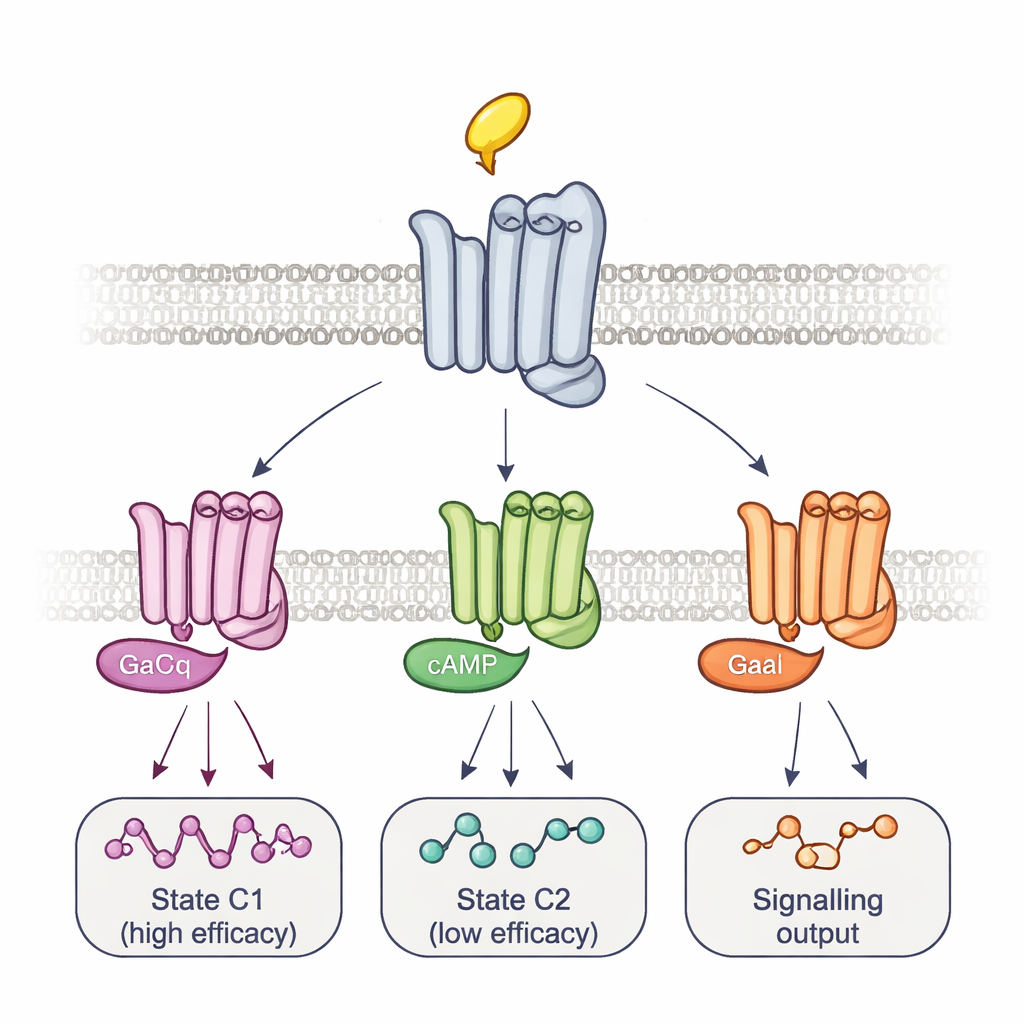
Múltiples complejos y rutas temporizadas hacia la señalización
Para conectar estas conformaciones con la señalización real, el equipo modificó las propias proteínas G. La sobreexpresión de una proteína G mutante que forma complejos muy estables y de larga duración con los receptores borró selectivamente la señal de algunos sitios reporteros mientras potenciaba otros. Este patrón, junto con la cronología de los cambios de fluorescencia, reveló al menos dos complejos principales receptor–proteína G: un complejo de formación rápida y alta eficacia y otro más lento y de baja eficacia. Diferentes fármacos desplazaban el equilibrio entre estos complejos e incluso utilizaban distintos pasos intermedios para alcanzarlos, trazando trayectorias de activación específicas del fármaco. Mediante un ensayo de bioluminiscencia independiente que monitoriza un panel de 14 subtipos de proteínas G, los autores mostraron que estos equilibrios ayudan a determinar no sólo cuán intensamente un fármaco activa la señalización en general, sino qué proteínas G exactas se activan. Por ejemplo, la arecolina activó preferentemente ciertos Go, mientras que la pilocarpina favoreció con fuerza el complejo de baja eficacia.
Por qué esto importa para mejores medicamentos
Para los no especialistas, el mensaje clave es que un único receptor no es sólo un interruptor, sino un conjunto de interruptores relacionados, cada uno accesible por distintas rutas y cada uno conectado a efectos descendentes ligeramente diferentes. Este estudio ofrece una visión directa de esas rutas y estados en células intactas, en lugar de en sistemas simplificados de tubo de ensayo. Al mapear cómo fármacos particulares sesgan el receptor hacia complejos y socios de proteínas G específicos, los investigadores obtienen un plano para diseñar medicamentos "más inteligentes": compuestos que empujen a los receptores hacia estados que desencadenen señales útiles evitando aquellos ligados a efectos secundarios. La estrategia de biosensores fluorescentes desarrollada aquí debería ser adaptable a muchos otros receptores, abriendo una ventana a la coreografía en tiempo real de la acción farmacológica en células vivas.
Cita: Thomas, R., Jacoby, P.S., De Faveri, C. et al. Ligand-specific activation trajectories dictate GPCR signalling in cells. Nature 650, 1053–1062 (2026). https://doi.org/10.1038/s41586-025-09963-3
Palabras clave: Señalización de GPCR, eficacia del ligando, proteínas G, biosensores conformacionales, descubrimiento de fármacos