Clear Sky Science · es
El estrés controla la herencia de la heterocromatina mediante la ubiquitilación de la histona H3
Cómo las células recuerdan el estrés
Nuestras células necesitan mecanismos para «recordar» estreses pasados —como el calor, la falta de nutrientes o la exposición a fármacos— para poder responder con mayor rapidez la próxima vez. Un sistema de memoria poderoso se basa en la heterocromatina, ADN empaquetado de forma compacta que mantiene ciertos genes apagados durante muchas divisiones celulares. Este artículo explora cómo las células ajustan activamente esa memoria en respuesta al estrés, revelando un centro molecular que conecta las señales ambientales con cambios duraderos en la actividad génica. Entender este sistema de control podría ayudar a explicar cómo los hongos desarrollan resistencia a fármacos y cómo el estrés remodela el paisaje epigenético de nuestras propias células.
Un cerrojo sobre el genoma
La heterocromatina puede entenderse como un cerrojo molecular sobre tramos de ADN, que mantiene silenciados los genes próximos. Ese cerrojo se construye a partir de marcas químicas en las histonas, en especial una señal llamada H3K9me3. Una vez establecida, puede copiarse cada vez que se replica el ADN, permitiendo que los patrones de represión génica se hereden sin alterar la secuencia de ADN subyacente. Hasta ahora, la mayor parte de los trabajos sugerían que esta auto‑copia depende principalmente de un bucle de realimentación «leer‑escribir»: un complejo enzimático reconoce las marcas H3K9me3 existentes y añade la misma marca a histonas vecinas, extendiendo gradualmente el dominio silencioso. Pero este modelo no explicaba por completo cómo las condiciones ambientales aceleran, ralentizan o redirigen la expansión de la heterocromatina.
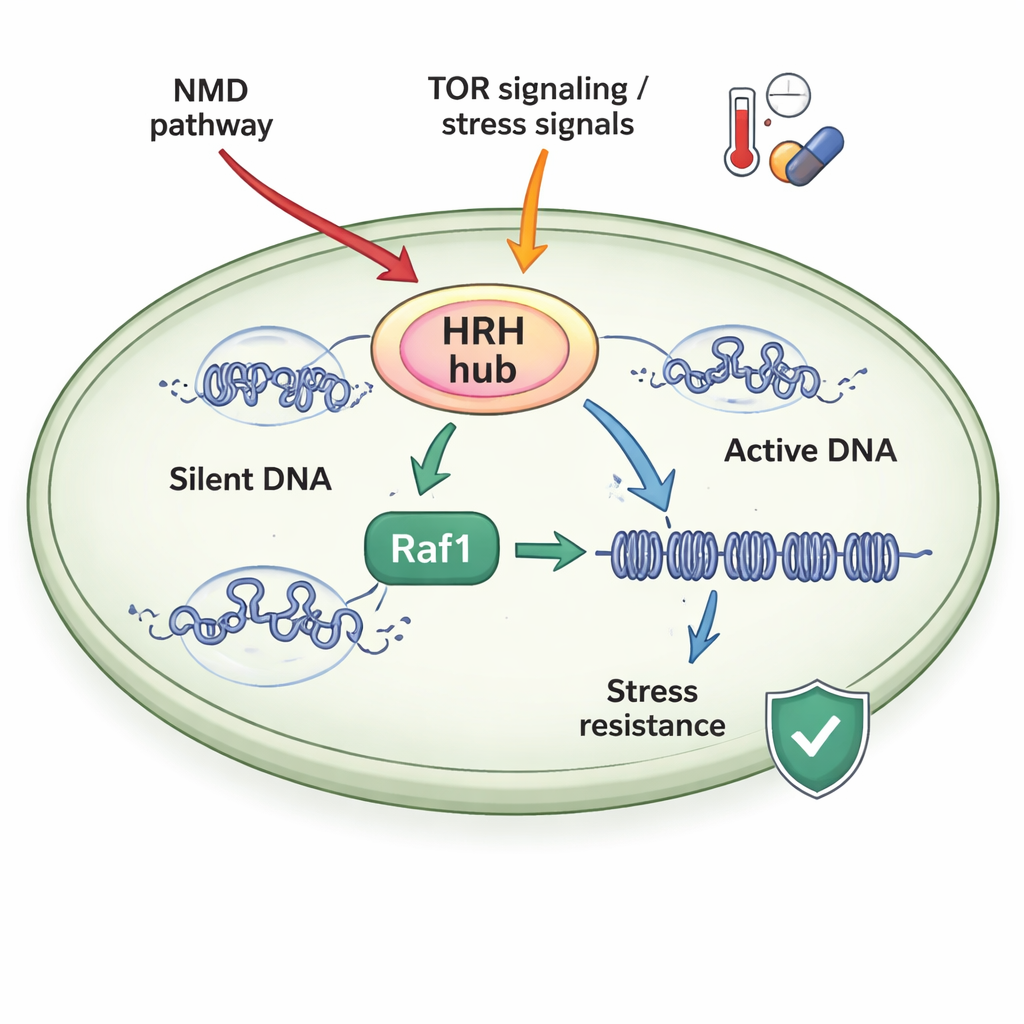
Un centro de control sensible al estrés
Los autores estudiaron la levadura de fisión, un organismo modelo sencillo cuyo aparato de cromatina se parece mucho al de organismos superiores. Se centraron en un complejo llamado ClrC, que tanto escribe la marca H3K9me3 como añade una pequeña proteína, ubiquitina, en otra posición de la histona H3 (H3K14ub). Una subunidad clave de ClrC, Raf1, actúa como «portero» limitante: cuando Raf1 escasea, gran parte de la enzima principal (Clr4) queda libre en lugar de integrarse en el complejo sobre la cromatina, y los dominios silenciosos no logran expandirse. Cuando Raf1 es abundante, se ensamblan más complejos ClrC y se unen de modo estable al ADN, permitiendo que las marcas H3K14ub y H3K9me3 se extiendan a lo largo de los cromosomas y refuercen el silenciado génico.
Ajustar el cerrojo con ubiquitina
Mediante el mapeo de marcas de cromatina a lo largo del genoma, el equipo mostró que H3K14ub está altamente enriquecida donde se forma heterocromatina y que esta marca prácticamente desaparece si se elimina Raf1. Cuando las células portan una mutación que bloquea el paso de añadir ubiquitina (manteniendo H3K9me3 intacta en el punto de origen), los dominios silenciosos no pueden propagarse hacia afuera. En otras palabras, H3K14ub no es meramente decorativa; es necesaria para empujar el frente de la heterocromatina hacia adelante. Experimentos bioquímicos y de imagen revelan por qué: H3K14ub potencia en gran medida la actividad de la enzima Clr4 y ayuda a mantener el complejo estacionado sobre la cromatina, elevando la densidad local de H3K9me3 por encima del umbral necesario para una herencia estable. De forma notable, incrementar los niveles de Raf1 puede sustituir a varios otros factores necesarios normalmente para mantener estos dominios silenciosos, subrayando que la ubiquitilación dirigida por Raf1 es una palanca de control central.
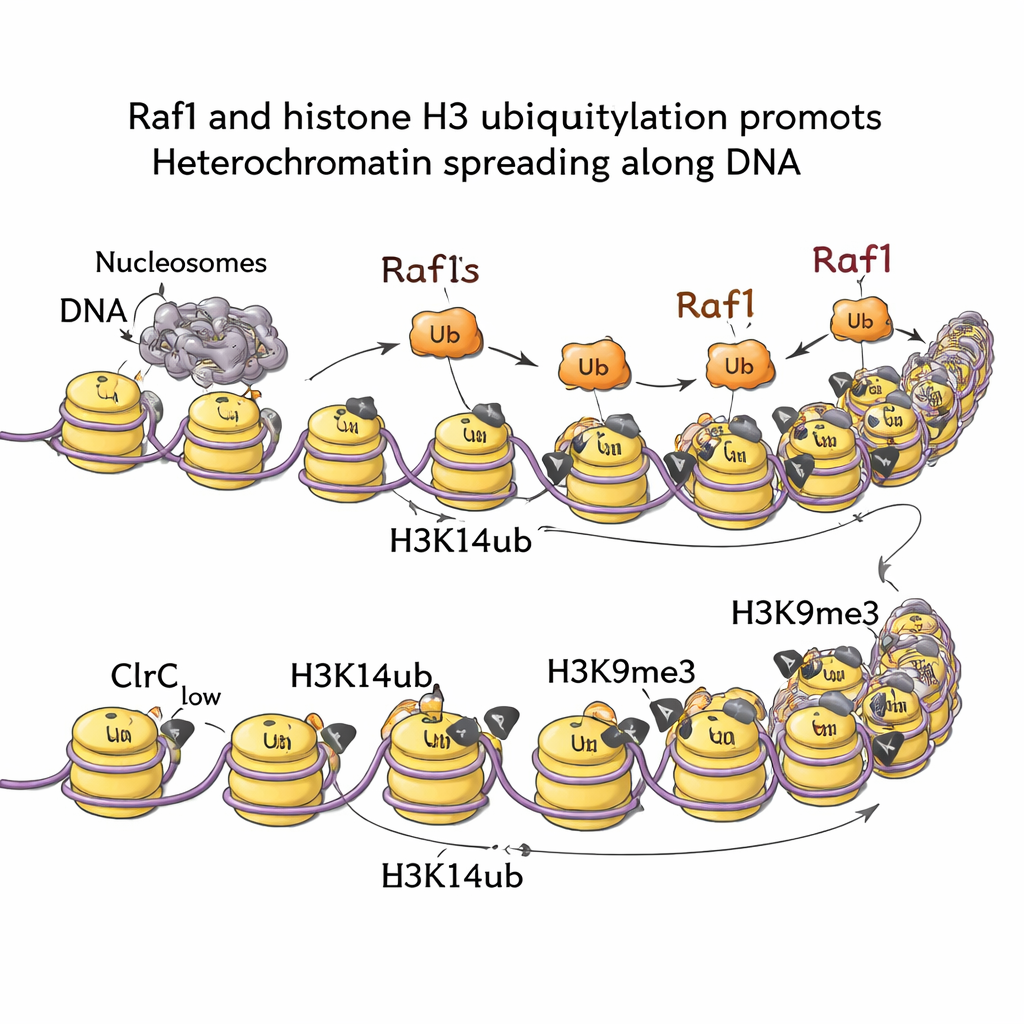
Señales desde la degradación de ARN y vías de crecimiento
Las células no dejan los niveles de Raf1 al azar. El estudio muestra que dos grandes sistemas sensibles al estrés alimentan lo que los autores denominan un centro regulador de la heredabilidad de la heterocromatina (HRH), centrado en Raf1. Primero, la vía de degradación mediada por nonsense (NMD), conocida por destruir ARNm defectuosos, tiene como blanco el ARNm que codifica Raf1, manteniendo bajos los niveles de Raf1 en condiciones normales. Inactivar la NMD estabiliza el ARNm de Raf1, aumenta la abundancia de la proteína Raf1 y restaura la expansión de la heterocromatina en mutantes que de otro modo no pueden mantener dominios silenciosos. Segundo, un sensor de crecimiento y estrés llamado TORC2, actuando a través de la quinasa Gad8, promueve la expresión de Raf1. Las temperaturas altas apagan esta vía, reduciendo los niveles de Raf1, debilitando la heterocromatina y dificultando que las células mantengan estados silenciosos a menos que Raf1 se aumente experimentalmente.
Estrés, resistencia a fármacos e implicaciones más amplias
Los autores conectan entonces este centro molecular con la adaptación en el mundo real. Exponer la levadura a cafeína, un estrés que también se sabe que atenúa la NMD en otros sistemas, eleva los niveles de Raf1 y potencia la expansión de la heterocromatina hacia sitios nuevos, incluidos genes cuyo silenciamiento confiere resistencia a la cafeína y a antifúngicos. De igual modo, las células con Raf1 aumentada artificialmente se vuelven más resistentes al fluconazol y al clotrimazol, agentes antifúngicos comunes. Por el contrario, cuando Raf1 se reduce —por calor o por pérdida de la señalización TORC2–Gad8— la heterocromatina se vuelve inestable y la memoria epigenética se desvanece, a menos que Raf1 sea restaurado. Dado que proteínas similares a Raf1, el complejo ClrC y la marca H3K14ub tienen homólogos en hongos patógenos y en mamíferos, estos hallazgos sugieren que un centro epigenético sensor del estrés similar podría modelar la resistencia a fármacos, el desarrollo y la enfermedad en muchas especies.
Por qué importa esto
En términos cotidianos, este trabajo muestra que el silenciado génico por cromatina no es un cerrojo rígido sino un sistema inteligente y ajustable. Las células usan un centro central para leer las señales ambientales —cambios de temperatura, estado nutritivo, estreses químicos— y ajustar los niveles de Raf1. Eso, a su vez, gobierna cuánto del genoma queda envuelto en silencio duradero y cuán fácilmente las células pueden «reprogramarse» sin mutar su ADN. Al descubrir el papel clave de la ubiquitilación de la histona H3 y de la dosis de Raf1 en este proceso, el estudio proporciona un plan de cómo el estrés puede remodelar rápidamente el paisaje epigenético —y apunta a nuevas formas de influir en la resistencia a fármacos en hongos o en el silenciamiento génico aberrante en enfermedades humanas.
Cita: Bhatt, B., Wei, Y., Pradhan, A.K. et al. Stress controls heterochromatin inheritance via histone H3 ubiquitylation. Nature 650, 768–778 (2026). https://doi.org/10.1038/s41586-025-09899-8
Palabras clave: heterocromatina, herencia epigenética, ubiquitinación de histonas, adaptación al estrés, resistencia fúngica a fármacos