Clear Sky Science · es
Resolución de la integridad estructural y la farmacocinética del origami de ADN in vivo
Observando pequeñas máquinas de ADN dentro del cuerpo
El ADN puede plegarse como papel en diminutas formas tridimensionales, una técnica conocida como origami de ADN. Estas nanoestructuras pueden programarse para transportar fármacos, vacunas o moléculas señalizadoras con una precisión exquisita. Pero una vez inyectadas en el cuerpo, ¿permanecen lo bastante intactas para funcionar o se deshacen rápidamente? Este artículo presenta una nueva forma de observar estas máquinas de ADN en acción dentro de animales vivos, revelando cuánto tiempo sobreviven, cómo viajan por el torrente sanguíneo e incluso qué partes de cada estructura se rompen primero.
Por qué plegar ADN podría cambiar la medicina
El origami de ADN aprovecha las mismas reglas de apareamiento de bases que almacenan nuestra información genética, pero las reutiliza para construir objetos a escala nanométrica. Los investigadores pueden colocar proteínas, fármacos o señales que estimulan el sistema inmunitario sobre estos objetos como clavijas en una placa de Lego, creando terapias muy controladas contra el cáncer, enfermedades autoinmunes e infecciones. Para que esos tratamientos precisos sean seguros y eficaces, reguladores y científicos deben saber cuán intactas permanecen estas estructuras en el cuerpo y con qué rapidez se eliminan, aspecto conocido en conjunto como su farmacocinética. Los métodos de seguimiento existentes suelen añadir tintes fluorescentes o simplemente contar fragmentos de ADN, lo que puede hacer que los escombros desensamblados parezcan nanoestructuras completamente intactas. Hasta ahora, no había una manera práctica de saber, en animales vivos, si las formas originales de origami de ADN siguen enteras.
Una “prueba de integridad” molecular para el origami de ADN
El equipo desarrolló un método que llama PLASTIQ, siglas de proximity ligation assay for structural tracking and integrity quantification (ensayo de ligación por proximidad para seguimiento estructural y cuantificación de integridad). La idea clave es permitir que el propio origami de ADN informe sobre su estado. En posiciones específicas de cada estructura, los investigadores colocan pares de pequeñas grapas de ADN que quedan adyacentes a lo largo de una hélice cuando el origami está correctamente plegado. Una de cada par porta una pequeña etiqueta química que permite que se unan enzimáticamente, o liguen, pero solo si siguen mantenidas juntas por una hebra de andamiaje intacta. Si la estructura se deshace, se rompe o es degradada por enzimas, esas dos piezas se separan y ya no pueden ligarse. Tras la ligación, los pares unidos se amplifican usando la reacción en cadena de la polimerasa estándar y se cuantifican mediante qPCR sensible o secuenciación, convirtiendo la presencia de segmentos locales intactos en señales medibles a partir de apenas microlitros de sangre.
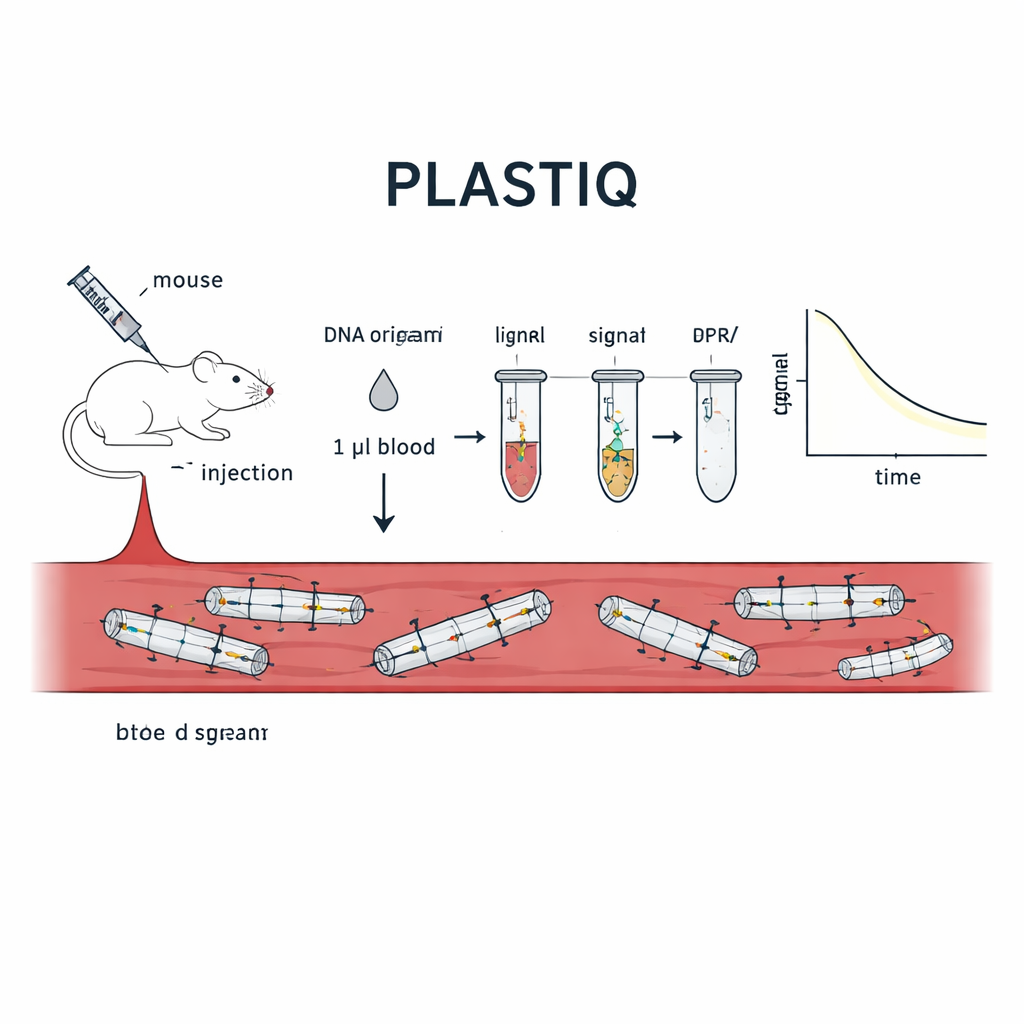
Poniendo la prueba a trabajar en ratones vivos
Para demostrar que PLASTIQ realmente mide la integridad estructural, los autores lo aplicaron primero a diseños simples de origami de ADN en forma de varilla en tubos de ensayo. Las señales aparecían solo cuando las varillas estaban intactas y desaparecían tras el desdoblamiento por calor, mientras que los ensayos de ADN más tradicionales seguían detectando ADN independientemente de la forma. Luego inyectaron estas varillas en ratones por distintas vías: directamente en el torrente sanguíneo, en la cavidad abdominal, en el músculo y bajo la piel, y llegaron a tomar tan solo un microlitro de sangre en distintos momentos. PLASTIQ mostró cómo la concentración de estructuras intactas subía y luego caía según la vía de inyección, coincidiendo con las expectativas generales de la farmacología de fármacos pero con un detalle estructural mucho más fino. El método fue sensible hasta 0,01 femtomolar y requirió una cantidad mínima de sangre, lo que permitió muestreos repetidos del mismo animal a lo largo de horas.
Probando recubrimientos protectores y puntos débiles ocultos
Muchos grupos intentan proteger el origami de ADN recubriéndolo con polímeros como PEG, entrecruzando hebras con luz ultravioleta o añadiendo ligandos químicos, pero ha sido difícil saber cuánto ayudan realmente estas tretas in vivo. Usando PLASTIQ, los autores demostraron que las varillas recubiertas con PEG en la sangre permanecen intactas algo más de tiempo que las desnudas, pero también se eliminan más rápido una vez en circulación, y que el recubrimiento no impide que las enzimas de PLASTIQ realicen su función. Al combinar PLASTIQ con modelos matemáticos sencillos, extrajeron tasas de absorción y eliminación para distintas vías de inyección y recubrimientos, e incluso pudieron simular regímenes de dosificación repetida. Luego llevaron el método más allá con un origami en forma de barril de doble capa, más densamente empaquetado por dentro que por fuera. Las mediciones PLASTIQ mostraron que las grapas en la superficie exterior expuesta perdían integridad más rápido que las orientadas hacia la cavidad interior, confirmando directamente que las hélices enterradas están protegidas de las enzimas degradantes en la sangre.
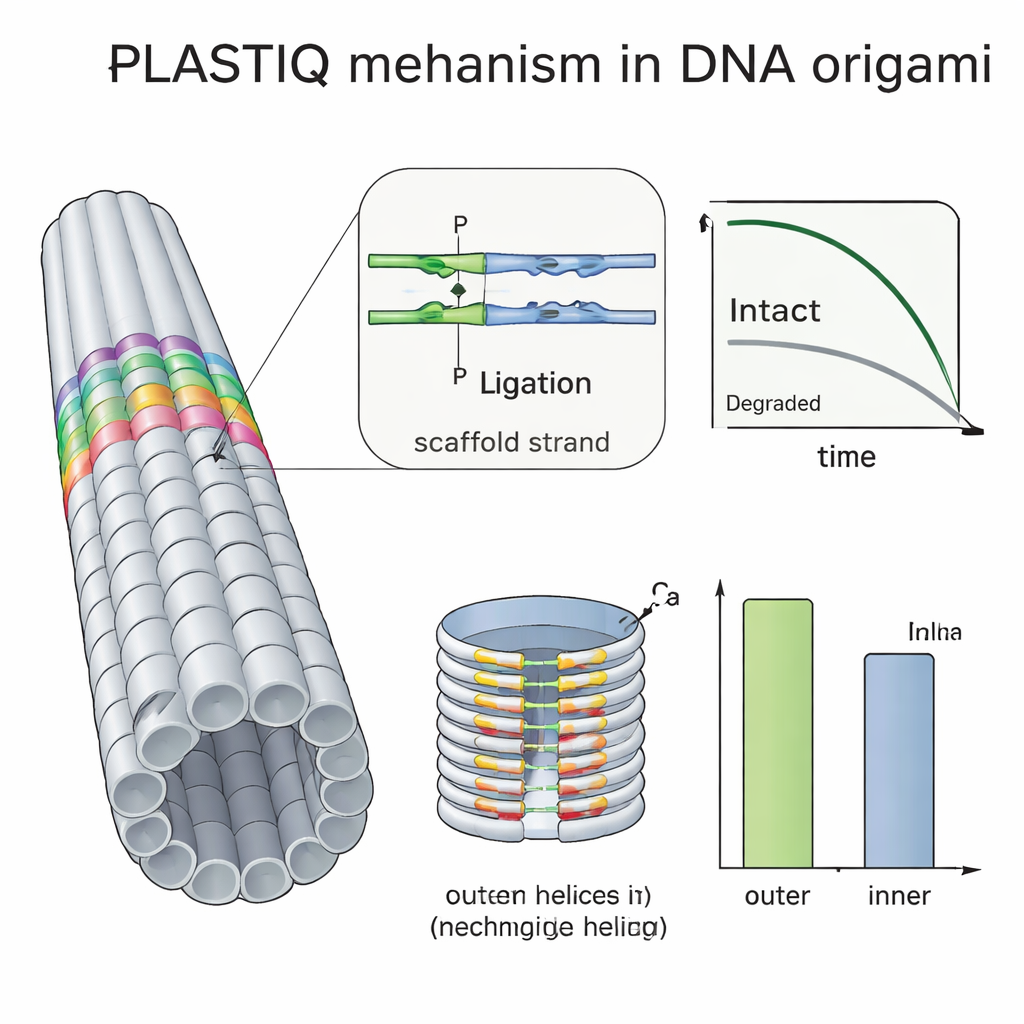
Qué significa esto para futuras terapias basadas en ADN
Para un no especialista, PLASTIQ puede verse como un chequeo estructural para dispositivos de ADN a escala nanométrica que viajan por el cuerpo. En lugar de limitarse a preguntar “¿hay ADN aquí?”, pregunta “¿está este ADN todavía plegado en el objeto preciso que diseñamos?”. Al responder a esa pregunta con alta sensibilidad a partir de pequeñas muestras de sangre, PLASTIQ ofrece a los desarrolladores de fármacos una forma de optimizar el diseño, el recubrimiento y la dosificación de medicamentos y vacunas basados en origami de ADN. Con el tiempo, este tipo de visión detallada y cuantitativa sobre cómo se comportan estas nanoestructuras en entornos biológicos reales podría ayudar a convertir el origami de ADN de un elegante concepto de laboratorio en terapias fiables y aptas para la regulación.
Cita: Wang, Y., Rocamonde-Lago, I., Waldvogel, J. et al. Resolving DNA origami structural integrity and pharmacokinetics in vivo. Nat. Nanotechnol. 21, 268–276 (2026). https://doi.org/10.1038/s41565-025-02091-z
Palabras clave: Origami de ADN, nanomedicina, administración de fármacos, farmacocinética, nanotecnología