Clear Sky Science · es
La interrupción de la triptofanasa promueve el mutualismo insecto–bacteria
Cómo los pequeños socios intestinales pueden forjar o arruinar un insecto
Muchos animales, incluidos los humanos, dependen de billones de microbios que viven en sus intestinos. Estos socios ocultos pueden ayudar a digerir los alimentos, sintetizar vitaminas o, en algunos casos, enfermarnos. Este estudio examina un ajuste genético sencillo pero sorprendente en bacterias que convierte a un microbio ordinario en un compañero que salva la vida de una chinche fitófaga. Al enfocar la atención en un único gen bacteriano, el trabajo revela cómo un cambio microscópico puede poner en marcha una amistad estable entre formas de vida muy distintas.
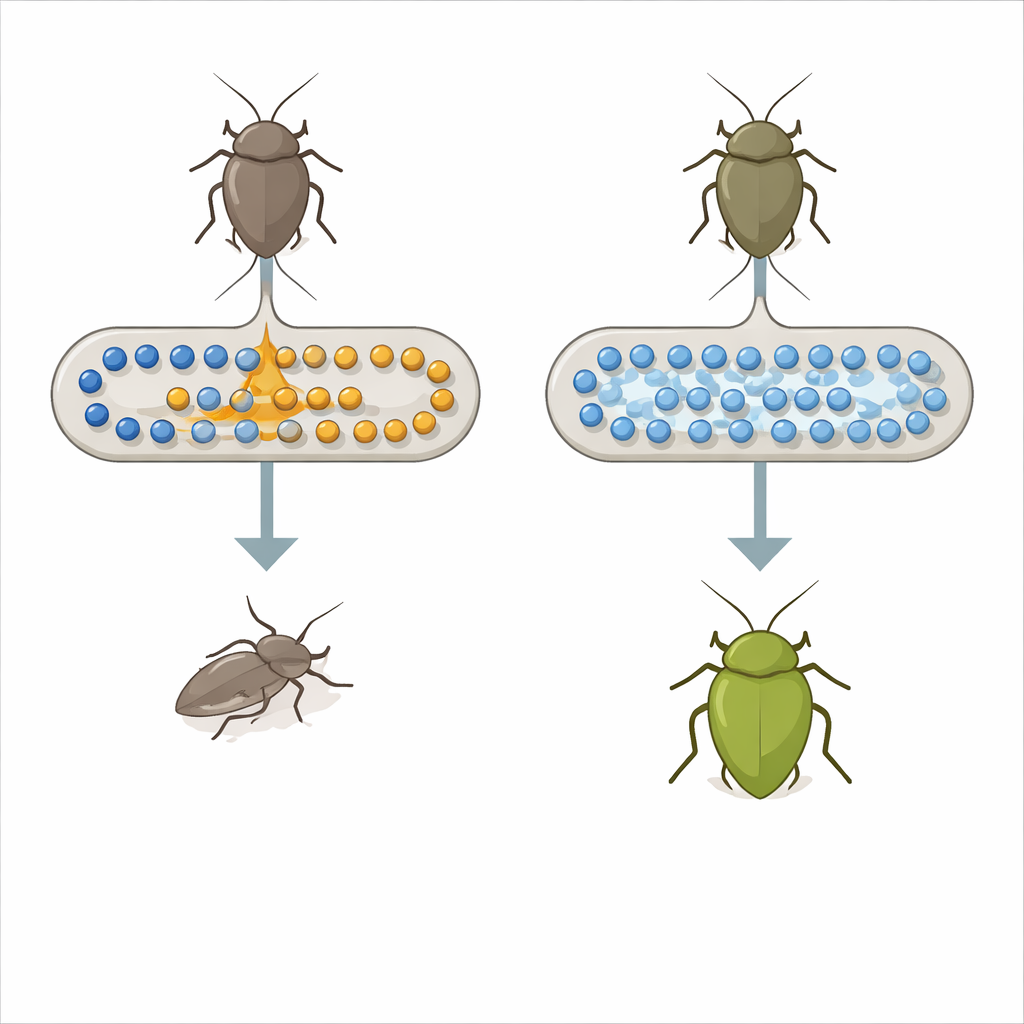
Una chinche, una bacteria y una alianza improbable
La chinche Plautia stali depende de bacterias especiales que viven en una bolsa del intestino medio para crecer y sobrevivir. En la naturaleza, estos socios suelen pertenecer al género Pantoea, que suministra nutrientes que el insecto no puede obtener solo de la savia vegetal. Trabajos de laboratorio ya habían mostrado que una cepa común de laboratorio de Escherichia coli, una típica bacteria intestinal de mamíferos, puede evolucionar rápidamente hasta convertirse en un socio útil para esta chinche tras una sola mutación en un sistema de control global llamado represión por catabolitos de carbono. Ese hallazgo anterior planteó una gran pregunta: ¿es realmente ese cambio regulatorio drástico la forma en que surgen las simbiosis útiles en la naturaleza, o existe un interruptor genético más específico?
Siguiendo la pista de un solo bloque de construcción
Para responder, los investigadores compararon chinches portadoras de E. coli ordinaria con otras portadoras de mutantes de E. coli evolucionados y beneficiosos. Midieron muchas moléculas pequeñas en la sangre y el intestino del insecto. Un aminoácido esencial, el triptófano, destacó: sus niveles fueron más de diez veces superiores en los insectos hospedando a los mutantes beneficiosos que en aquellos con E. coli normal. Entre las docenas de genes bacterianos afectados por la mutación regulatoria previa, dos estaban vinculados al procesamiento del triptófano. Uno, llamado tnaA, codifica una enzima que descompone el triptófano en un compuesto denominado indol junto con otros subproductos; el otro ayuda a transportar el triptófano hacia el interior de la célula. Cuando el equipo eliminó el gen tnaA de E. coli, las chinches de repente mejoraron mucho, con mayor supervivencia y un color corporal verde intenso característico de insectos sanos y bien nutridos.
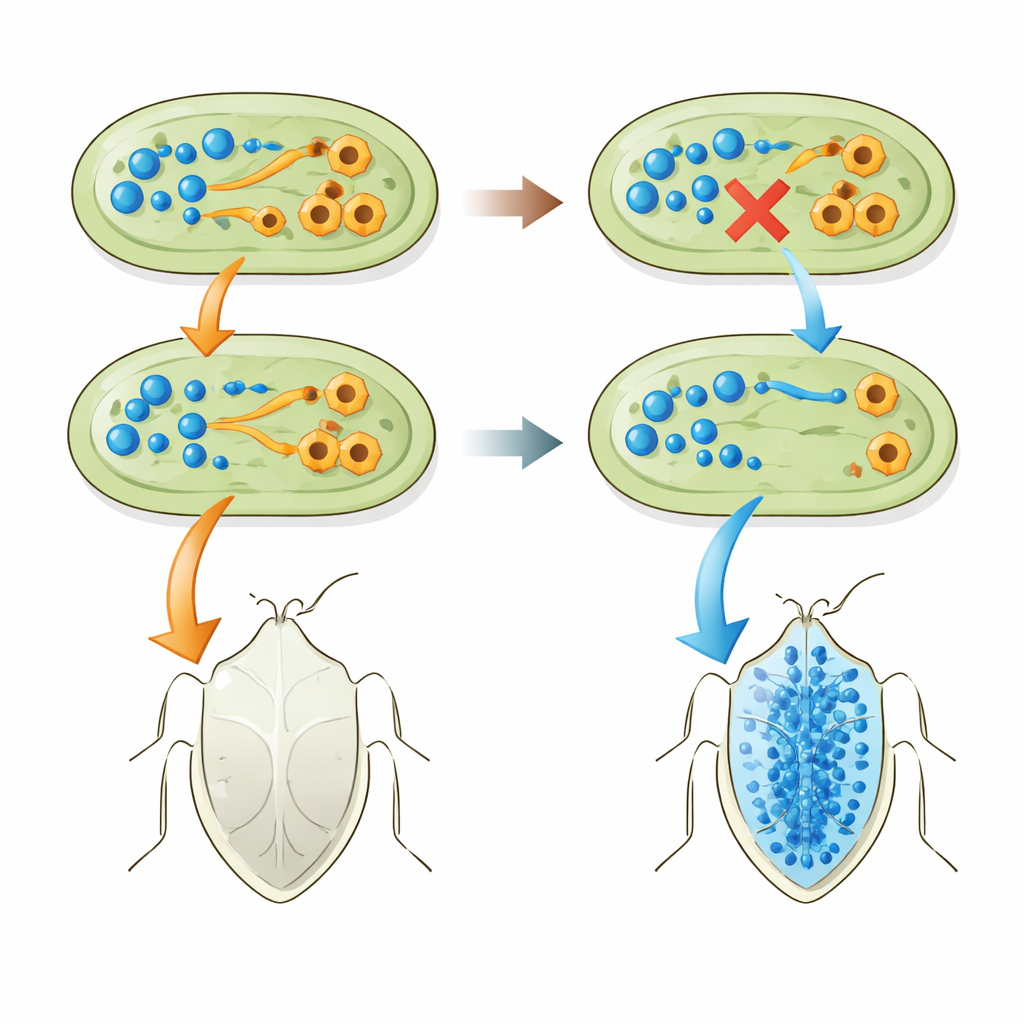
Cuando destruir menos significa ayudar más
El cambio clave no fue que las bacterias produjeran más triptófano, sino que dejaron de destruirlo y de generar indol en exceso. Los insectos que albergaban E. coli deficiente en tnaA tenían mucho triptófano y casi nada de indol circulando en sus cuerpos. En contraste, los insectos con E. coli normal presentaban poco triptófano y niveles mucho más altos de indol. Experimentos de alimentación apoyaron este panorama: administrar indol en el agua de bebida perjudicó a los insectos, especialmente a los que tenían bacterias productoras de indol, mientras que un exceso de triptófano solo fue dañino cuando las bacterias podían convertirlo en más indol. Una cepa separada de E. coli diseñada para sobreproducir triptófano dio a las chinches un impulso modesto, lo que refuerza la idea de que más de este bloque de construcción, y menos producto de degradación tóxico, mejora la salud del insecto.
Los socios naturales comparten la misma pérdida genética
El equipo preguntó entonces si esa misma pérdida génica aparece en las simbiosis del mundo real. Secuenciaron genomas de muchas bacterias Pantoea que viven dentro de P. stali y chinches relacionadas en las islas Ryukyu de Japón, así como cepas de Pantoea aisladas del suelo que podían inducirse a ayudar a las chinches. De forma llamativa, todo simbionte exitoso o potencialmente exitoso carecía del gen tnaA y no mostraba actividad de la enzima que rompe el triptófano. En contraste, varias cepas de Pantoea ananatis de vida libre que aún tenían tnaA no pudieron sostener en absoluto el desarrollo de las chinches. Cuando los investigadores eliminaron tnaA en una de esas cepas de P. ananatis, su capacidad para ayudar a los insectos mejoró, aunque no alcanzó el nivel de los socios naturales. Y cuando forzaron a un simbionte natural a portar un operón tnaA activo, los insectos empeoraron y presentaron menor triptófano y mayor indol en su sangre.
Qué significa esto para las alianzas ocultas de la vida
En conjunto, los resultados apuntan a una regla simple pero poderosa: las bacterias que dejan de descomponer el triptófano, y por tanto evitan inundar a su huésped con indol, tienen más probabilidad de convertirse en parejas fiables para chinches fitófagas. En el laboratorio, esto puede desencadenarse por una mutación en un sistema regulador global; en la naturaleza, se manifiesta como la pérdida directa del gen que escinde el triptófano. De una u otra forma, apagar esa única enzima ayuda a alinear los intereses del insecto y del microbio. El estudio sugiere que el paso de una asociación laxa a un mutualismo estrecho puede a veces depender de pasos genéticos sorprendentemente pequeños, y que pérdidas funcionales similares en el metabolismo bacteriano pueden subyacer muchas otras alianzas ocultas a lo largo del árbol de la vida.
Cita: Wang, Y., Moriyama, M., Koga, R. et al. Tryptophanase disruption promotes insect–bacterium mutualism. Nat Microbiol 11, 759–769 (2026). https://doi.org/10.1038/s41564-026-02264-z
Palabras clave: microbioma de insectos, mutualismo bacteriano, metabolismo del triptófano, evolución de la simbiosis, simbiontes Pantoea