Clear Sky Science · es
La vacunación con ARNm supera la alteración mediada por hemozoin de las vacunas antipalúdicas de parásito entero en ratones
Por qué la malaria previa hace que las vacunas sean menos eficaces
La malaria causa la muerte de cientos de miles de personas cada año, y una de las vacunas más prometedoras utiliza parásitos enteros debilitados para entrenar al sistema inmunitario. Sin embargo, curiosamente, este enfoque “estándar de oro” funciona mucho mejor en personas que nunca han tenido malaria que en aquellas que crecieron en zonas donde la enfermedad es común. Este estudio, realizado en ratones, plantea una pregunta simple pero crucial: ¿qué tiene la infección previa por malaria que hace que una vacuna muy eficaz de repente falle—y puede un nuevo tipo de vacuna de ARNm solucionar el problema?
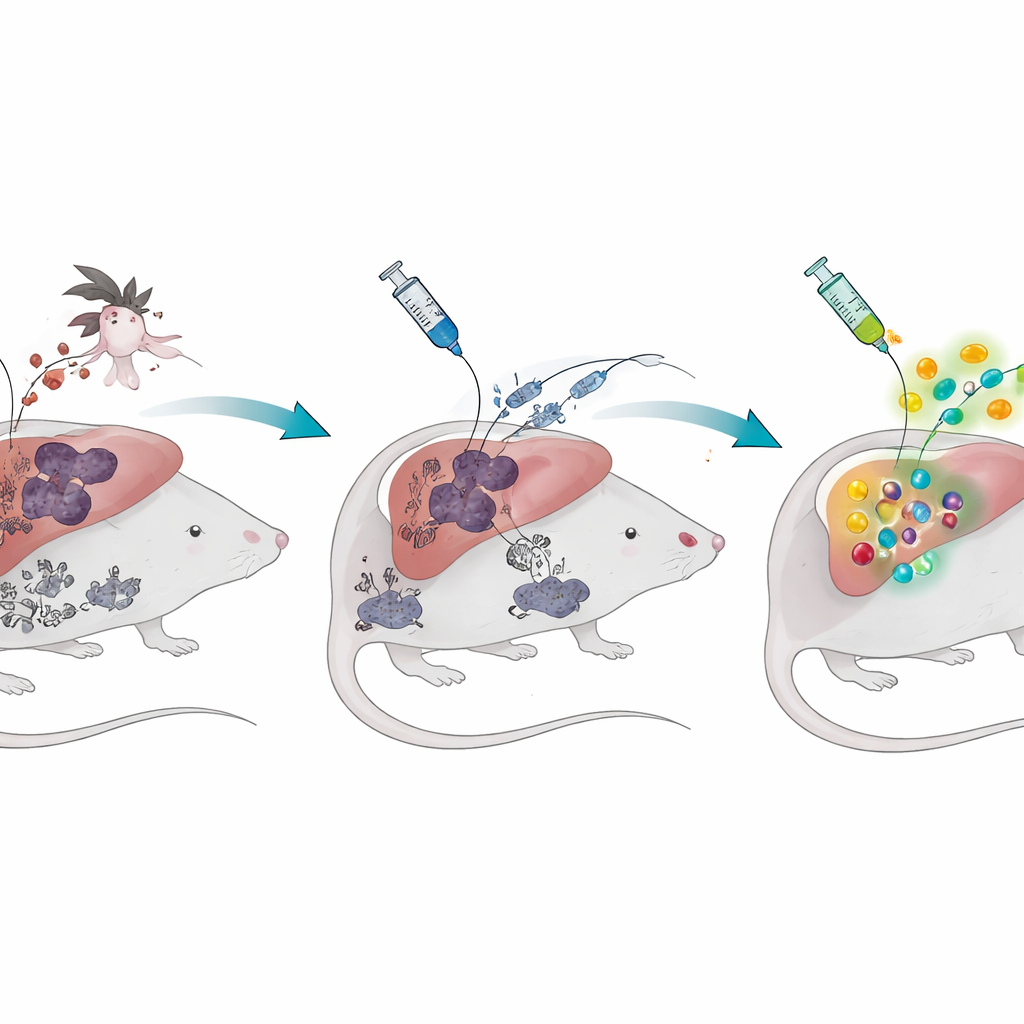
La historia de dos fases de la malaria
El parásito de la malaria tiene dos etapas principales en el cuerpo humano. Primero, tras la picadura de un mosquito, infecta silenciosamente el hígado. Más tarde, invade los glóbulos rojos, provocando fiebre y enfermedad. Las vacunas de parásito entero llamadas esporozoítos atenuados por radiación se dirigen a la silenciosa fase hepática: los parásitos entran en las células del hígado pero no pueden completar su ciclo vital, ofreciendo al sistema inmunitario una vista previa segura. En ratones no expuestos a la malaria, esta estrategia genera gran número de células T citotóxicas especializadas que se establecen en el hígado y pueden eliminar los parásitos antes de que causen enfermedad. Pero cuando los investigadores infectaron primero a los ratones con malaria en fase sanguínea y dejaron que se resolviera, la misma vacuna produjo muchas menos células T protectoras, y los animales estuvieron mucho menos protegidos al ser desafiados con parásitos vivos.
Un pigmento persistente que no desaparece
El equipo preguntó entonces qué era diferente en estos ratones “con experiencia en malaria”. Un sospechoso destacado fue el hemozoin, un pigmento oscuro y cristalino que el parásito fabrica dentro de los glóbulos rojos para desintoxicar los desechos ricos en hierro resultantes de la digestión de la hemoglobina. Este pigmento no desaparece cuando la infección se resuelve; puede permanecer en el hígado, el bazo y la médula ósea durante muchos meses. Los científicos encontraron que incluso más de un año después de que hubiese terminado una infección en fase sanguínea, los ratones todavía mostraban hemozoin almacenado y una respuesta de células T debilitada frente a la vacuna dirigida a la fase hepática. Administrar a ratones sanos hemozoin sintético purificado por sí solo—sin ningún parásito vivo—fue suficiente para imitar esta debilidad vacunal duradera y reducir la protección frente a un posterior desafío con malaria.
Cómo el hemozoin entorpece a las centinelas inmunitarias
Investigando más a fondo, los investigadores se centraron en las células dendríticas, las centinelas del sistema inmunitario que recogen fragmentos de patógenos y los presentan a las células T. Para que la vacuna de parásito entero dirigida al hígado funcione, las células dendríticas deben capturar material del parásito procedente de células hepáticas infectadas y mostrárselo a las células T citotóxicas. En experimentos en cultivo celular, el equipo demostró que el hemozoin interfiere directamente con este paso de captura: cuanto más hemozoin habían estado expuestas las células dendríticas, menos eficientemente fagocitaban antígenos proteicos. Este defecto apareció tanto en células de ratón como en células inmunitarias humanas derivadas de donantes de sangre, y no dependía de un sensor inflamatorio bien conocido, lo que sugiere que el hemozoin actúa por sí mismo como un obstáculo físico o bioquímico para el manejo normal de antígenos.
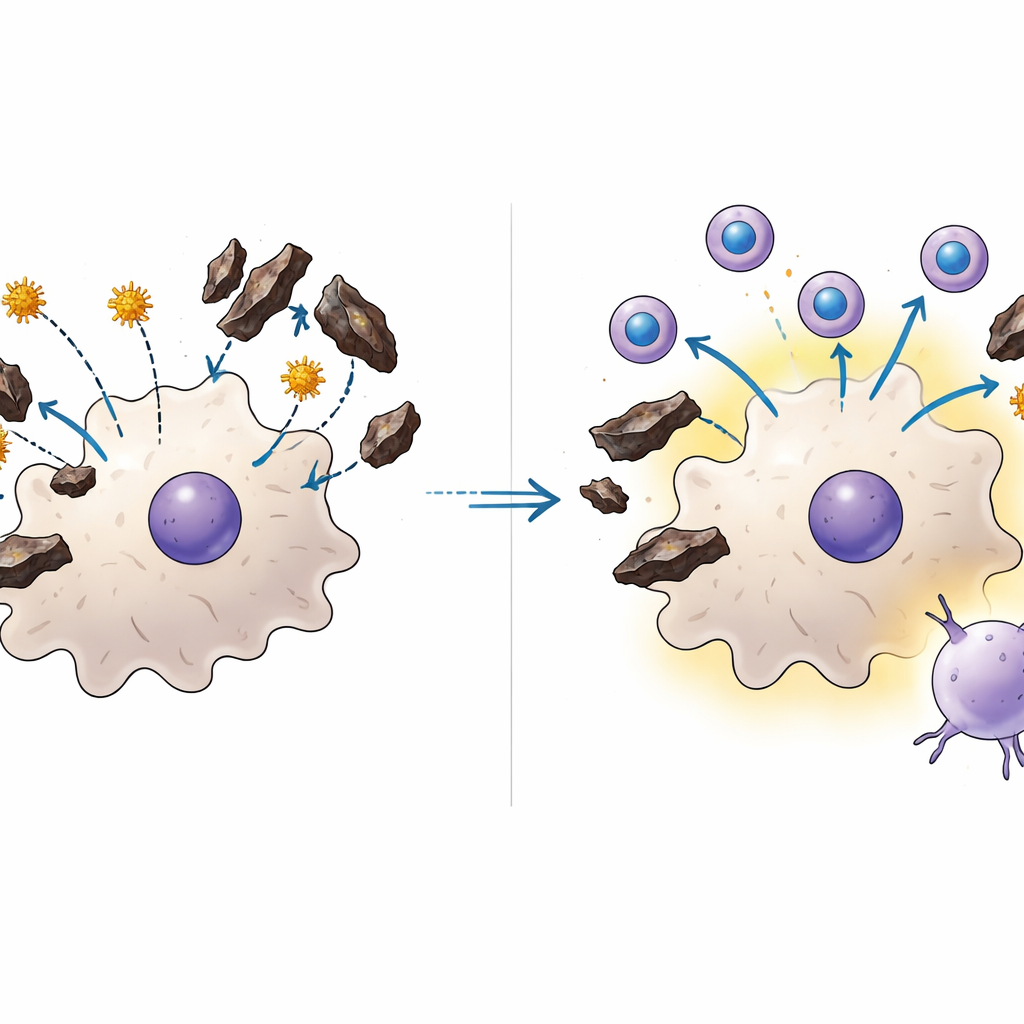
Las vacunas de ARNm encuentran una vía alrededor del obstáculo
Para ver si un formato vacunal diferente podría sortear este problema, los científicos diseñaron una vacuna de ARNm empaquetada en nanopartículas lipídicas. En lugar de aportar proteínas del parásito desde el exterior, este enfoque da a las células del huésped instrucciones genéticas para fabricar dentro de la célula fragmentos cortos de varias proteínas parasitarias. En ratones con o sin malaria previa, la vacuna de ARNm generó respuestas de células T citotóxicas igualmente potentes y mejoró el control de la infección hepática. De forma llamativa, cuando la vacuna de ARNm se combinó con una única dosis de la vacuna de parásito entero para el hígado, los ratones desarrollaron piscinas especialmente grandes de células T que tomaron residencia a largo plazo en el hígado—una población celular conocida por ser clave para la protección rápida. En cultivos, el hemozoin no bloqueó la captación ni la función de las nanopartículas cargadas de ARNm, lo que explica cómo esta estrategia puede tener éxito donde la vacuna tradicional por sí sola fracasa.
Qué significa esto para futuras vacunas contra la malaria
En términos cotidianos, el estudio muestra que las infecciones previas por malaria dejan residuos microscópicos parecidos a minerales que obstruyen la forma en que ciertas células inmunitarias aprenden normalmente de las vacunas, debilitando una de las vacunas de parásito entero líderes. Pero al cambiar a, o combinar con, una vacuna basada en ARNm que introduce disimuladamente las instrucciones para piezas del parásito directamente en las células, los científicos pueden sortear esos residuos y restaurar una protección fuerte en huéspedes con experiencia en malaria—al menos en ratones. El trabajo señala al hemozoin como un obstáculo importante para las vacunas en personas que viven en regiones endémicas, y sugiere que regímenes vacunales cuidadosamente diseñados con ARNm o combinados podrían ser una vía prometedora hacia una inmunización antipalúdica más eficaz y de amplia utilidad.
Cita: Hassert, M., Drewry, L.L., Pewe, L.L. et al. mRNA vaccination overcomes haemozoin-mediated impairment of whole-parasite malaria vaccines in mice. Nat Microbiol 11, 718–730 (2026). https://doi.org/10.1038/s41564-026-02263-0
Palabras clave: vacunas contra la malaria, hemozoin, vacuna de ARNm, inmunidad mediada por células T, infección por Plasmodium