Clear Sky Science · es
Sitios iniciales del rebrote de SIV tras la interrupción del tratamiento antirretroviral en macacos rhesus
Por qué vuelve el virus
Los medicamentos modernos contra el VIH pueden reducir la cantidad de virus en la sangre hasta niveles tan bajos que las pruebas estándar no detectan nada. Sin embargo, cuando se interrumpe el tratamiento, el virus casi siempre regresa. Este estudio en macacos rhesus, infectados con un virus emparentado con el VIH llamado SIV, plantea una pregunta básica pero crucial: ¿dónde, exactamente, surge la primera chispa de este rebrote viral dentro del cuerpo, y qué tipos de tejidos la avivan?
Siguiendo códigos de barras virales
Para rastrear el virus con una precisión poco habitual, los investigadores usaron un SIV especial en el que cada partícula viral lleva un “código de barras” genético único: una secuencia corta e inofensiva que actúa como número de serie. Veinticuatro macacos fueron infectados con una mezcla de miles de estos virus codificados y, rápidamente, se les inició un potente régimen antirretroviral de tres fármacos. Los medicamentos redujeron el virus en sangre a niveles esencialmente indetectables y lo mantuvieron así durante más de un año, imitando una terapia efectiva a largo plazo en personas con VIH. Como cada código marcaba una familia viral distinta, el equipo pudo identificar más tarde qué linajes virales específicos se reactivaron cuando se suspendió el tratamiento y dónde en el cuerpo tuvo lugar ese despertar.
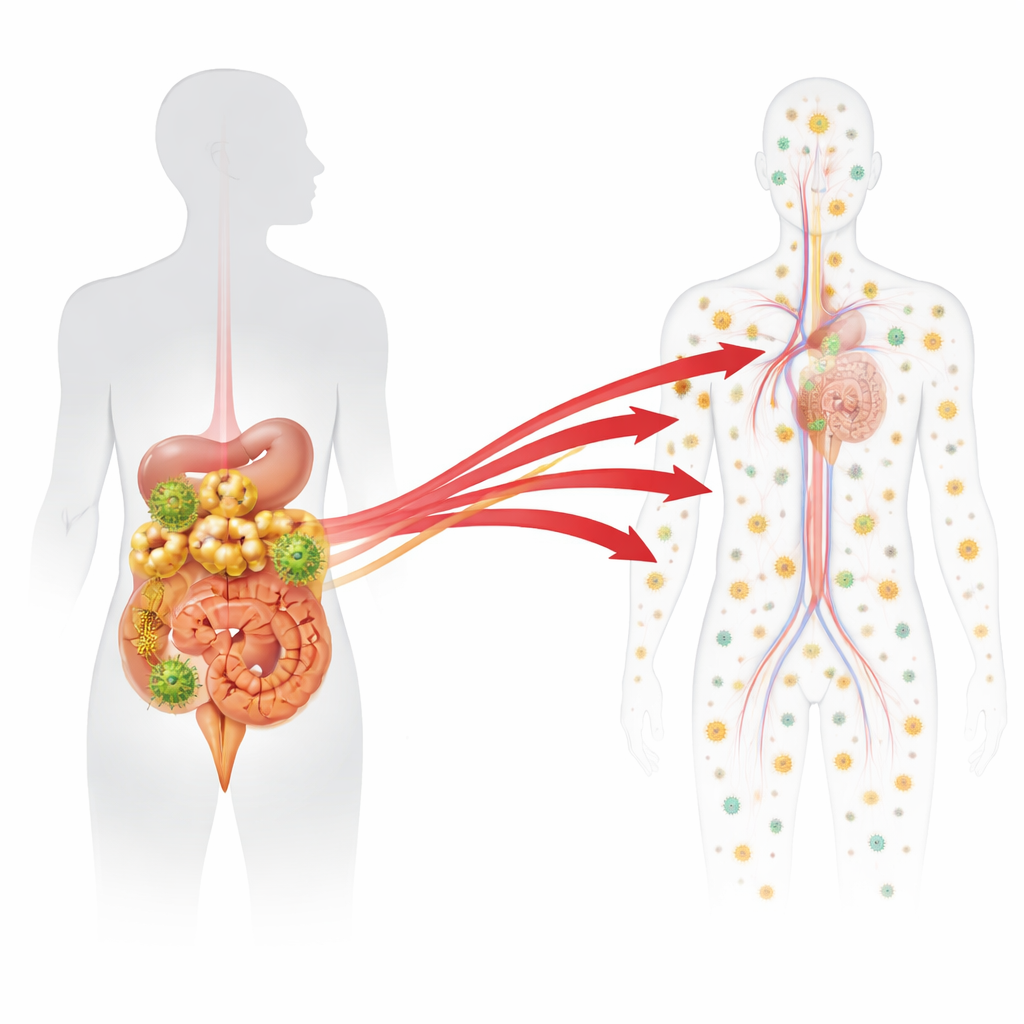
Explorando los tejidos durante y después del tratamiento
Al final del prolongado periodo de tratamiento, los macacos se dividieron en grupos. Algunos fueron examinados mientras seguían con la terapia para definir el patrón de fondo normal de pequeñas cantidades de material genético viral que persisten a pesar de los fármacos. A otros se les interrumpió el tratamiento y se examinaron ya sea cinco o siete días después, antes o justo cuando el virus empezaba a reaparecer en la sangre. De cada animal, los científicos recogieron y analizaron alrededor de 90 muestras de tejidos que abarcaban el intestino, muchos tipos de ganglios linfáticos, órganos formadores de sangre como la médula ósea y órganos no inmunitarios como el hígado y el pulmón. En cada tejido midieron cuánto ADN viral (señal de células infectadas) y ARN viral (señal de producción activa de virus) estaba presente para cada código de barras. Luego emplearon modelos estadísticos para señalar cualquier código cuya cantidad de ARN en un tejido particular aumentara muy por encima de lo esperado por la mera actividad de fondo de bajo nivel observada durante el tratamiento.
Localizando las primeras chispas del rebrote
Esos códigos inusualmente activos, que los investigadores denominaron “atípicos”, identificaron linajes virales que probablemente estaban experimentando nuevos estallidos de replicación y propagación local tras la retirada de los fármacos. En todos los animales, identificaron 32 códigos atípicos. De forma crucial, cuando el virus reapareció en la sangre, aproximadamente la mitad de los códigos detectados en plasma coincidían con esos atípicos en los tejidos, vinculando directamente sitios tisulares específicos con la etapa más temprana del rebrote sistémico. La mayoría de los atípicos aparecieron en una sola muestra de tejido, coherente con un punto de inicio muy localizado, mientras que una fracción menor ya se había extendido a segmentos intestinales vecinos y a sus ganglios linfáticos de drenaje. Solo en el único animal con niveles claramente mayores de virus en sangre el equipo observó evidencia de que múltiples tejidos —incluyendo sitios distantes— ya habían sido resembrados. Esto sugiere una progresión por etapas: primero una ignición silenciosa en un punto, luego expansión local y, después, diseminación por todo el cuerpo.
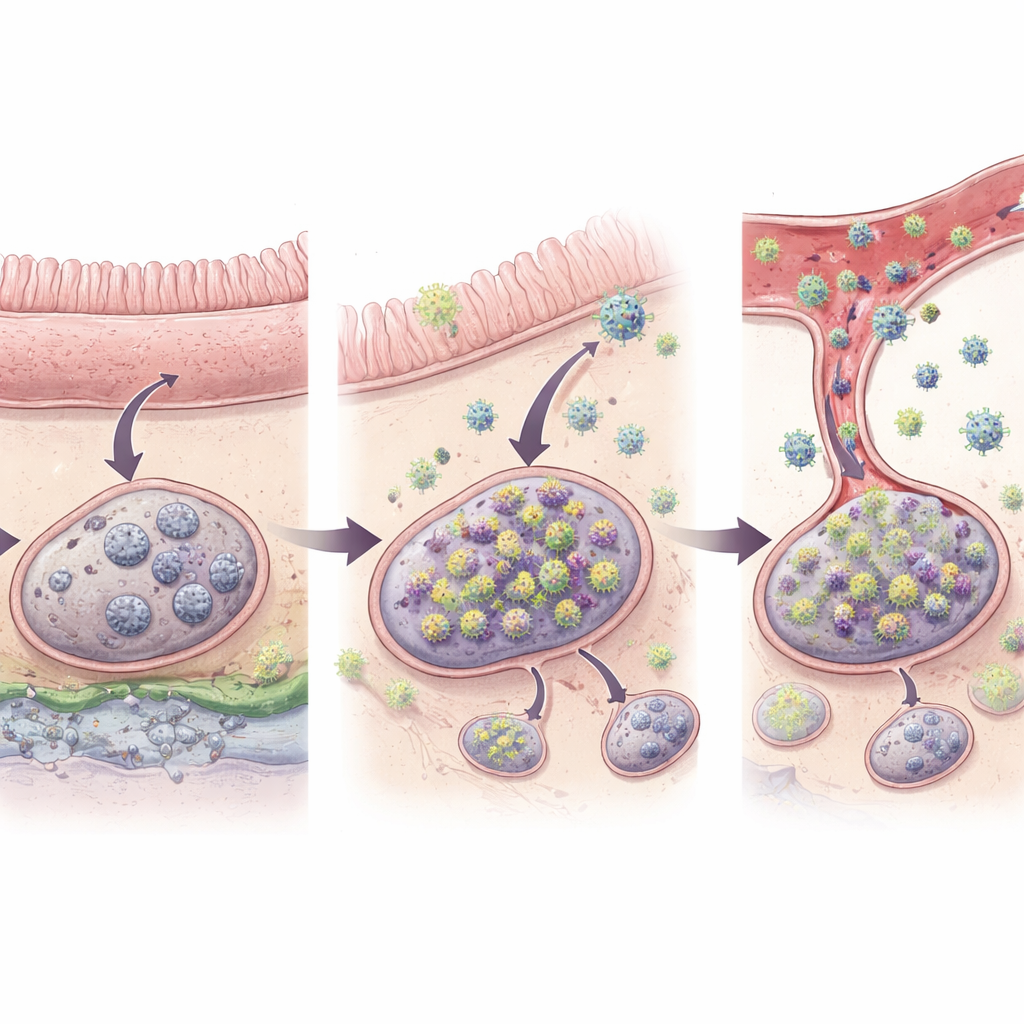
Por qué el intestino importa más
Un hallazgo fue especialmente llamativo: casi todos los eventos tempranos de rebrote se remontaron al tracto digestivo y a los tejidos inmunitarios que lo sirven. De los 27 códigos considerados orígenes genuinos del rebrote, el 96% estaban en los intestinos mismos o en ganglios linfáticos asociados al intestino, como los ganglios mesentéricos que drenan el intestino delgado y grueso. Solo un sitio de origen apareció en un ganglio no vinculado al intestino, y no se identificaron orígenes en órganos como hígado, pulmón o médula ósea. Los análisis estadísticos mostraron que, incluso teniendo en cuenta cuántas células infectadas había, los tejidos linfoides asociados al intestino tenían aproximadamente diez veces más probabilidad que otros sitios linfoides de dar lugar a virus reactivados. El entorno único del intestino —constantemente expuesto a alimentos y microbios y a menudo inflamado en infecciones similares al VIH— podría mantener allí las células infectadas más activas y más proclives a reanudar la producción viral.
Qué significa esto para futuras curas
En pocas palabras, este trabajo sostiene que, cuando se detienen antivirales potentes similares a los del VIH, el virus casi siempre se reactiva desde unos pocos reservorios ocultos en y alrededor del intestino, en lugar de hacerlo por igual desde todos los rincones del cuerpo. Al principio, estos brotes son pequeños y están confinados a un parche de tejido, pero una vez que el virus alcanza la sangre y órganos distantes, las cantidades aumentan rápidamente. Para los esfuerzos dirigidos a la remisión a largo plazo o la cura, esto implica que las terapias deben alcanzar y actuar eficazmente en los tejidos inmunitarios del intestino. Herramientas que permitan visualizar o muestrear estos sitios de difícil acceso en personas, o fármacos diseñados específicamente para actuar allí, podrían ser clave para evitar que las primeras chispas del rebrote lleguen a prenderse.
Cita: Keele, B.F., Okoye, A.A., Immonen, T.T. et al. Initial sites of SIV rebound after antiretroviral treatment cessation in rhesus macaques. Nat Microbiol 11, 648–663 (2026). https://doi.org/10.1038/s41564-025-02258-3
Palabras clave: Rebrote de VIH, reservorios virales, tejido linfoide intestinal, modelo de macaco rhesus, interrupción de la terapia antirretroviral