Clear Sky Science · es
Análisis comparativo de conjuntos de datos de escaneo mutacional profundo en enterovirus A y B identifica divergencia funcional y dianas terapéuticas
Por qué nos importan los virus de ARN diminutos
Los enterovirus son un gran grupo de diminutos virus de ARN que circulan de forma silenciosa por todo el mundo, causando por lo general resfriados leves o gastroenteritis, pero a veces desencadenando parálisis, daño cardíaco u otras enfermedades graves. Contamos con pocas vacunas y aún menos fármacos de acción amplia contra ellos, en parte porque estos virus evolucionan con gran rapidez. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones prácticas: cuando estos virus mutan, ¿qué partes de su maquinaria pueden cambiar con libertad y qué partes son tan vitales que la evolución las mantiene casi inmóviles? Las respuestas señalan nuevas estrategias para diseñar tratamientos difíciles de eludir por el virus.
Leyendo el libro de instrucciones del virus, mutación a mutación
Los investigadores se centraron en dos enterovirus humanos que causan enfermedades muy distintas: el enterovirus A71, vinculado a enfermedades neurológicas graves en niños, y el coxsackievirus B3, asociado a inflamación cardíaca e incluso cáncer pancreático. Usando una técnica llamada escaneo mutacional profundo, crearon bibliotecas virales en las que casi cada posición de las proteínas de cada virus fue cambiada sistemáticamente. Estos virus mutantes se permitieron infectar células en cultivo y se utilizó secuenciación de alto rendimiento para medir cómo cada cambio afectaba al crecimiento viral. Al comparar cada mutante con el virus original, el equipo construyó un mapa detallado de qué sitios del proteoma viral toleran el cambio y cuáles están fuertemente constreñidos. 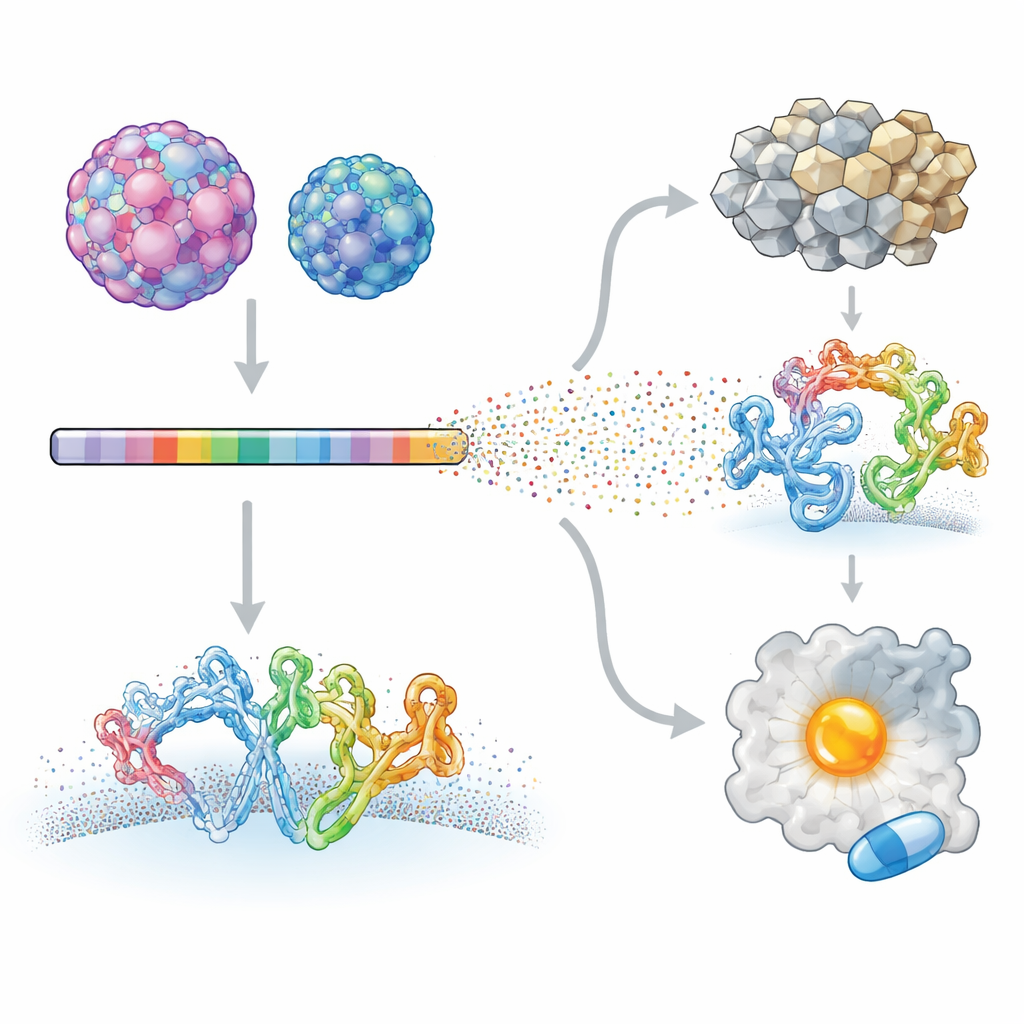
Límites rígidos compartidos y flexibilidad específica de cada virus
A pesar de compartir solo alrededor de la mitad de sus secuencias de aminoácidos, los dos virus mostraron patrones generales de constricción notablemente similares. Las «caballos de trabajo» enzimáticos internos que copian el genoma, cortan proteínas virales y desenrollan ARN fueron muy sensibles a la mutación en ambos virus. Del mismo modo, las superficies ocultas que mantienen unido el caparazón proteico, o cápside, resultaron difíciles de modificar sin dañar al virus. En contraste, muchas regiones orientadas hacia el exterior e implicadas en la interacción con el huésped fueron más libres de cambiar y a menudo diferían de forma notable entre las dos especies. El análisis estructural mostró que las regiones conservadas e intolerantes a mutaciones se agrupan alrededor de sitios activos e interfaces de ensamblaje, mientras que las regiones que contactan receptores, membranas o moléculas inmunes son focos de flexibilidad específica por especie.
Cómo los virus se unen a las células y esquivan las defensas
El equipo se fijó entonces en el apretón molecular entre virus y huésped. El enterovirus A71 y el coxsackievirus B3 usan diferentes receptores celulares para entrar y el estudio encontró que las huellas de contacto exactas en la superficie de la cápside están entre las regiones más divergentes en términos de tolerancia a mutaciones. Los residuos que sujetan el receptor en un virus están fuertemente constreñidos en ese virus pero son relativamente permisivos en el otro, reflejando cómo cada uno ha afinado su plataforma de acoplamiento. Una divergencia similar surgió en una pequeña proteína ligada a la membrana llamada 3A, que ayuda a remodelar membranas celulares y reclutar factores del huésped para la replicación del genoma. El modelado sugirió que los dos virus usan parches de contacto parcialmente distintos en 3A para enganchar el mismo factor hospedador, GBF1, y que además pueden insertar esta proteína en las membranas a diferentes profundidades. Estas diferencias ayudan a explicar por qué virus estrechamente relacionados pueden infectar diferentes tejidos y provocar patrones de enfermedad distintos.
Lo que la evolución en el laboratorio no capta—y lo que sí acierta
Para situar sus experimentos en cultivo celular en un contexto del mundo real, los autores compararon sus mapas mutacionales con miles de secuencias virales naturales procedentes de muestras de pacientes. En general, los sitios flexibles en el laboratorio tendieron también a ser variables en la naturaleza, especialmente en comparaciones a nivel de especies más amplias. Sin embargo, cuando examinaron qué aminoácidos específicos eran preferidos en cada sitio, la evolución natural y la selección en el laboratorio concordaron con mayor exactitud dentro de un mismo tipo viral. Cabe destacar que los mayores desajustes se concentraron en la superficie externa de la cápside y en regiones que interactúan con el huésped de las proteínas no estructurales 2A y 3A—precisamente donde se espera que las respuestas inmunes y los entornos complejos del huésped importen más. Esto sugiere que el escaneo mutacional profundo captura las limitaciones mecánicas básicas de las proteínas virales, mientras que las infecciones reales superponen presiones adicionales debidas a la inmunidad y la tropismo tisular que son más difíciles de reproducir in vitro.
Encontrar un punto débil compartido para futuros fármacos
Por último, los investigadores preguntaron si estos mapas podían destacar un talón de Aquiles común para el desarrollo de fármacos. Usando herramientas computacionales, buscaron en ambos virus bolsillos en las superficies proteicas que, en principio, podrían unirse a pequeñas moléculas. Luego superpusieron los datos mutacionales para ver qué bolsillos estaban formados por residuos que el virus no puede cambiar fácilmente sin perjudicarse. Un bolsillo, ubicado en la helicasa 2C—un motor en forma de anillo que ayuda a desenrollar el ARN viral—sobresalió. Su forma y los residuos que lo constituyen están altamente conservados entre cuatro principales especies humanas de enterovirus, se sitúa alejado de sitios activos ya conocidos, y los cambios allí son poco frecuentes en la naturaleza y fuertemente perjudiciales en pruebas de laboratorio. 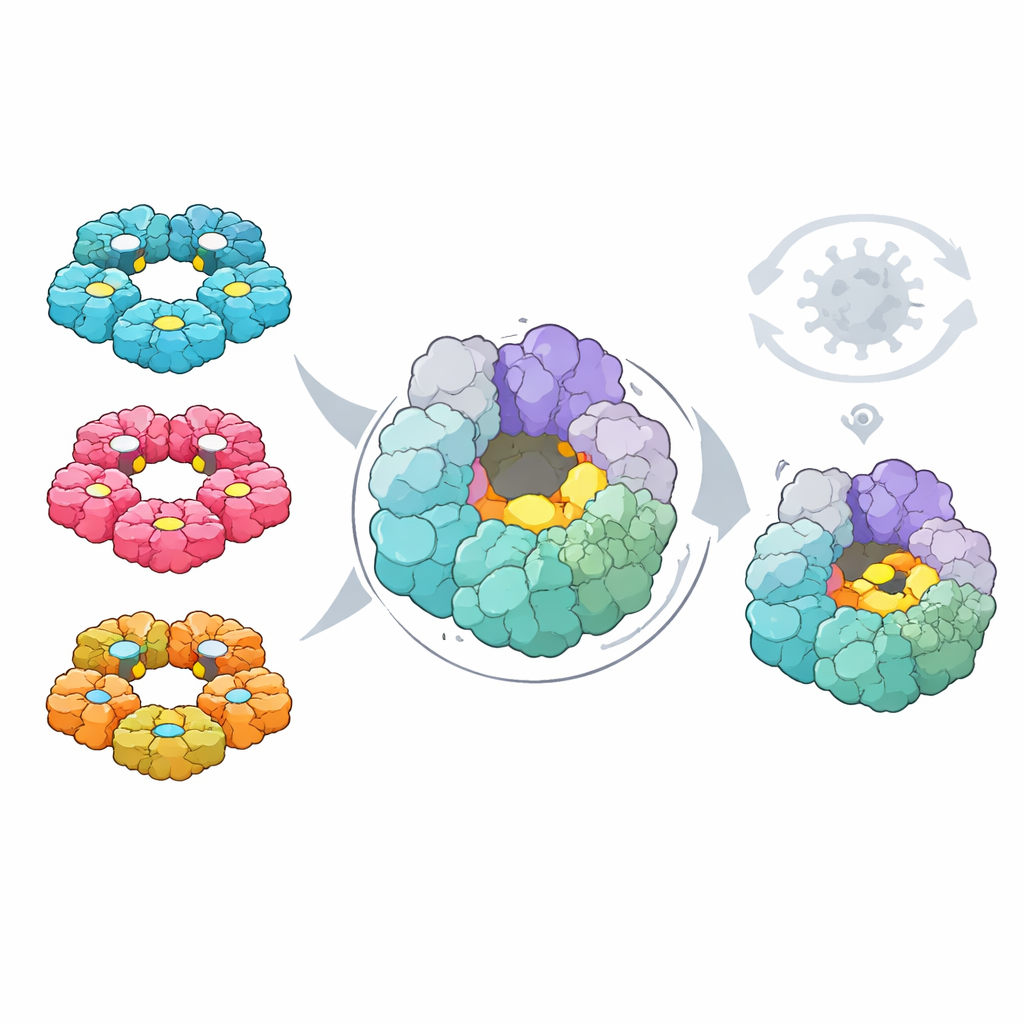
Qué significa esto para futuros tratamientos
Al sondear sistemáticamente cómo afecta cada posible cambio de una sola letra a dos enterovirus importantes, este estudio revela una clara división entre un núcleo compartido y rígido de la maquinaria viral y superficies más flexibles y específicas de cada virus que interaccionan con el huésped. El núcleo conservado incluye un bolsillo recientemente destacado en la helicasa 2C que parece difícil de mutar para el virus sin sacrificar aptitud, lo que lo convierte en una diana atractiva para antivirales de amplio espectro con alta barrera a la resistencia. Al mismo tiempo, las superficies externas y los sitios de contacto con el huésped, más adaptables, explican por qué virus relacionados se comportan de forma tan diferente en el organismo y señalan dónde las vacunas y las terapias basadas en la inmunidad deberán afrontar la rápida evolución. En conjunto, estos hallazgos proporcionan una hoja de ruta para diseñar tratamientos que exploten los propios límites evolutivos del virus.
Cita: Álvarez-Rodríguez, B., Bakhache, W., McCormick, L. et al. Comparative analysis of deep mutational scanning datasets in enteroviruses A and B identifies functional divergence and therapeutic targets. Nat Ecol Evol 10, 467–480 (2026). https://doi.org/10.1038/s41559-026-02993-8
Palabras clave: enterovirus, evolución viral, escaneo mutacional profundo, dianas antivirales, helicasa 2C