Clear Sky Science · es
Vías nativas de H2 permiten la hidrogenación biocompatible de alquenos metabólicos en bacterias
Convertir microbios en pequeñas fábricas ecológicas
Imagine si bacterias comunes del intestino pudieran ayudar a sustituir los combustibles fósiles en la fabricación de productos cotidianos—desde conservantes alimentarios hasta plásticos—mientras incluso aprovechan los residuos alimentarios. Este estudio muestra que cepas de laboratorio corrientes de Escherichia coli pueden hacer precisamente eso: generan hidrógeno dentro de sus células de forma natural, y ese hidrógeno puede aprovecharse en la superficie celular para impulsar reacciones químicas de estilo industrial bajo condiciones suaves y acuosas. Al emparejar microbios vivos con un catalizador metálico sólido, los investigadores trazan un camino hacia una fabricación más limpia y con menor huella de carbono.
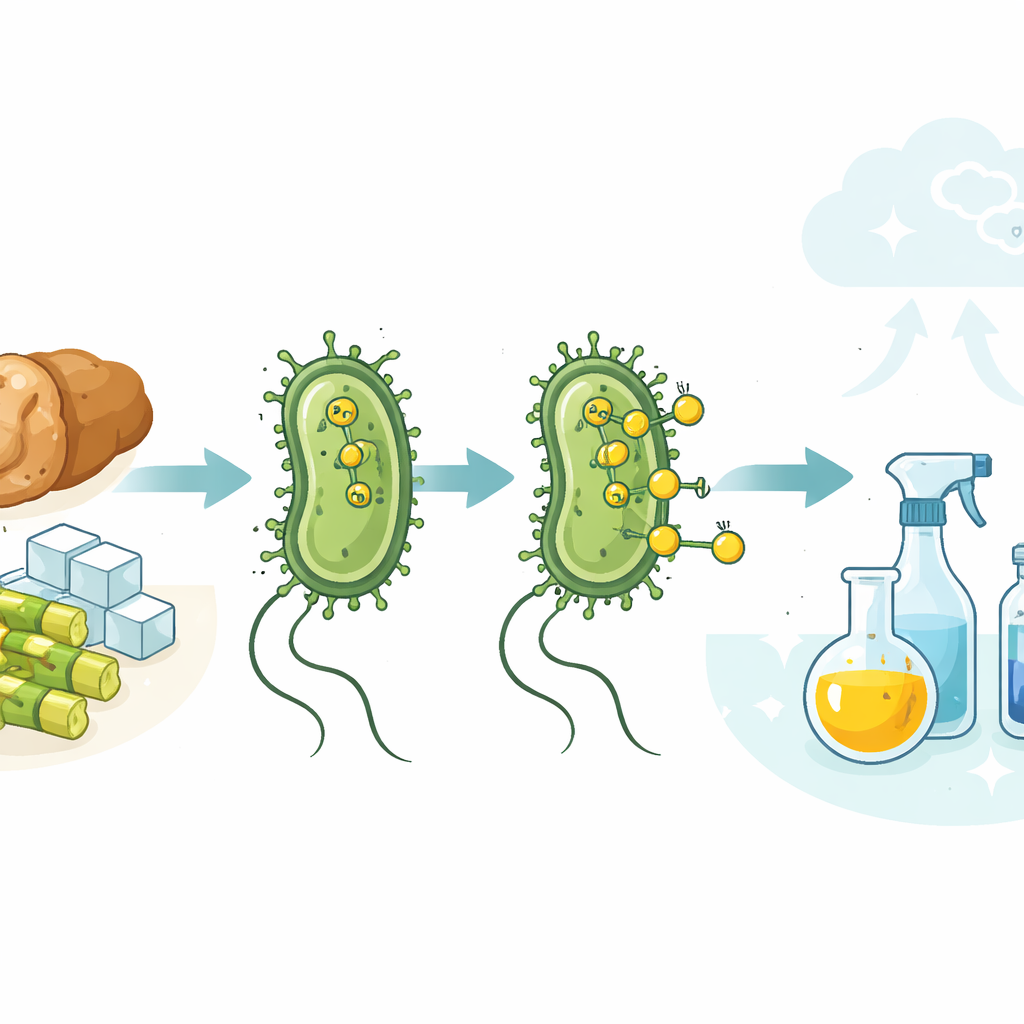
Por qué el hidrógeno importa para los productos cotidianos
El gas hidrógeno está en el centro de la química moderna. Se usa para transformar aceites líquidos en untables, mejorar combustibles crudos y fabricar muchos ingredientes de medicamentos y plásticos. Hoy en día, casi todo ese hidrógeno procede de combustibles fósiles, principalmente gas natural y carbón, liberando grandes cantidades de dióxido de carbono. Al mismo tiempo, muchos microbios expulsan hidrógeno de forma natural al descomponer azúcares cuando el oxígeno es escaso. El reto que abordan los autores es cómo aprovechar este flujo de hidrógeno biológico y suave para impulsar el tipo de reacciones que la industria actualmente realiza con altas presiones, disolventes orgánicos y gas de origen fósil.
Permitir que las bacterias alimenten un catalizador metálico
El equipo se centró en reacciones simples de adición de hidrógeno, donde un doble enlace en una molécula se “satura” con hidrógeno. Hicieron crecer varias cepas no modificadas de E. coli en medios a base de azúcar y añadieron un catalizador de paladio finamente disperso compatible con células vivas. En condiciones sin oxígeno, el metabolismo nativo de las bacterias convirtió el azúcar en formiato y después en gas hidrógeno en la cara interna de la membrana celular. La microscopía mostró que las partículas de catalizador, con carga positiva, se asientan sobre la superficie celular cargada negativamente, donde se encuentran con el hidrógeno que escapa. Allí, el metal usa el hidrógeno microbiano para reducir una molécula de prueba, el ácido cafeico, a su producto saturado con rendimientos muy altos—con frecuencia mejores que los obtenidos con una cepa previamente y fuertemente modificada.
Ampliando el abanico de productos y materias primas
Una vez que la reacción básica funcionó, los investigadores probaron una amplia gama de moléculas que contienen dobles enlaces carbono–carbono, incluidas ácidos de origen vegetal y compuestos grasos de cadena larga. Muchas se convirtieron sin problemas a sus formas saturadas, algunas casi en rendimientos cuantitativos. También construyeron cepas de E. coli que producen más hidrógeno desviando mayor flujo metabólico hacia la vía nativa formadora de hidrógeno. Estas cepas potenciadas permitieron conversiones similares con menos catalizador metálico. En un giro llamativo, el equipo reemplazó el azúcar pura por pan rancio licuado como fuente de alimento. Enzimas descompusieron el pan en glucosa, que las bacterias fermentaron con igual eficacia, convirtiendo un residuo alimentario común tanto en hidrógeno biológico como en productos químicos de mayor valor.
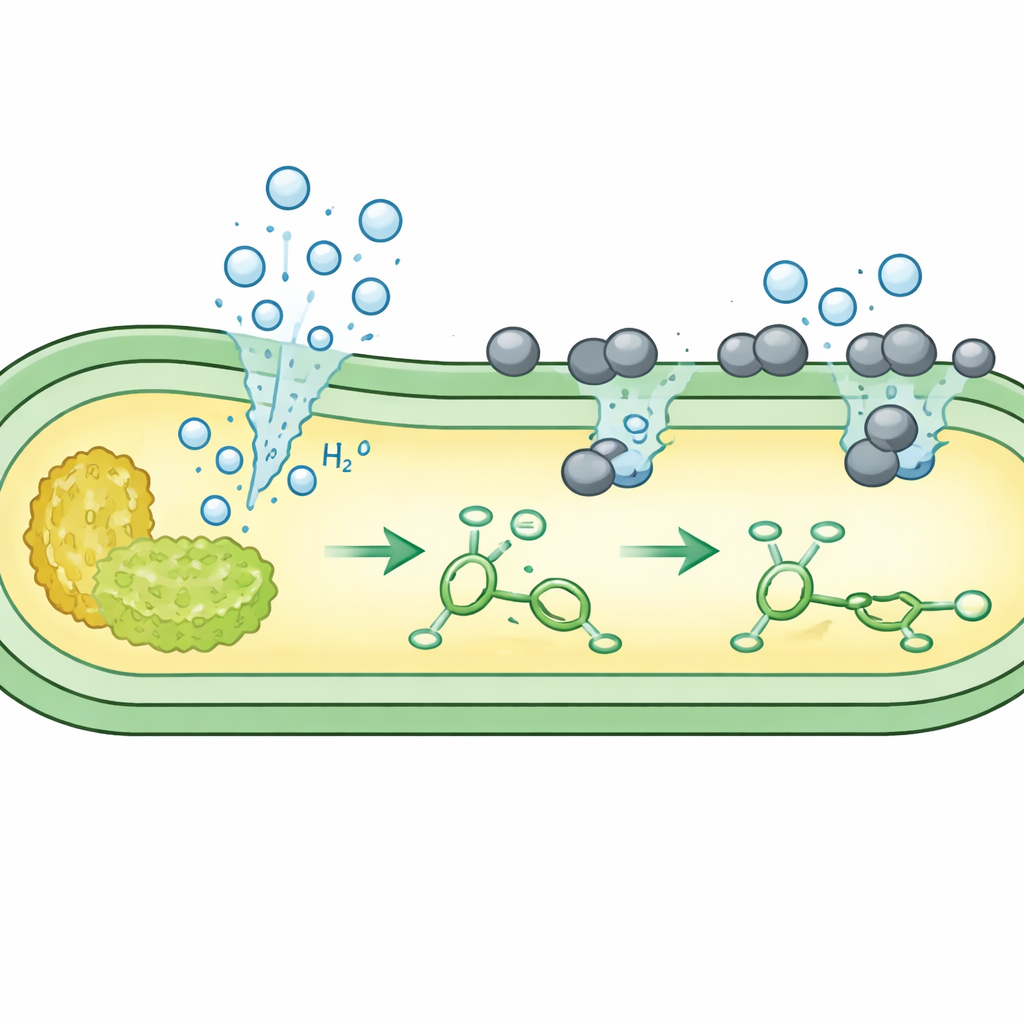
Producir tanto ingrediente como combustible dentro de una sola célula
Acto seguido, los autores se preguntaron si una sola bacteria podría fabricar no solo el «reactivo» hidrógeno sino también el «sustrato» insaturado que debía modificar. Ingenierizaron E. coli para que el azúcar fluya primero hacia vías que producen bloques aromáticos como los ácidos cinámico y coumáreo, y hacia otra vía que produce hidrógeno. Cuando el cultivo acumuló estos metabolitos internos, añadieron el catalizador de paladio. En la superficie celular, el catalizador usó el hidrógeno in situ para convertir los metabolitos recién formados con dobles enlaces en productos completamente saturados como ácido hidrocínamico, desaminotirosina y ácido adípico, un precursor clave del nailon. En algunos diseños, esta cometabolización alcanzó conversiones casi completas, todo ello dentro del mismo cultivo vivo.
Medir el beneficio climático
Para comprobar si esta bioquímica ingeniosa realmente ayuda al planeta, el equipo realizó una evaluación del ciclo de vida comparando su enfoque híbrido «quimio‑microbiano» con rutas estándar de hidrogenación impulsadas por hidrógeno de origen fósil o electrolítico. Cuando el hidrógeno biológico y la producción intracelular de sustratos se combinaron en un solo proceso eficiente térmicamente, las emisiones totales de gases de efecto invernadero cayeron notablemente. Usar pan de desecho como materia prima impulsó aún más el sistema: al evitar vertederos o incineración y convertir alimentos descartados en productos químicos, algunos escenarios resultaron en balance neto de carbono negativo, es decir, eliminan más gases de efecto invernadero de los que emiten.
Qué significa esto para la fabricación futura
En términos sencillos, el estudio demuestra que bacterias cotidianas pueden inducirse a actuar tanto como fuente de energía como fábrica de ingredientes para reacciones químicas importantes, mientras que un metal sólido en su superficie remata silenciosamente la transformación. Dado que todo ocurre en agua, a temperaturas cercanas a la corporal y usando azúcares renovables o de desecho, este enfoque podría algún día ofrecer alternativas más limpias a las plantas petroquímicas tradicionales. Con ingeniería adicional de vías microbianas y catalizadores, esta plataforma de células vivas podría permitir una nueva generación de procesos sostenibles que conviertan carbono renovable y alimentos descartados en productos útiles con una huella climática mucho menor.
Cita: White, M.F.M., Trotter, C.L., Steele, J.F.C. et al. Native H2 pathways enable biocompatible hydrogenation of metabolic alkenes in bacteria. Nat. Chem. 18, 535–543 (2026). https://doi.org/10.1038/s41557-025-02052-y
Palabras clave: hidrógeno microbiano, química verde, biocatálisis, residuos a productos químicos, fabricación sostenible