Clear Sky Science · es
Pseudo-productos naturales monovalentes sobrecargan la degradación de IDO1 por su E3 nativa KLHDC3
Apagando una enzima favorable al cáncer
Nuestro sistema inmune vigila constantemente en busca de células cancerosas, pero los tumores con frecuencia contraatacan secuestrando la propia química del cuerpo. Un actor clave en esta lucha es una enzima llamada IDO1, que ayuda a los tumores a desactivar las células inmunitarias. Este estudio describe una nueva clase de pequeñas moléculas que hacen más que bloquear la actividad de IDO1: persuaden a las células para que eliminen la enzima por completo. Al aprovechar la maquinaria celular natural de eliminación de desechos, estos compuestos podrían reactivar los ataques inmunitarios contra los tumores de maneras que los fármacos anteriores no lograron.
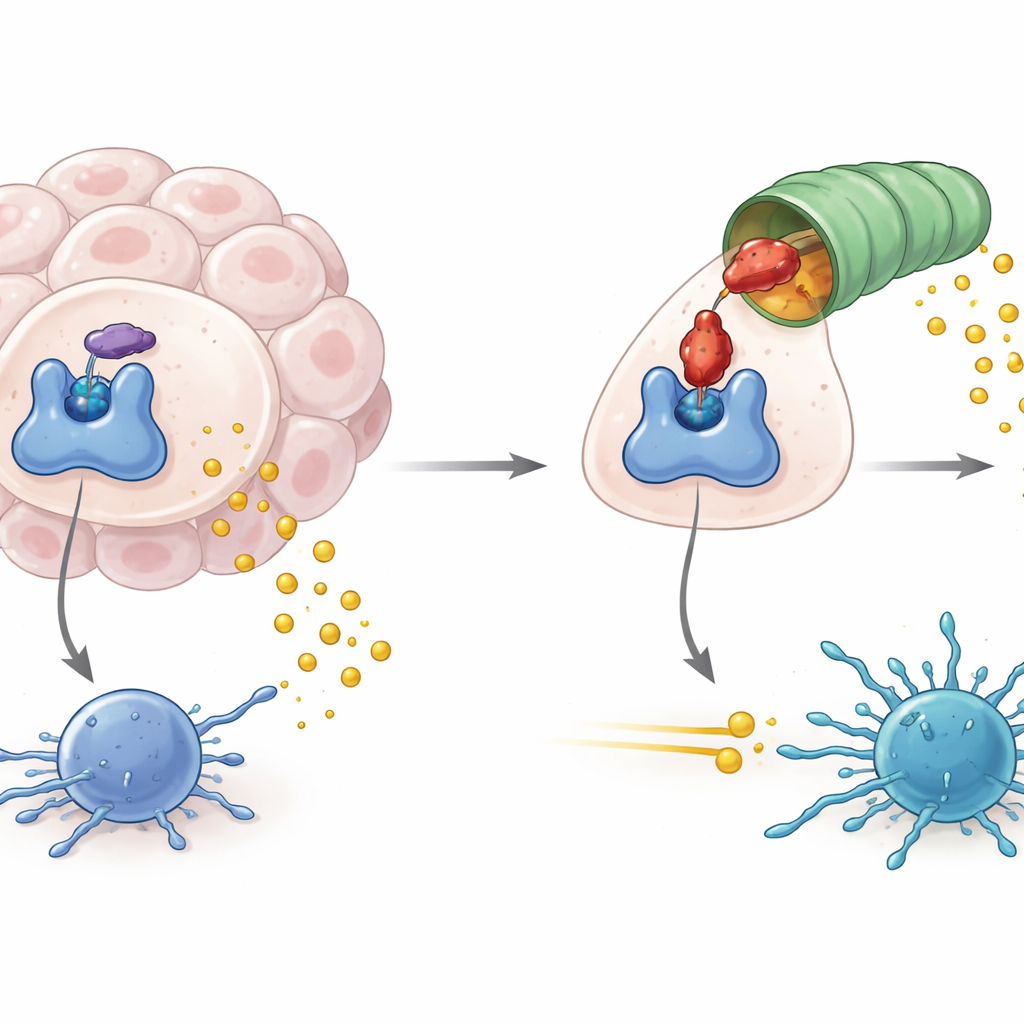
Cómo los tumores explotan a un guardián metabólico
IDO1 se sitúa en el punto de entrada de una vía metabólica que descompone el aminoácido triptófano en un producto llamado quinurenina. Cuando IDO1 es abundante y está activo, los niveles de triptófano caen y la quinurenina aumenta, creando un entorno químico que atenúa la actividad de las células inmunitarias, incluidas las células T antitumorales. Una alta actividad de IDO1 se ha asociado no solo con una inmunidad antitumoral más débil, sino también con linfomas inducidos por virus y algunas formas de neurodegeneración. Por ello, los desarrolladores de fármacos se han centrado en bloquear la actividad enzimática de IDO1, con la esperanza de cortar esta señal inmunosupresora y ayudar a que las inmunoterapias contra el cáncer existentes funcionen mejor.
Por qué los simples inhibidores enzimáticos se han quedado cortos
A pesar de resultados prometedores en animales, los ensayos clínicos de los inhibidores tradicionales de IDO1 han sido decepcionantes. Una explicación emergente es que IDO1 es más que un simple catalizador. Incluso cuando su química está bloqueada, la proteína en sí puede actuar como un centro de señalización que sigue promoviendo el crecimiento y la diseminación tumoral. Algunos inhibidores incluso estabilizan a IDO1, aumentando la cantidad de proteína presente en las células. En otras palabras, apagar solo la función catalítica puede dejar intactos sus roles pro-tumorales no enzimáticos—o, peor aún, puede llegar a reforzarlos.
Diseñando compuestos que desencadenan la autodestrucción
Los autores exploraron una gran biblioteca de moléculas “pseudo-naturales”: compuestos sintéticos construidos a partir de fragmentos inspirados en productos naturales pero recombinados de formas nuevas. Encontraron una familia de moléculas, denominadas iDegs, derivadas de un bloque constructivo de tipo vegetal llamado (−)-myrtanol. Estos compuestos se unen dentro del bolsillo habitual de IDO1 para su cofactor que contiene hierro, el hemo. Al desplazar el hemo, los iDegs tanto debilitan la capacidad de IDO1 para producir quinurenina como, crucialmente, remodelan parte de la región terminal de la proteína. Estructuras cristalográficas de alta resolución revelan que cuando los iDegs ocupan el sitio del hemo, aflojan y desordenan parcialmente una hélice C-terminal que normalmente se mantiene en una conformación compacta y protegida.
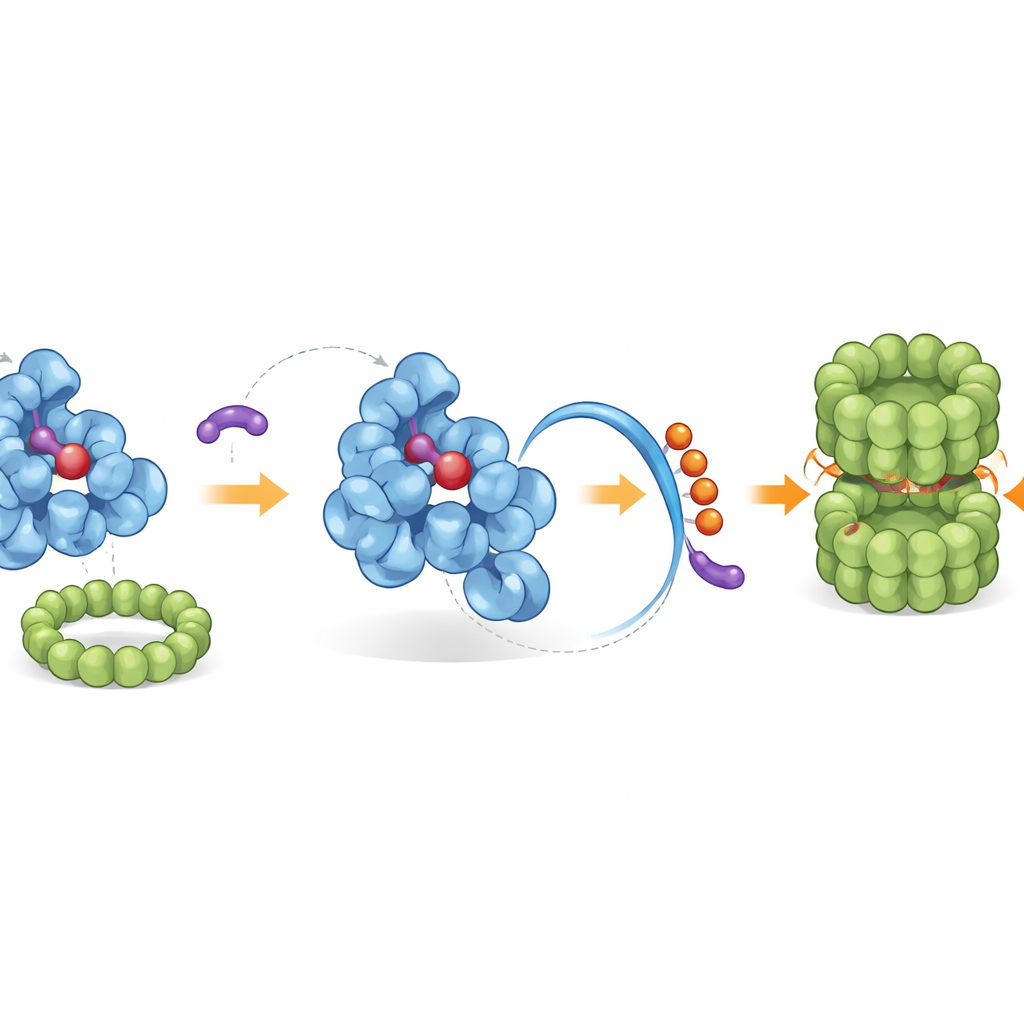
Reclutando al equipo de limpieza nativo de la célula
La cola reconfigurada expone una “etiqueta final” incorporada que la maquinaria de eliminación celular reconoce. Mediante cribados genéticos y reconstrucción bioquímica, los investigadores identificaron un complejo ligasa específico, llamado CRL2–KLHDC3, que de forma natural une pequeñas “banderas” de ubiquitina a la cola expuesta de IDO1, marcándola para su destrucción por el proteasoma—la trituradora molecular de la célula. En condiciones normales, solo la forma libre de hemo de IDO1 se etiqueta de forma eficiente de este modo, mientras que la IDO1 unida al hemo está protegida. Los iDegs inclinan este equilibrio al unirse solo a la forma libre de hemo, amplificando la vía natural de degradación. Miembros potentes de la serie no solo bloquean la producción de quinurenina, sino que también aumentan el marcado con ubiquitina sobre IDO1 y reducen drásticamente sus niveles proteicos en varios tipos de células cancerosas.
Cambiando el destino de IDO1—y las respuestas inmunitarias
Este comportamiento de doble acción tiene importantes consecuencias funcionales. En ensayos de migración con células de cáncer de ovario, un inhibidor de IDO1 explorado clínicamente que estabiliza la enzima en realidad aceleró el movimiento celular, en consonancia con el papel no enzimático y pro-tumoral de IDO1. Por el contrario, un compuesto iDeg ralentizó la migración, coherente tanto con la inhibición enzimática como con la pérdida de la proteína en sí. El estudio descubre así una nueva forma de manipular IDO1: no arrastrándola forzosamente hacia una ligasa ajena con una molécula diseñadora voluminosa, sino “sobrealimentando” una vía de degradación nativa que ya existe en las células.
Lo que esto podría significar para futuras terapias contra el cáncer
Para los no especialistas, el mensaje clave es que la calidad—no solo la cantidad—de la inhibición enzimática importa. Estas nuevas pequeñas moléculas actúan como interruptores de precisión: bloquean a IDO1 en una conformación vulnerable que la célula está predispuesta a destruir, cortando tanto sus contribuciones metabólicas como sus funciones de señalización al soporte tumoral. Dado que los iDegs son compactos, con propiedades similares a las de un fármaco y dependen de la ligasa propia de la célula para la eliminación de IDO1, pueden ofrecer un enfoque más sutil y de aplicación más amplia que los anteriores fármacos “degradadores de proteínas”. Si estrategias similares pueden aplicarse a otras proteínas problemáticas, este trabajo apunta a una nueva generación de terapias que incitan a las células enfermas a desmantelar sus propias armas moleculares.
Cita: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
Palabras clave: IDO1, inmunoterapia contra el cáncer, degradación dirigida de proteínas, ligasa de ubiquitina, degradadores de pequeña molécula