Clear Sky Science · es
Equilibrio de ligandos biocompatibles en coordinación de metales de transición permite arilación proteica in situ inocua
Convertir metales en herramientas suaves para las células
Muchas reacciones químicas poderosas dependen de metales, pero si acercas esos mismos metales a células vivas normalmente surge un problema: daño, estrés y muerte celular. Este estudio demuestra que, con la “presa” molecular adecuada alrededor de un átomo de níquel, es posible ejecutar una reacción sofisticada dentro de células vivas sin dañarlas. Ese avance permite a los científicos marcar miles de puntos específicos en proteínas e incluso seguir la aparición de patógenos difíciles de rastrear, abriendo nuevas vías para mapear lo que realmente ocurre dentro de las células en salud y enfermedad.
Por qué los metales son a la vez aliados y enemigos
El níquel y otros metales ya actúan discretamente en nuestro organismo como parte de enzimas naturales, pero también pueden ser tóxicos si se unen en lugares erróneos. La naturaleza lo resuelve rodeando los metales con pequeñas moléculas y proteínas cuidadosamente seleccionadas, que los dirigen hacia los dianas correctas y bloquean reacciones no deseadas. Los químicos, en cambio, suelen emplear reactivos metálicos extremadamente reactivos y nada adaptados a la vida. Estos han sido herramientas excelentes para construir moléculas complejas en un matraz, pero demasiado agresivos para usar dentro de células, sobre todo cuando el objetivo es añadir una pequeña “etiqueta” a un aminoácido concreto de una proteína sin alterar el resto de la célula.
Diseñando un reactivo de níquel más amable
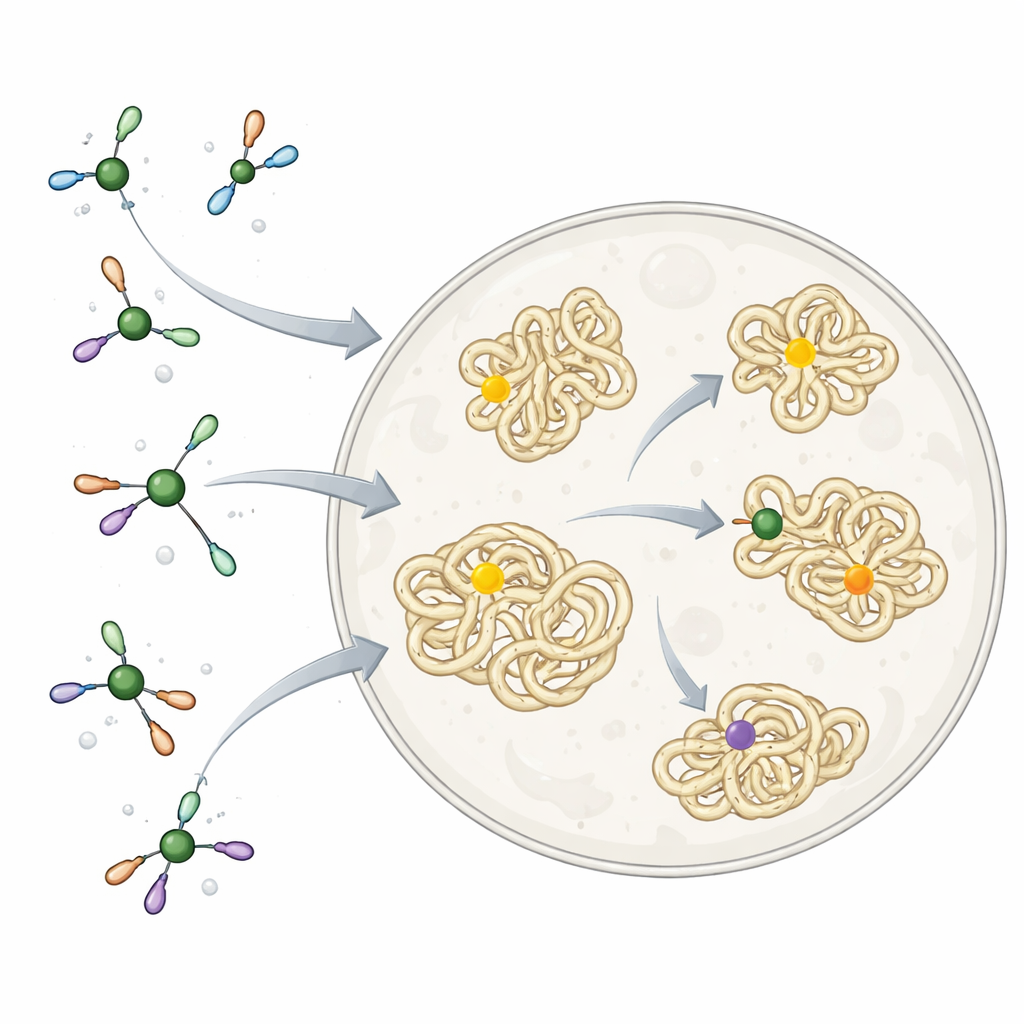
Los investigadores se inspiraron en la forma en que las propias células manejan el níquel. Construyeron una serie de complejos de níquel envueltos en un ligando simple y biocompatible llamado TMEDA. Esta pequeña molécula actúa como una abrazadera blanda: lo bastante ajustada para evitar que el níquel se adhiera a componentes celulares inapropiados, pero lo bastante laxa para permitir que realice la reacción clave. La reacción une un fragmento “arilo” —un grupo plano en forma de anillo frecuente en fármacos— al átomo de azufre del aminoácido cisteína en proteínas. En proteínas purificadas en solución, estos complejos de níquel adhirieron grupos arilo muy rápida y selectivamente a sitios individuales de cisteína, y funcionaron en muchas conformaciones y posiciones proteicas distintas, mostrando que la química era ampliamente compatible con moléculas biológicas reales.
Editar proteínas dentro de células vivas
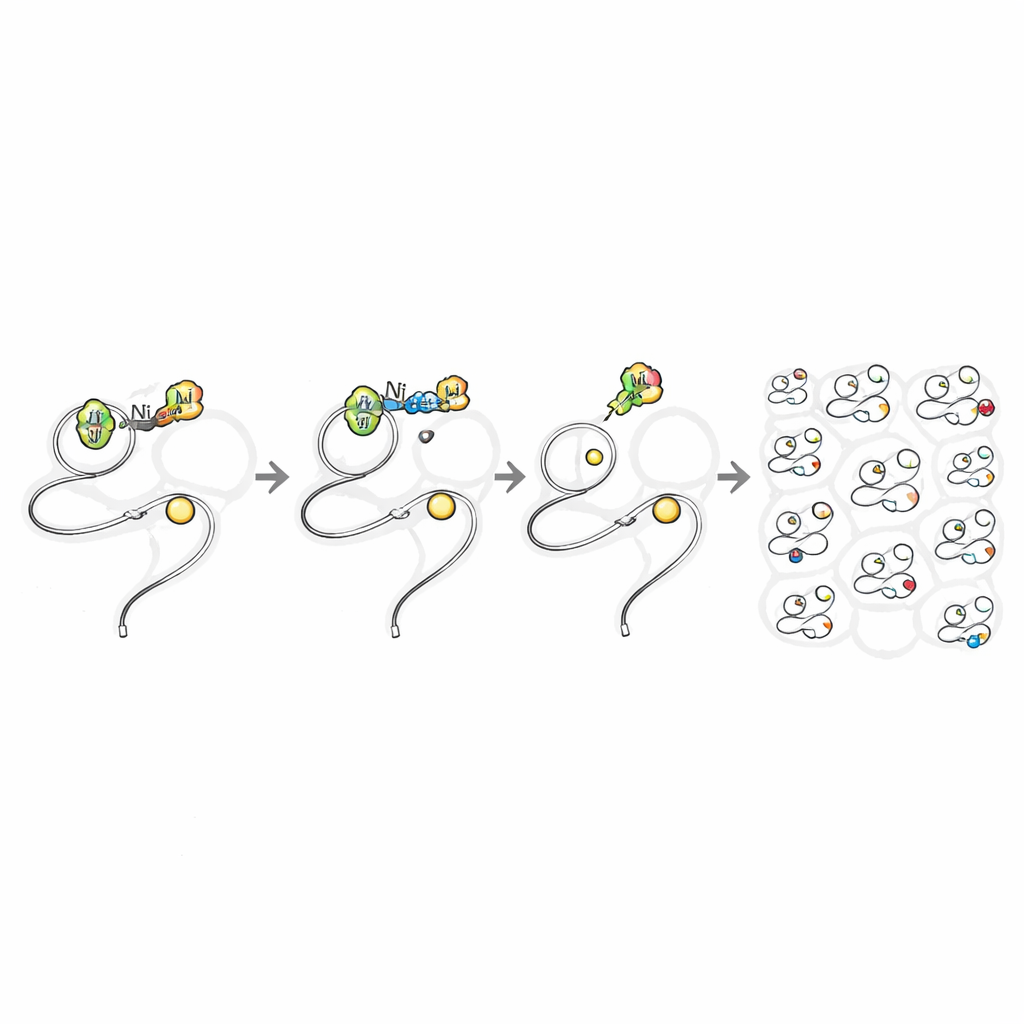
A continuación, el equipo preguntó si estos mismos reactivos podrían funcionar dentro de células vivas sin resultar venenosos. Compararon sales simples de níquel, conocidas por ser dañinas, con los complejos de níquel unidos a TMEDA. En células de mamífero, las fuentes sencillas de níquel provocaron una muerte celular sustancial a dosis relativamente bajas, pero los complejos con ligando equilibrado se mantuvieron bien tolerados incluso a concentraciones milimolares. Esa ventana de seguridad permitió a los investigadores exponer células bacterianas y de mamífero a los reactivos de níquel el tiempo suficiente para que entraran y modificaran proteínas. Al incorporar un “asa” azida en una versión del grupo arilo, pudieron acoplar después colorantes fluorescentes o etiquetas de biotina tras la reacción, revelando una tinción clara y dependiente de la dosis de proteínas por todo el citoplasma y el núcleo de células vivas.
Mapear sitios proteicos reactivos en todo el proteoma
Con una reacción in situ segura y rápida, los autores la convirtieron en una herramienta de descubrimiento. Trataron células humanas vivas con el reactivo de níquel portador de azida, luego utilizaron una biotina foto‑cleavable y espectrometría de masas avanzada para ver exactamente qué cisteínas habían sido modificadas. En un solo experimento detectaron casi 11.000 sitios de cisteína en casi 5.000 proteínas —aproximadamente el doble de proteínas que todos los estudios previos de perfilado de cisteínas en células vivas combinados. El marcado fue altamente selectivo para cisteína y mostró poco sesgo respecto a tipos de proteínas, localizaciones o sitios activos conocidos. De manera notable, muchas de las proteínas objetivo se consideraban “no ligandeables” según los estándares actuales de descubrimiento de fármacos, incluidos proteínas de señalización en baja abundancia y conmutadores redox sensibles que son difíciles de estudiar solo con genética.
Seguir patógenos ocultos en tiempo real
La misma química también demostró ser lo bastante sensible para detectar proteínas extrañas producidas durante la infección. En células humanas que portaban secuencias virales latentes, el método detectó factores de transcripción virales presentes a niveles extremadamente bajos, incluidas formas alternativas por empalme. El equipo infectó luego células con dos patógenos muy diferentes: la bacteria intracelular Chlamydia trachomatis y el virus Sindbis, un virus ARN relacionado con el chikunguña. Al aplicar el reactivo de níquel a las células infectadas en pulsos temporales, pudieron atrapar sitios de cisteína en proteínas ribosomales y reguladoras bacterianas clave mientras la bacteria cambiaba de etapa en su ciclo de vida, y en proteínas no estructurales virales críticas que impulsan la replicación del ARN. Esos sitios marcados destacan ahora como posibles puntos débiles para futuras estrategias antivirales o antibacterianas.
Qué significa esto para la química celular futura
Al equilibrar cuidadosamente la capa de ligandos alrededor del níquel, este trabajo muestra que un metal tradicionalmente riesgoso puede llevar a cabo una reacción covalente precisa de edición proteica en el interior de células vivas con un daño mínimo. Eso hace posible trazar un mapa funcional y detallado de sitios reactivos de cisteína en todo el proteoma, incluidas proteínas escasas, transitorias o difíciles de orientar con fármacos. También ofrece una forma de rastrear y sondar patógenos dentro de sus células hospedadoras a nivel de aminoácido. En términos más amplios, el estudio sugiere que muchas otras químicas metálicas “prohibidas” podrían domarse de forma similar, abriendo una nueva era en la que las poderosas herramientas de la química sintética operen de forma segura dentro de sistemas vivos.
Cita: Fu, X., Liu, W., Demyanenko, Y. et al. Biocompatible ligand balancing in transition metal coordination enables benign in-cell protein arylation. Nat. Chem. 18, 457–472 (2026). https://doi.org/10.1038/s41557-025-02017-1
Palabras clave: perfilado de cisteínas, bioconjugación con níquel, marcado de proteínas en células vivas, quimoproteómica, mapeo del proteoma de patógenos